
【题目】下列说法正确的是
A. 向BaCl2溶液中通入SO2可产生白色浑浊
B. 常温下,铁、铝不与浓硫酸反应,因此可用铁、铝容器贮存运输浓硫酸
C. 已知电离能力H2CO3>HClO>HCO3-,则向氯水中加入碳酸氢钠晶体,能提高溶液中HClO的浓度
D. 氯气有氧化性,可使干燥布条漂白褪色
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:
【题目】根据要求完成下列问题
(1)单质铝和氢氧化钠溶液反应的化学方程式_________________,本反应中的氧化剂是_______。
(2)实验室用二氧化锰和浓盐酸制取氯气的离子方程式_____________________。本反应中的氧化剂和还原剂的物质的量比为_____________________。
(3)二氧化硫和氯气按等物质的量通入足量水中的化学方程式_______________,本反应中若有1mol氧化剂参加反应则转移电子数目为_____________________。
(4)浓硝酸一般显黄色,用方程式解释原因:______________,可向浓硝酸中通入_______消除黄色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如下图所示。下列说法正确的是 ( )
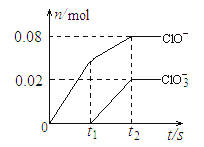
A. 苛性钾溶液中KOH的质量是5.6 g B. 反应中转移电子的物质的量是0.18mol
C. 在酸性条件下 ClO- 和ClO3-可生成Cl2 D. 一定有3.136 L氯气参与反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对反应A+B![]() AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应:
①20mL溶液中含A、B各0.01mol ②50mL溶液中含A、B各0.05mol
③0.1mol·L-1的A、B溶液各10mL ④0.5mol·L-1的A、B溶液各50mL
四者反应速率的大小关系是
A. ①>②>③>④ B. ④>③>②>①
C. ①>②>④>③ D. ②>①>④>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学气敏传感器可用于监测环境中NH3的含量,其工作原理如图所示,其中NH3被氧化为常见的无毒物质。下列说法错误的是( )

A. 溶液中OH-向电极a移动
B. 电极b上发生还原反应
C. 负极的电极反应为2NH3-6e-+6OH-![]() N2+6H2O
N2+6H2O
D. 理论反应消耗的NH3与O2的物质的量之比为3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金在生产和生活具有广泛的应用。下列用品中所用的材料不属于合金的是
A. 铁锅 (生铁) B. 铜壶(黄铜)
C. 高压锅(硬铝) D. 温度计(水银)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是
A.Na+、Mg2+、OH-、Cl-B.H+、Ca2+、CO32-、NO3-
C.K+、Zn2+、NO3-、SO42-D.Na+、HCO3-、OH-、Ba2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeS 与一定浓度的HNO3 反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO 和H2O,当NO2、N2O4、NO 的物质的量之比为1:1:2 时,实际参加反应的FeS 与被还原的HNO3的物质的量之比为 ( )
A. 1:4 B. 1:5 C. 1:6 D. 1:7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】哈大齐高铁的通车,标志我国高寒地区高铁技术领先世界,车厢大部分采用铝合金材料制造,这是因为铝合金
A. 质量轻,强度大,抗腐蚀能力比较强 B. 具有比较活泼的化学性质
C. 各种成分在自然界中含量丰富,容易获取 D. 比纯铝熔点高,耐高温
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com