
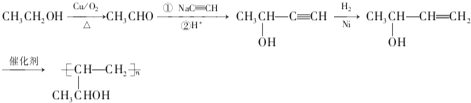
����Ŀ������أ�H�����������˷ܼ�����ϳ�·����ͼ��ʾ��NBS��һ��ѡ��������Լ���

��֪��CH3��C��CH+H2O![]() CH3COCH3
CH3COCH3
(1)A�Ľṹ��ʽ��_______��E�й����ŵ�����Ϊ___________________��
(2)��ӦB��C�ķ�Ӧ�������Լ���_______________���ݵķ�Ӧ������________��
(3)F�Ľṹ��ʽ��______________������أ�H�� �ķ���ʽ��________��
(4)д��C��D�Ļ�ѧ����ʽ______________________________________��
(5)������F�ķ�����ͬ���칹���ж��֣��ṹ���������£���FeCl3��Һ������ɫ��Ӧ���ܺ�������Һ����������Ӧ��������ֻ��������λȡ���������������Ҫ���ͬ���칹��ṹ��ʽ����Ϊ________________________________________��
(6)��������кϳ�����ͼ��������Ҵ�Ϊ��ʼ��ԭ�Ϻϳ�ǿ��ˮ����֬![]() �ĺϳ�·��______________(������ͼ��ʾ�������Լ����ܼ���ѡ)��
�ĺϳ�·��______________(������ͼ��ʾ�������Լ����ܼ���ѡ)��
���𰸡�![]() CH3 �ǻ���̼̼���� ��������ˮ��Һ������ �ӳɷ�Ӧ
CH3 �ǻ���̼̼���� ��������ˮ��Һ������ �ӳɷ�Ӧ ![]() C10H15NO
C10H15NO ![]()
![]()
��������
��E�Ľṹ��֪A�к��б���������NBS����ȡ����Ӧ����B��B�ķ���ʽΪC7H7Br��B����ˮ�ⷴӦ����C��C���Է���������Ӧ����D����AΪ![]() �� BΪ
�� BΪ![]() ��CΪ
��CΪ![]() ��DΪ
��DΪ![]() ��E�����ӳɷ�Ӧ����ˮ�õ�F�����
��E�����ӳɷ�Ӧ����ˮ�õ�F�����![]() ��֪FΪ
��֪FΪ![]() ��
��![]() �����������ӳɷ�Ӧ�õ�����أ�
�����������ӳɷ�Ӧ�õ�����أ�
(6)�Ҵ�����������ȩ����ȩ��NaC��CH��Ӧ���ữ�õ�![]() ���������������ӳɷ�Ӧ�õ�
���������������ӳɷ�Ӧ�õ�![]() ��������Ӿ۷�Ӧ����
��������Ӿ۷�Ӧ����![]() ��
��
(1) ��������ķ�����֪��AΪ![]() ��E�Ľṹ��ʽΪ
��E�Ľṹ��ʽΪ![]() ������������Ϊ�ǻ���̼̼������
������������Ϊ�ǻ���̼̼������
(2) ��ӦB��C��±�����ļ���ˮ�⣬���Է�Ӧ�������Լ�����������ˮ��Һ�����ȣ��ݵķ�Ӧ�����Ǽӳɷ�Ӧ��
(3) ������ķ�����֪��F�Ľṹ��ʽ��![]() �������(H)�Ľṹ��ʽΪ
�������(H)�Ľṹ��ʽΪ![]() �����ʽ��C10H15NO��
�����ʽ��C10H15NO��
(4) C��DΪ���ǻ��Ĵ�������������Ӧ�Ļ�ѧ����ʽΪ![]() ��
��
(5) ������F��ͬ���칹����FeCl3��Һ������ɫ��Ӧ��˵�����з��ǻ����ܺ�������Һ����������Ӧ��˵������ȩ����������ֻ��������λȡ�����������������Ľṹ��ʽ����Ϊ![]() ��
��
(6) �Ҵ�����������ȩ����ȩ��NaC��CH��Ӧ���ữ�õ�![]() ���������������ӳɷ�Ӧ�õ�
���������������ӳɷ�Ӧ�õ�![]() ��������Ӿ۷�Ӧ����
��������Ӿ۷�Ӧ����![]() ���ϳ�·������ͼΪ
���ϳ�·������ͼΪ ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijһ�ݻ�Ϊ5 L���ܱ������ڣ����� 0.2 mol��CO��0.2 mol��H2O���ڴ������ں�800���������¼��ȣ��������·�Ӧ��CO(g)+H2O(g)![]() CO2(g)+H2(g)����H��0��Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
CO2(g)+H2(g)����H��0��Ӧ��CO2��Ũ����ʱ��仯�������ͼ��
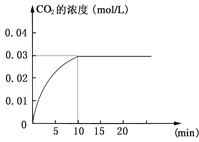
(1)������ͼ���ݣ���Ӧ��ʼ���ﵽƽ��ʱ��CO�Ļ�ѧ��Ӧ����Ϊv(CO)�� mol/(L��min)����Ӧ��ƽ��ʱ��c(H2)��____________mol/L�����¶��µ�ƽ�ⳣ��K= (��������)��
(2)�жϸ÷�Ӧ�ﵽƽ���������________________��
�� CO���ٵĻ�ѧ��Ӧ���ʺ�CO2���ٵĻ�ѧ��Ӧ�������
�� CO��H2O��CO2��H2��Ũ�ȶ����
�� CO��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
�� �����淴Ӧ���ʶ�Ϊ��
(3)��Ҫһ��ʼ����0.1 mol��CO��0.1 mol��H2O��0.1 mol�� CO2��0.1 mol��H2������ͬ�������£���Ӧ��ƽ��ʱ��c(H2O)��_____________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ӷ���ʽ�У���ȷ����()
�ٹ������Ƽ���ˮ�У�![]()
����С�մ�����θ����ࣺ![]()
��ʵ������ʯ��ʯ�����ᷴӦ��ȡ![]() ��
��![]()
��![]() ��
��![]() ��Ӧ��
��Ӧ��![]()
���Ȼ�����Һ�м�����![]()
��������![]() ͨ��NaOH��Һ��
ͨ��NaOH��Һ�� ![]()
A.�٢ۢܢ�B.�ڢ�C.�٢ڢۢ�D.�ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2��CH4���������Ʊ��ϳ������䷴Ӧ����ʾ��ͼ���£�
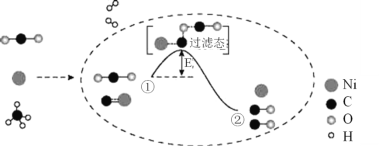
����˵���в���ȷ���ǣ� ����
A.Ni�Ǹ÷�Ӧ�Ĵ���
B.�����١�������̼�����Ķ��ѣ�����̼�������γ�
C.�����١��������ȷ�Ӧ
D.��Ӧ���ܻ�ѧ����ʽ�ɱ�ʾΪ��CH4 +CO2![]() 2CO+2H2
2CO+2H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ��ɱ���ܱ������г���2 mol A��1 mol B������Ӧ��mA(g) + nB(g) ![]() pC(g)����һ���¶��´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�������˵����ȷ����
pC(g)����һ���¶��´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ�����±�������˵����ȷ����
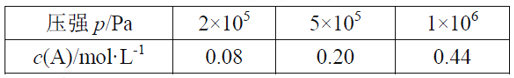
A. ά��ѹǿ2��105Pa������Ӧ��ʼ��5minʱ�ﵽƽ�⣬��v(A)=0.016mol/(L��min)
B. P��2��105Pa���ӵ�5��105Paʱ��ƽ�������ƶ�
C. PΪ1��106Paʱ��ƽ�ⳣ������ʽK=![]()
D. ����������ͬʱ������������ѹǿ�·ֱ����÷�Ӧ��A��ת������ʱ��仯������ͼ��ʾ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�Ϊ������Ԫ�أ�����������ŷֱ����һ��Ԫ�ء�(��˵���ⶼ�û�ѧ�������)
�� | �� | |||||||
�� | �� | �� | �� | �� | �� | �� | ||
(1)����Ԫ���н�������ǿ�ͷǽ�������ǿ��Ԫ�����Ʒֱ���______��_______��
(2)�ٺ͢ڵ���̬�⻯���ȶ��ԱȽ�(д��ѧʽ)��______________��
(3)������Ԫ����������������Ӧˮ����������ǿ����Ϊ_________��д���ݵ�����۵�����������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽΪ____________ ������H2�ڢ����ȼ�յ�����___________________��
(4)�����ϱ���ijһ��Ԫ�أ��䵥��ͨ�뵽��ɫʯ����Һ�е�����Ϊ�ȱ�����ɫ����Ԫ�������ڱ��е�λ����_________________��
(5)�ȽϢں͢۶�Ӧ�����ӵ����Ӱ뾶��С(����Ӧ���ӷ��ű�ʾ)________��
(6)д���۵�����������Ӧˮ����ĵ���ʽ___________���京�еĻ�ѧ��������____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���谢���ӵ�������ֵΪN![]() �����ڷ�Ӧ
�����ڷ�Ӧ ����˵���������
����˵���������
A.8.8gCO2�й��õ��ӶԵ���ĿΪ0.8NA
B.����CO24.48L����״���£�ʱת�Ƶ��ӵ���ĿΪ0.8NA
C.12g���ʯ��C�����������ۼ�����ĿΪ4NA
D.0.1molMgO���������ӵ�����������֮��Ϊ1.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ʻ���(COS)�㷺������ú��ʯ�ͺ���Ȼ��Ϊԭ�ϵĻ��������У���������ֱ���ŷŻ����������Ⱦ��ʯ�ͻ����в������ʻ����ͨ�����·����ѳ���
��.�ɷ��ѳ����ڴ��������£�COS��H2�ɷ�������ƽ�з�Ӧ��
i. COS(g)+H2(g)![]() H2S(g)+CO(g)��H1=-17kJ/mol
H2S(g)+CO(g)��H1=-17kJ/mol
ii. COS(g)+4H2(g)![]() H2S(g)+CH4(g)+H2O(g) ��H2
H2S(g)+CH4(g)+H2O(g) ��H2
(1)��֪��CH4(g)+H2O(g)![]() CO(g)+3H2(g)��H=+206kJ/mol�����H2=______________��
CO(g)+3H2(g)��H=+206kJ/mol�����H2=______________��
(2)T1��ʱ����10L�����ܱ������г���1molCOS��4molH2��������Ӧi��ii��5minʱ�ﵽƽ�⣬�����ϵѹǿ������20%��CO���������Ϊ10%����ƽ���ѹΪP1��
��0-5min�ڣ�v(COS)=______________��
�ڷ�Ӧi��ƽ�ⳣ��K=______________��
��������ʼ�¶�ΪT1���ľ����������ظ�����ʵ�飬H2��ƽ���ѹP2______________P1(����>����=������<��)������Ϊ______________��
��.ʪ���ѳ���ԭ��ΪCOS+4OH-=S2-+CO32-+2H2O���¶�Ϊ293Kʱ����COS�Թ̶���������ͨ��һ��Ũ�ȵ�NaOH��Һ�У������ϵ��c(S2-)��ʱ��(t)�ı仯��ͼ��ʾ��
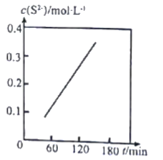
(3)��ͼ��֪������NaOH��Һ�ij�ʼŨ�ȣ�COS����������______________(��������������С������������)���ж�����Ϊ______________��
(4)��������Ӧ��ϵ��ͬʱ����������ˮ��Ҳ������COS���õ�������Һ��������Ӧ�Ļ�ѧ����ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ�����ĩ������Cu��Fe2O3��Cu2O�е�һ�ֻ��֣�Ϊ̽������ɣ���a g�ù����ĩ��Ʒ���ù�����ϡH2SO4��ַ�Ӧ��(��֪��Cu2O+2H+=Cu+Cu2++H2O)�����ջ�ʣ�¹����ҳ���������Ϊb g���������ƶ�����������( )
A.���ʣ��Ĺ���ֻ��Cu
B.��Ӧ����Һ�д������ڵ������������3��
C.b��ȡֵ��Χ��0��b��a
D.��b =![]() a�����ɫ�����ĩһ��Ϊ������
a�����ɫ�����ĩһ��Ϊ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com