
【题目】已知:25℃时H2C2O4的pKa1=1.22,pK a2=4.19,CH3COOH的pK a=4.76(电离常数K的负对数-1gK=pK)。下列说法正确的是
A. 浓度均为0.1mol·L-1NH4HC2O4和CH3COONH4溶液中:c(NH4+)前者小于后者
B. 0.1 mol·L-1KHC2 O 4溶液滴加氨水至中性:(NH4+)<c(C2O42-)
C. 0.1 mol·L-1K2C2O4溶液滴加盐酸至pH=1.22:C(H+)-c(OH-)=c(Cl-)-3c(HC2O4-)
D. 0.1 mol·L-1CH3COONa溶液中滴加KHC2O4溶液至PH=4.76;c(K+)>c(Na+)>c(HC2O4-)>c(C2O42-)>c(CH3COO-)
【答案】BC
【解析】A、由已知数据分析可得,HC2O4—的水解程度小于CH3COO—的,HC2O4—对NH4+水解的促进作用小于CH3COO—,故c(NH4+)前者大于后者,则A错误;B、向0.1 mol·L-1KHC2O 4溶液滴加氨水至中性,溶液中存在如下平衡:NH3·H2O![]() NH4++OH-,HC2O4-+H2O
NH4++OH-,HC2O4-+H2O![]() H2C2O4+OH-,HC2O4-
H2C2O4+OH-,HC2O4-![]() C2O42—+H+,因为c(OH-) =c(H+),所以c(NH4+) +c(H2C2O4) = c(C2O42—),则(NH4+)<c(C2O42-),所以B正确;C、0.1 mol·L-1K2C2O4溶液滴加盐酸至pH=1.22,则生成KCl和H2C2O4,且c(H+)=10-1.22 mol·L-1,已知H2C2O4
C2O42—+H+,因为c(OH-) =c(H+),所以c(NH4+) +c(H2C2O4) = c(C2O42—),则(NH4+)<c(C2O42-),所以B正确;C、0.1 mol·L-1K2C2O4溶液滴加盐酸至pH=1.22,则生成KCl和H2C2O4,且c(H+)=10-1.22 mol·L-1,已知H2C2O4![]() HC2O4-+H+,Ka1=1.22,所以c(H2C2O4) = c(HC2O4—),由质子守恒可得c(H+)+ c(HC2O4—)+ 2c(H2C2O4)= c(OH-)+ c(Cl-),所以C(H+)-c(OH-)=c(Cl-)-3c(HC2O4-),故C正确;D、溶液呈酸性即c(OH-) < c(H+),由电荷守恒可得,c(K+)+c(Na+) < c(HC2O4-)+ c(C2O42-) +c(CH3COO-),所以D错误。本题正确答案为BC。
HC2O4-+H+,Ka1=1.22,所以c(H2C2O4) = c(HC2O4—),由质子守恒可得c(H+)+ c(HC2O4—)+ 2c(H2C2O4)= c(OH-)+ c(Cl-),所以C(H+)-c(OH-)=c(Cl-)-3c(HC2O4-),故C正确;D、溶液呈酸性即c(OH-) < c(H+),由电荷守恒可得,c(K+)+c(Na+) < c(HC2O4-)+ c(C2O42-) +c(CH3COO-),所以D错误。本题正确答案为BC。


科目:高中化学 来源: 题型:
【题目】短周期元素T、Q、R.、W原子序数依次增大,其组成物质可进行下列转化:金属单质A与气体单质B加热反应生成M,M具有硬度高、耐高温等特点,易与常见液体D反应,生成刺激性气味气体E能使湿润的红色石蕊试纸变蓝 。A不溶于碱溶液但可与E在加热条件下反应得到M。下列说法正确的是
A. 化合物M是一种新型无机非金属材料氮化铝
B. Q元素组成的单质常温下较稳定
C. R元素组成的单质A又称作“国防金属”
D. A与E反应中,每生成0.1molM可得气态产物3.36L(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl和Na2CO3的固体混合物与一定质量的稀盐酸恰好完全反应,得到4.4gCO2和100g21.1%的NaCl溶液,求:原混合物中NaCl的质量分数?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质与指定物质的主要成分对应正确的是
A. 赤铁矿—Fe2O3 B. 漂白粉—NaClO
C. 纯碱—NaOH D. 大理石—Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4FeO42-+10H2O=4Fe(OH)3↓+8OH-+3O2↑ ,测得c(FeO42-)在不同条件下变化如图甲、乙、丙、丁所示:
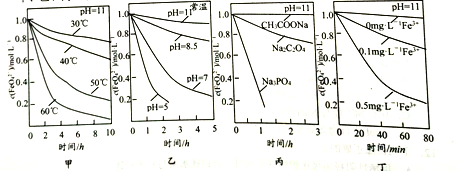
下列说法正确的是
A. 图甲表明,其他条件相同时,温度越低FeO42-转化速率越快
B. 图乙表明,其他条件相同时,碱性越强FeO42-转化速率越快
C. 图丙表明,其他条件相同时,钠盐都是FeO42-优良的稳定剂
D. 图丁表明,其他条件相同时,碱性条件下Fe3+能加快FeO42-的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列说法正确的是
A. 2.1g丙烯中所含的共用电子对总数为0.3NA
B. 4.6gNO2和N2O4的混合气体中含有的氮原子数为0.1NA
C. 过氧化氢分解制得标准状况下2.24LO2,转移电子数目为0.4NA
D. 在高温高压、催化剂的条件下,56gN2和12gH2充分反应,生成NH3的分子数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(变式探究)已知有以下物质相互转化。
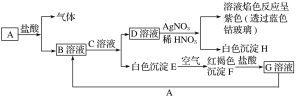
试回答下列问题:
(1)B的化学式为__________,D的化学式为________。
(2)由E转变成F的化学方程式为___________________________。
(3)用KSCN鉴别G溶液的离子方程式为_______________________;
向G溶液加入A的有关反应离子方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求计算
(1)0.5mol H2SO4 的质量是 g,其中含有 mol S, 个O.
(2)同温同压下,等体积的CO和CO2的物质的量之比 ,质量比 ,所含氧元素的质量比 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com