
【题目】(变式探究)已知有以下物质相互转化。
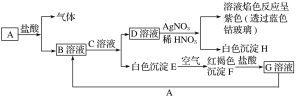
试回答下列问题:
(1)B的化学式为__________,D的化学式为________。
(2)由E转变成F的化学方程式为___________________________。
(3)用KSCN鉴别G溶液的离子方程式为_______________________;
向G溶液加入A的有关反应离子方程式为_______________________________。
【答案】FeCl2KCl4Fe(OH)2+O2+2H2O===4Fe(OH)3Fe3++3SCN-===Fe(SCN)32Fe3++Fe===3Fe2+
【解析】
分析流程图可知白色沉淀E在空气中变化为红褐色沉淀F,说明E为Fe(OH)2,F为Fe(OH)3,F+HCl=G,推断G为FeCl3,B+C=Fe(OH)2+D溶液,D溶液和硝酸酸化的硝酸银反应生成白色沉淀H为AgCl,溶液焰色反应隔着钴玻璃为紫色,证明溶液中含有钾元素,D为KCl,证明C溶液为KOH,B溶液为FeCl2,G+A=B判断A为Fe,依据分析判断出的物质分析选项回答问题。
(1)根据以上分析可知B是氯化亚铁,化学式是FeCl2,D为氯化钾,化学式为KCl;
(2)E转变成F的反应是氢氧化亚铁被氧气氧化为氢氧化铁的反应,方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)G溶液为FeCl3,用KSCN鉴别的离子方程式是铁离子和硫氰酸根离子反应生成血红色溶液,反应的离子方程式为Fe3++3SCN-=Fe(SCN)3;向G溶液FeCl3加入Fe的有关离子反应方程式为2Fe3++Fe=3Fe2+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是__________
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2 H2O,当1mol O2发生反应时,还原剂所失电子的物质的量为___mol。向CuSO4溶液中加入镁条时有气体生成,该气体是____。
(3)右图为电解精炼银的示意图,_____(填a或b)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为____________。
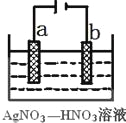
(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于钠的叙述中,正确的是( )
A.钠是银白色金属,熔点低,硬度大
B.钠放置于空气中,会迅速被氧化而生成淡黄色的氧化钠
C.在氧气中加热时,金属钠剧烈燃烧,火焰呈黄色
D.金属钠着火可以用水灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25℃时H2C2O4的pKa1=1.22,pK a2=4.19,CH3COOH的pK a=4.76(电离常数K的负对数-1gK=pK)。下列说法正确的是
A. 浓度均为0.1mol·L-1NH4HC2O4和CH3COONH4溶液中:c(NH4+)前者小于后者
B. 0.1 mol·L-1KHC2 O 4溶液滴加氨水至中性:(NH4+)<c(C2O42-)
C. 0.1 mol·L-1K2C2O4溶液滴加盐酸至pH=1.22:C(H+)-c(OH-)=c(Cl-)-3c(HC2O4-)
D. 0.1 mol·L-1CH3COONa溶液中滴加KHC2O4溶液至PH=4.76;c(K+)>c(Na+)>c(HC2O4-)>c(C2O42-)>c(CH3COO-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:I2+2 S2O32-![]() S4O62-+2I-。相关物质的溶度积常数见下表:
S4O62-+2I-。相关物质的溶度积常数见下表:
物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl22H2O晶体,加入________;调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=_____________;过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl22H2O晶体。
(2)在空气中直接加热CuCl22H2O晶体得不到纯的无水CuCl2,原因是________________。(用化学方程式表示)。由CuCl22H2O晶体得到纯的无水CuCl2的合理方法是_______________。
(3)某学习小组用“间接碘量法”测定含有CuCl22H2O晶体的试样(不含能与I-发生反应的氧化性质杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.1000 mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知:CuCl2溶液与KI反应的离子方程式为Cu2+ + 4I- = 2CuI↓ + I2
①可选用___________作滴定指示剂,滴定终点的现象是_________________。
②该试样中CuCl22H2O的质量百分数为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】规律提炼题组
完成下列与溶液pH有关的计算,并提炼解题规律。
(1)室温下pH=4的NH4Cl溶液和HCl溶液中由水电离出的c(H+)之比为_______
(2)在25℃时,pH等于9和pH等于11的两种氢氧化钠溶液等体积混合后,溶液中的氢离子浓度为 _____
(3)某温度时,水的KW=10-13,将此温度下pH=12的NaOH溶液aL与pH=2的H2SO4溶液bL混合:,
①若所得混合溶液为中性,则a:b= ____
②若所得混合溶液pH=3,则a:b=_____
(4)已知某温度时0.1 molL-1NaOH pH等于11,在此温度下,若将100体积pH1=a的H2SO4溶液与1体积pH2=b的NaOH溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是________________(用含a、b的表达式表示)
(5)(学法题)总结归纳求混合溶液pH时,应注意的问题:__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图I的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法不正确的是
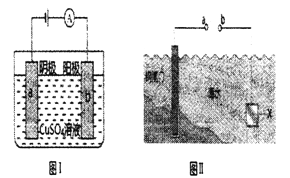
A. 图I中SO42-向b极移动
B. 图I中a为纯铜
C. 图Ⅱ中如果a、b间连接电源,则a连接负极
D. 图Ⅱ中如果a、b间用导线连接,则X可以是铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示下列描述正确的是

A. 反应开始到10s,用Z表示的反应速率为0.158 mol/(Ls)
B. 反应开始到10s,X的物质的量浓度减少了0.79 mol/L
C. 反应开始到10s,Y的转化率为79.0 %
D. 反应的化学方程式为:X+Y![]() Z
Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是

A. Y的原子半径比X的大
B. Q的最高价氧化物的水化物的酸性比Z的强
C. Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
D. X、Y和氢3种元素形成的化合物中都只有共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com