
【题目】海冰是海水冻结而成的咸水冰,海水冻结时,部分来不及流走的盐分(设以NaCl为主)以卤汁的形式被包围在冰晶之间,形成“盐泡”,其大致结钩如图所示,若海冰的冰龄达到1年以上,融化后的水为淡水。下列说法错误的是
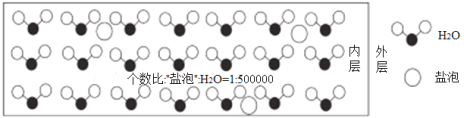
A.海冰的坚固程度不如淡水冰
B.海冰内层“盐泡”越多,密度越小
C.海冰内层NaCl的浓度约为10-4 mol·L1 (设冰的密度为0.9g·cm3)
D.海冰冰龄越长,内层的“盐泡”越少
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能,此时硫酸铅电极处生成Pb。下列有关说法正确的是
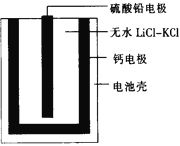
A. 输出电能时,外电路中的电子由硫酸铅电极流向钙电极
B. 放电时电解质LiCl-KCl中的Li+向钙电极区迁移
C. 电池总反应为Ca+PbSO4+2LiCl![]() Pb+Li2SO4+CaCl2
Pb+Li2SO4+CaCl2
D. 每转移0.2 mol电子,理论上消耗42.5 g LiCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车的启动电源常用铅蓄电池,电池反应如下: PbO2 + Pb + 2H2SO4 ![]() 2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
2PbSO4+ 2H2O,根据此反应判断下列叙述中正确的是( )
A. PbO2放电时是电池的负极,充电时是电池的阳极
B. 负极的电极反应式为:Pb + SO42—– 2e–=PbSO4
C. 放电时,PbO2得电子,被氧化
D. 电池放电时,溶液酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯胺![]() 是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
是重要的化工原料。某兴趣小组在实验室里进行苯胺的相关实验。
已知:①![]() 和NH3相似,与盐酸反应生成易溶于水的盐
和NH3相似,与盐酸反应生成易溶于水的盐![]()
②用硝基苯制取苯胺的反应原理: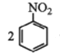 +3Sn+12HCl
+3Sn+12HCl![]()
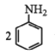 +3SnCl4+4H2O
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
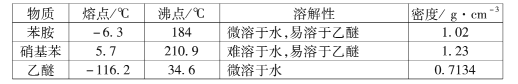
I.比较苯胺与氨气的性质
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为____;用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是____。
Ⅱ.制备苯胺
往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50% NaOH溶液,至溶液呈碱性。

(2)冷凝管的进水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为____。
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示装置。加热装置A产生水蒸气,烧瓶C中收集到苯胺与水的混合物;分离混合物得到粗苯胺和水溶液。

ii.往所得水溶液中加入氯化钠固体,使溶液达到饱和状态,再用乙醚萃取,得到乙醚萃取液。
iii.合并粗苯胺和乙醚萃取液,用NaOH固体干燥,蒸馏后得到苯胺2.79g。
(4)装置B无需用到温度计,理由是____。
(5)操作i中,为了分离混合物,取出烧瓶C前,应先打开止水夹d,再停止加热,理由是____。
(6)该实验中苯胺的产率为____。
(7)欲在不加热条件下除去苯胺中的少量硝基苯杂质,简述实验方案:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值,下列说法正确的是
A.0.1molKHSO4晶体中含有H+数为0.1NA
B.标准状况下,5.6LSO3分子中含有的电子总数为10NA
C.在50g质量分数为46%的乙醇水溶液中,含氢原子总数为3NA
D.33.6gFe与足量的水蒸气加热充分反应,转移电子数为1.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,X的原子半径是所有短周期主族元素中最大的,W的核外电子数与X、Z的最外层电子数之和相等,Y的原子序数是Z的最外层电子数的2倍,由W、X、Y三种元素形成的化合物M的结构如图所示。下列说法错误的是
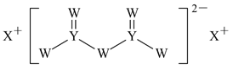
A.气态氢化物的稳定性:Z>Y
B.W和Y形成的晶体为共价晶体
C.Y单质的熔点低于X单质
D.化合物M中W、Y都满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍钴锰三元材料是近年来开发的一类新型锂离子电池正极材料,该材料中Ni为主要活泼元素,通常可以简写为LiAO2。充电时总反应为LiAO2+nC=Li1-xAO2+LixCn(0<x<1),工作原理如图所示,下列说法正确的是
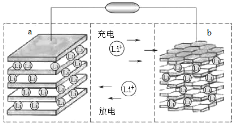
A.放电时Ni元素最先失去电子
B.放电时电子从a电极由导线移向b电极
C.充电时的阳极反应式为LiAO2 xe-= Li1-xAO2 + xLi+
D.充电时转移1mol电子,理论上阴极材料质量增加7g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的贵重金属,其化合物在催化剂研究和光电材料等方面应用广泛。回答下列问题:
(1)在铜的配合物中,H2O、NH3、CO等常用作配体。
①基态Cu2+的价电子轨道表示式为_________。
②H、C、N、O元素中,元素的第一电离能最高的为_____,元素电负性由大到小的顺序为________。
③水溶液中有H3O+、H5O2+、H9O4+等微粒的形式。H3O+中O的杂化轨道类型为_____,其H-O-H键角_______(填“>”或“<”)H2O中H-O-H的键角。H5O2+内部存在氢键,H5O2+的结构式可表示为__________。
④Cu2Cl2·2CO·2H2O是一种配合物,其结构如图所示:![]() ,其中每个Cu原子能与其他原子形成_________个配位键。
,其中每个Cu原子能与其他原子形成_________个配位键。
(2)CuCl结构属于立方晶系,其晶胞如图所示:

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。则A原子分数坐标为_________。
②晶胞中距离每个Cu+最近的Cl-的个数为_______,若晶胞的棱长为a pm,晶体的密度为ρ g·cm-3,计算阿伏加德罗常数NA=________(列式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用示意图或图示的方法能够直观形象地将化学知识传授给学生,下列示意图或图示正确的是( )
A.砷原子的结构示意图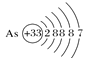 B.BF4—的结构式
B.BF4—的结构式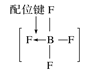
C.HF分子间的氢键 D.丙氨酸的手性异构
D.丙氨酸的手性异构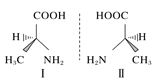
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com