
����Ŀ�������ҹ�����ӵ�����ʽϿ��������ƣ�����β���ѳ�Ϊ��Ҫ�Ŀ�����Ⱦ��ش��������⣺

��1����������������ʱ������Ӧ��N2(g)+O2(g) ![]() 2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��һ����NO�����ֽ�Ĺ����У�NO��ת������ʱ��仯�Ĺ�ϵ����ͼ��ʾ��
2NO(g)���ǵ�������β���к���NO��ԭ��֮һ��һ����NO�����ֽ�Ĺ����У�NO��ת������ʱ��仯�Ĺ�ϵ����ͼ��ʾ��
�ٷ�Ӧ2NO(g) ![]() N2(g)+O2(g)Ϊ________��Ӧ(����ȡ����ȡ�)��
N2(g)+O2(g)Ϊ________��Ӧ(����ȡ����ȡ�)��
��һ���¶��£��ܹ�˵����Ӧ2NO(g) ![]() N2(g)+O2(g)�Ѵﵽƽ�����______(�����)��
N2(g)+O2(g)�Ѵﵽƽ�����______(�����)��
a�������ڵ�ѹǿ�������仯 b�����������ܶȲ������仯
c��NO��N2��O2��Ũ�ȱ��ֲ��� d����λʱ���ڷֽ�4 mol NO��ͬʱ����2 mol N2
��2��������������ϡ��ȼ��ʱ��β���е���Ҫ��Ⱦ��ΪNOx������CH4����ԭNOx����������������Ⱦ��
��֪��CH4(g)+4NO2(g)=== 4NO(g)+CO2(g)+2H2O(g) ��H=��574 kJ��mol-1
CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ��H=��867 kJ��mo1-1
д��CH4��NO��Ӧ����N2��CO2��H2O(g)���Ȼ�ѧ����ʽ��______________________��
��3��������Ⱦ�ﵪ����������û���̿��ԭ��������ij�о�С����ij0.5L���ܱ������м���һ�����Ļ���̿��NO��������ӦC(s)��2NO(g)![]() N2(g)��CO2 (g)����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ������£�
N2(g)��CO2 (g)����T1��ʱ����Ӧ���е���ͬʱ���ø����ʵ����ʵ������£�
ʱ�䣨min�� ���ʵ�����mol�� | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.32 | 0.32 |
N2 | 0 | 0.21 | 0.30 | 0.30/span> | 0.34 | 0.34 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.17 | 0.17 |
��0~10min�ڣ�NO��ƽ����Ӧ����v(NO)��________________��T1��ʱ���÷�Ӧ��ƽ�ⳣ��K��___________________________��
��30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������__________������ĸ��ţ���
a������һ�����Ļ���̿ b��ͨ��һ������NO
c���ʵ���С��������� d��������ʵĴ���
f���Ƴ�һ������CO2
����30min�������¶���T2�����ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ5:3:3���� H_________0��������������������������
���𰸡� ���� c CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=-1160kJ/mol 0.084mol��L��1��min��1 ![]() ����0.56�� f ��
����0.56�� f ��
����������1���ٸ��ݡ��ȹ���ƽ����֪��T2����T1���¶�Խ�ߣ�NO��ת����ԽС���������¶�ƽ�����淴Ӧ�����ƶ������淴ӦΪ���ȣ�����ӦΪ���ȷ�Ӧ����a���÷�Ӧ�Ƿ�Ӧ�����������ķ�Ӧ���������۷�Ӧ�Ƿ�ﵽƽ��״̬����ϵ��ѹǿʼ�ղ��䣬��a����b�������������������䣬����������䣬�ܶ�ʼ�ձ��ֲ��䣬�ܶȲ��䲻����Ϊƽ��״̬�ı�־����b����c.NO��N2��O2��Ũ�ȱ��ֲ��䣬�ﵽƽ��״̬����c��ȷ��d.��λʱ���ڷֽ�4molNO��ͬʱ����2molN2�������淴Ӧ���ʣ�����˵����Ӧ�ﵽƽ��״����d����ѡc����2����֪����CH4(g)+4NO2(g)=== 4NO(g)+CO2(g)+2H2O(g) ��H1=��574 kJ��mol-1
��CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(g) ��H2=��867 kJ��mo1-1
���ݸ�˹���ɣ��ɢ�![]() -�ٵ÷�ӦCH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=��867 kJ��mo1-1
-�ٵ÷�ӦCH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H=��867 kJ��mo1-1![]() -����574 kJ��mol-1��=-1160kJ/mol����3���ٷ���ͼ�����ݣ�0��10min�ڣ�NO��ƽ����Ӧ����v��NO��=
-����574 kJ��mol-1��=-1160kJ/mol����3���ٷ���ͼ�����ݣ�0��10min�ڣ�NO��ƽ����Ӧ����v��NO��=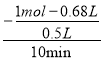 =0.084mol��L��1��min��1��20minʱ��ӦC(s)��2NO(g)
=0.084mol��L��1��min��1��20minʱ��ӦC(s)��2NO(g)![]() N2(g)��CO2 (g)��ƽ�⣬NO��N2��CO2�����ʵ���Ũ�ȷֱ�Ϊ0.80mol/L��0.60mol/L��0.60mol/L,��ѧƽ�ⳣ������ʽΪK=
N2(g)��CO2 (g)��ƽ�⣬NO��N2��CO2�����ʵ���Ũ�ȷֱ�Ϊ0.80mol/L��0.60mol/L��0.60mol/L,��ѧƽ�ⳣ������ʽΪK=![]() ����30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬ͼ�����ݷ�����֪����Ũ������һ��������������̼Ũ�ȶ���С��a������һ�����Ļ���̿�ǹ��壬��ƽ����Ӱ�죬�����ϣ�b��ͨ��һ������NO����Ӧ������У��ﵽƽ���һ��������������������̼Ũ���������ϣ�c���ʵ���С�������������Ӧǰ���������������ķ�Ӧ��ƽ�ⲻ������������Ũ�ȶ��������ϣ�d��������ʵĴ�����ֻ�ܸı仯ѧ��Ӧ���ʣ����ܸı�ƽ�⣬Ũ�Ȳ��䣬�����ϣ�f���Ƴ�һ������CO2��ƽ�������ƶ���������Ũ������һ��������������̼��Ũ�ȼ�С�����ϡ���ѡf������
����30min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬ͼ�����ݷ�����֪����Ũ������һ��������������̼Ũ�ȶ���С��a������һ�����Ļ���̿�ǹ��壬��ƽ����Ӱ�죬�����ϣ�b��ͨ��һ������NO����Ӧ������У��ﵽƽ���һ��������������������̼Ũ���������ϣ�c���ʵ���С�������������Ӧǰ���������������ķ�Ӧ��ƽ�ⲻ������������Ũ�ȶ��������ϣ�d��������ʵĴ�����ֻ�ܸı仯ѧ��Ӧ���ʣ����ܸı�ƽ�⣬Ũ�Ȳ��䣬�����ϣ�f���Ƴ�һ������CO2��ƽ�������ƶ���������Ũ������һ��������������̼��Ũ�ȼ�С�����ϡ���ѡf������
30min�ﵽƽ��ʱ������NO��N2��CO2��Ũ��֮��4��3��3�������¶���T2�棬�ﵽƽ��ʱ��������NO��N2��CO2��Ũ��֮��Ϊ5��3��3��˵��ƽ��������У����������ȷ�Ӧ������Ӧ�����Ƿ��ȷ�ӦH��0��


 �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д� ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС��ѧ�������Ϸ��з������ˮ��Һ���е�����������ͬʱ�õ��Ա������ᡣԭ����ͼ��ʾ��H2A��ʾ�Ա������ᣬA2-��ʾ�Ա�����������ӣ�������˵����ȷ���ǣ� ��

A. �缫aΪ�������缫b��������
B. ͨ��һ��ʱ���������ҺpH����
C. A2-ͨ�������ӽ���Ĥ����Ũ����
D. ��200ml��8.3g/L�Ա���������Һ��ͨ��һ��ʱ���Ũ��������0.1mol/L�����������������4.48L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Ԫ���� H2Y ��Һ�еμ� KOH ��Һ�����û����Һ�� pH ������Ũ�ȱ仯�Ĺ�ϵ����ͼ��ʾ�������й�˵����������

A. ���� M ��ʾ pH�� lg![]() �ı仯��ϵ
�ı仯��ϵ
B. a����Һ�У�c(H+) �D c(OH-)��2c(Y2��)��c(HY-) �D c(K+)
C. H2Y �ĵڶ������볣��Ka2(H2Y)��10��4.3
D. ����b����Һ�У�c(H2Y)��c(Y2-)��c(HY-)��c(H+)��c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
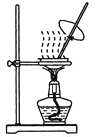
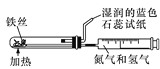
����Ŀ��������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���

�� �� �� ��
A. ��װ�ü����к��ȵIJⶨ
B. ��װ������ȡCO2����
C. ��װ�ñ�����CH3COONa��Һ��CH3COONa����
D. ��װ�ö�ģ�ҵ�ư������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���X��ij��ҩ�����Ҫ�ɷ֣���ҵ�Ϻϳɸû������һ��·������(���ַ�Ӧ���Ӧ������ȥ)��

��֪�����뺬�ǻ��Ļ�����ɷ���������������Ӧ��RCOO R�䣫R��OH![]() RCOOR�士R��OH(R��R�䡢R�����������)��
RCOOR�士R��OH(R��R�䡢R�����������)��
��1����Ӧ��������Լ���_______����Ӧ�ڵķ�Ӧ������_________��
��2��B�к��������ŵ�������________����Ӧ�ܵIJ������X���⣬��һ�ֲ����������________��
��3��D��һ���������ܷ������۷�Ӧ���ɸ߷��ӻ�����ø߷��ӻ�����Ľṹ��ʽΪ____________��
��4����Ӧ�۵Ļ�ѧ����ʽΪ_______________________��
��5��E��ͬ���칹���ж��֣�д�����������������л���ṹ��ʽ________��
��.������һ�ȴ���ֻ��һ��
��.���Ȼ�����Һ������ɫ��Ӧ
��.����̼��������Һ��Ӧ�ų�CO2
��6����֪����![]()
![]()
![]() ���ڵ�����������һ������CH3����Cl��ʱ���������ȡ����һ����������λ���λ��������������һ������NO2����COOH��ʱ���������ȡ����һ�������ļ�λ����д���Լױ����Ҵ�Ϊԭ���Ʊ�
���ڵ�����������һ������CH3����Cl��ʱ���������ȡ����һ����������λ���λ��������������һ������NO2����COOH��ʱ���������ȡ����һ�������ļ�λ����д���Լױ����Ҵ�Ϊԭ���Ʊ� �ĺϳ�·��ͼ(���Լ�����)____________��
�ĺϳ�·��ͼ(���Լ�����)____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��̼�����׳ƴ������Ϊ��ʹ�õ�ԭ����__________________�������ӷ���ʽ��ʾ����
��2��25��ʱ��pH��Ϊ11�� NaOH ��Һ��Na2CO3��Һ����ˮ�����OH-Ũ��֮����_____
��3����0.1 mol��L��1��Na2CO3��Һ�У���������Ũ�ȹ�ϵʽ��ȷ����________��
A��[CO32��]��[HCO3��]��0.1 mol��L��1
B��[CO32��]��[HCO3��]��[H2CO3]��0.1 mol��L��1
C��[OH��]��[H��]��[HCO3��]
D��[Na��]��[OH��]��[H��]��[HCO3��]
��4��������0.1 mol��L��1��Na2CO3��Һ�У�����Ũ���ɴ�С��˳����__________________________________��
��5������BaSO4�������Һ�еμ�Na2CO3��Һ������BaCO3��������ʱ��Һ��![]() =__________������֪Ksp(BaCO3)=2.6��109��Ksp(BaSO4)=1.1��1010���������һλС����
=__________������֪Ksp(BaCO3)=2.6��109��Ksp(BaSO4)=1.1��1010���������һλС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ��������������ȷ���ǣ� ��
A. 1 mol NH3�����е�ԭ����ΪNA
B. ��100 mL 0.1 mol��L-1��FeCl3��Һ�����ˮ�п��Ƶ�Fe(OH)3��������ĿΪ0.01NA
C. ���³�ѹ�£�48gO2��O3�Ļ������������ԭ����Ϊ3NA
D. 1L 0.1 mol��L-1 NaCl��Һ��������Na+ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ����400mL0.2mol/L����������Һ��ʵ�鲽�����£�
A������ƽ�ϳƳ�_______g�����ƹ��壬���������ձ��������������ˮ�ܽ⡣
B���ѵõ�����Һ��ȴ��С�ĵ�����__________ע��_______________ �С�
C������������ˮϴ���ձ��Ͳ�����2��3�Σ�ÿ��ϴ��ҺҲС��ת������ƿ�С�
D������������ƿ�м�����ˮ��Һ���̶�l~2cm��������________С�ĵμ�����ˮ����Һ��Һ��ײ���̶���ˮƽ���С�
E����ƿ�����������ҡ�ȡ�
F������õ���Һ�����Լ�ƿ�У����ϱ�ǩ����ϴ������ƿ��
(1) ����д�����հ״���
(2) ���������ʹ������ҺŨ��ƫ�͵���___________(�����)��

a��ijͬѧ����ʱ�۲�Һ��������ͼ��ʾ
b��û�н��������IJ�������C
c��ҡ�Ⱥ���Һ����ڿ̶���
d��B����ʱ������Һ����������
e������ƿ��ǰ�ڱ�մ��ˮ��
(3) ���ʵ������18mol/L��Ũ��������3. 6mol��L-1��ϡ����250mL����������Ũ��������Ϊ___________mL����ʵ��ʱӦ��_________��ȡŨ���ᡣ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ǻ�ѧ�о��Ļ��������й��ڸ�ʵ��װ�õ�������ȷ������ ��

A. װ�âٳ����ڷ��뻥�����ܵ�Һ������
B. װ�âڿ���������NH3��HCl���壬����ֹ����
C. װ�âܿ����ڸ���ռ��Ȼ��⣬�����ն�����Ȼ���
D. װ�âۿ������ռ�H2��CO2��Cl2��NH3������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com