
【题目】.某盐是一种重要的化工原料,在印染、制革、木材和农业等领域有重要用途,其溶液可能含有NH4+、Al3+、SO42-、Fe2+、Cl-等若干种离子,某同学设计并完成了如下实验:
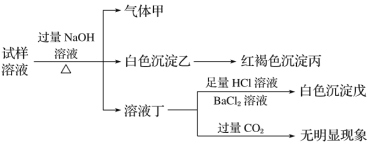
根据以上的实验操作与现象,该同学得出的结论不正确的是( )
A.试样中肯定有NH4+、SO42-和Fe2+
B.试样中一定没有Al3+
C.若气体甲在标准状况下体积为0.448 L,沉淀丙和沉淀戊分别为1.07 g和4.66 g,则可判断溶液中还有Cl-
D.该盐工业上可以用作净水剂
【答案】C
【解析】
加入过量氢氧化钠有气体放出,说明为氨气,则溶液中含有铵根离子,生成白色沉淀,又变为红褐色,说明含有亚铁离子,溶液丁加足量盐酸和氯化钡溶液,有白色沉淀,说明含有钡离子,加二氧化碳气体无现象,说明没有铝离子。
A现象,根据上面分析得出试样中肯定有NH4+、SO42-和Fe2+,故A正确,不符合题意;
B现象,根据上面分析得出试样中一定没有Al3+,故B正确,不符合题意;
C选项,若气体甲在标准状况下体积为0.448L,即物质的量为0.02mol,沉淀丙和沉淀戊分别为1.07g和4.66g,氢氧化铁物质的量为0.01mol,即亚铁离子物质的量为0.01mol,硫酸钡的物质的量为0.02mol级硫酸根物质的量为0.02mol,根据电荷守恒,刚好呈电中性,因此溶液中没有Cl-,故C错误,符合题意;
D选项,该盐含有亚铁离子,氧化水解生成氢氧化铁胶体,可以用作净水剂,故D正确,不符合题意;
综上所述,答案为C。


科目:高中化学 来源: 题型:
【题目】某强酸性溶液X,含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、NO3-中的一种或几种离子,取溶液进行连续实验,能实现如下转化:

依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是:________________;不能肯定的是:_______________。对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中,根据现象就可判断,则该试剂是:_________。(选填:①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸,⑤KSCN溶液,⑥KMnO4溶液)
(2)气体F的电子式为:_______________,实验中,可以观察到反应②的现象是:__________________。
(3)写出步骤①所有发生反应的离子方程式________________________、___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、X、Y 和 Z 是原子序数依次递增的短周期元素。其中A与Y同主族,X与Z同主族,A与B和X均可形成10个电子的化合物;B与Z 的最外层电子数之比为 2∶3,常见化合物Y2X2与水反应生成X的单质,其水溶液可使酚酞试液变红。请回答下列问题:
(1)Z 元素在元素周期表中的位置是______________ ,化合物 B2A4 的电子式为______________
(2)化合物A2X和A2Z中,沸点较高的是__________(填化学式),其主要原因是_____________
(3)A与X、A与Z均能形成18个电子的化合物,此两种化合物发生反应的化学方程式为:_______
(4)将Z与X 形成的气态化合物ZX2通入Ba(NO3)2 溶液中,有白色沉淀和NO气体生成,发生反应的离子方程式为___________________, 由此可得出一氧化氮与ZX2的还原性大小关系为________________
(5)将Y2X2投入到Y2Z的水溶液中可生成Z的单质,发生反应的离子方程式为:______________,并用单线桥标出此反应中电子转移的方向和数目。
(6)两种均含A、X、Y、Z四种元素的化合物相互反应放出气体的反应离子方程式为:_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分。

(1)②、⑥、⑧的离子半径由大到小的顺序为____________(用离子符号表示)。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_____ (用化学式表示)。
(3)As的原子结构示意图为_________其氢化物的化学式为__________;
(4)Y由②、⑥、⑧三种元索组成,它的水溶液是生活中常见的消毒剂。As 可与Y的水溶液反应,产物有As的最高价含氧酸,该反应的化学方程式为__________,当消耗l mol还原剂时,电子转移了_____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷与氯气发生取代反应的副产品生产盐酸的设想在工业上已成为现实。某化学兴趣小组模拟上述过程,所设计的装置如图所示:
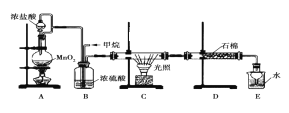
(1)A中制取Cl2的反应的化学方程式是_________________________。
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③_______________________。
(3)D装置中的石棉上吸附着潮湿的KI,其作用是________________。
(4)E装置的作用是_______________________。
(5)E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是______________。
(6)将1 mol CH4与Cl2发生取代反应,测得4种有机取代产物的物质的量相等,则消耗的氯气的物质的量是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X(g)+3Y (g)![]() 2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与2mol Y (g),下列说法正确的是( )
2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与2mol Y (g),下列说法正确的是( )
A.充分反应后,X的转化率和Y的转化率不相等,前者大于后者
B.当反应达到平衡状态时,W与M的物质的量浓度之比一定为2:1
C.当混合气体的密度不再改变,表明该反应已达平衡
D.若增大Y的浓度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.22.4LCl2溶于足量水,所得溶液中Cl2、Cl-、HClO和ClO-四种微粒总数为NA
B.标准状况下,38g3H2O2中含有3NA共价键
C.常温下,将5.6g铁块投入足量浓硝酸中,转移0.3NA电子
D.标准状况下,5.6L 一氧化氮和5.6L 氧气混合后的分子总数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是化学课外活动小组设计的用化学电源使LED灯发光的装置示意图。下列有关该装置的说法正确的是( )

A. 铜片为负极,其附近的溶液变蓝,溶液中有Cu2+产生
B. 如果将锌片换成铁片,电路中的电流方向将改变
C. 其能量转化的形式主要是“化学能→电能→光能”
D. 如果将稀硫酸换成柠檬汁,LED灯将不会发光
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿司匹林(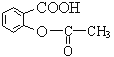 )能解热镇痛。
)能解热镇痛。
(1)阿司匹林属于__________(填“无机化合物”或“有机化合物”)。
(2)阿司匹林中含氧官能团有酯基和__________(填名称)。
(3)向阿司匹林的水溶液中滴入2~3滴紫色石蕊溶液,溶液颜色变红,说明阿司匹林溶液具有________性。
(4)根据阿司匹林的结构推断它能够发生的化学反应类型为________(填序号)。
①中和反应 ②加成反应 ③取代反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com