
����Ŀ��������ҵ�ǹ��ҹ�ҵ�Ļ�������ش������ʴ����������е��й����⣮
��1�������п��������������⣮�ֽ�һ�������Ƭ���������У������ⱻ��������Һ�з����Ļ��Ϸ�Ӧ�Ļ�ѧ����ʽ ��
��2����ͼ�ĸ�װ�ÿɷ�ֹ��������ʴ�����ţ��� 
��3����ʵ�������У����������ı����ͭ��ֹ������ʴ��װ��ʾ��ͼ��ͼ�� 
��A�缫��Ӧ�Ľ�������дԪ�����ƣ���B�缫�ĵ缫��Ӧʽ�� ��
�������ǰA��B������Ƭ������ͬ�������ɺ�����ȡ��ϴ������ɡ�����������������Ϊ5.12g������ʱ��·��ͨ���ĵ���Ϊmol��
�۶Ʋ������ͭ���ȶ�п�������ױ���ʴ�����Ҫ˵��ԭ���ǣ� ��
���𰸡�
��1��2FeCl3+Fe=3FeCl2
��2��BD
��3��ͭ��Cu2++2e��=Cu��0.08������ͭ���ã��Ʋ��ƻ����ڳ�ʪ�������γ�ԭ��أ���Ϊ�������������ĸ�ʴ
���������⣺��1�����������Ժ�����֮�䷴Ӧ�����Ȼ�����ˮ��������������������Ժ��Ȼ���֮�䷴Ӧ�õ��Ȼ���������2FeCl3+Fe=3FeCl2 ��
���Դ��ǣ�2FeCl3+Fe=3FeCl2����2��Bװ���У���������ԭ��ص����������������������⣬Dװ���У���������������������������Cװ�þ߱����������������Aװ���У���������ԭ��صĸ������ױ���ʴ��
���Դ��ǣ�BD����3�����������ı����ͭ������ͭ�������������ϣ������缫����ʧ���ӵ�������Ӧ���ҽ�����Ϊ�����������缫��Ӧ��Cu2++2e��=Cu��
���Դ��ǣ�ͭ��Cu2++2e��=Cu��
��������ͭ�������٣�������ͭ�������ӣ�����������Ϊ5.12gʱ������������ͭ������Ϊ2.56g������ͭ��ת�Ƶ���֮��Ĺ�ϵʽ֪��ת�Ƶ��ӵ����ʵ���= ![]() =0.08mol�����Դ��ǣ�0.08��
=0.08mol�����Դ��ǣ�0.08��
�۶�ͭ������������ͭ���ã��Ʋ��ƻ����ڳ�ʪ�������γ�ԭ��أ���Ϊ�������������ĸ�ʴ�����Ƕ�п�����Ʋ��������ZnΪ������������Ϊ�������������������������Դ��ǣ�����ͭ���ã��Ʋ��ƻ����ڳ�ʪ�������γ�ԭ��أ���Ϊ�������������ĸ�ʴ��
�����㾫�������ý����ĵ绯ѧ��ʴ���������Ŀ�����жϼ��ɵõ��𰸣���Ҫ��֪�����ı�����Ϳ�����㣻���ָ���ı�������ڲ��ṹ��ʹ���ȶ���������������������������һ�ָ�Ϊ���õĽ�����Ҫ�����Ľ�������ԭ��أ���ӵ�Դ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������Ӧ��ʱ����ԭ���õ��ǣ� ��
A.��������ˮ��
B.������������ʪ��
C.Ư�۾���������
D.������ʳƷ���ڵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2013��3���ҹ���ѧ�ұ�������ͼ��ʾ��ˮ��Һ����ӵ����ϵ����������������ǣ� �� 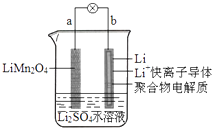
A.aΪ��ص�����
B.��طŵ練ӦΪLiMn2O4=Li1��xMn2O4+xLi
C.�ŵ�ʱ��a��﮵Ļ��ϼ۲������仯
D.�ŵ�ʱ����Һ�е�Li+��b��aǨ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ӧ����1molˮ�����ų�241.8kJ��������1gˮ����ת��ΪҺ̬ˮ�ų�2.45kJ���������������Ȼ�ѧ����ʽ��д��ȷ���ǣ� ��
A.H2��g��+ ![]() O2��g��=H2O��l������H=��285.9 kJ/mol
O2��g��=H2O��l������H=��285.9 kJ/mol
B.H2��g��+ ![]() O2��g��=H2O��l������H=��241.8 kJ/mol
O2��g��=H2O��l������H=��241.8 kJ/mol
C.H2��g��+ ![]() O2��g��=H2O��l������H=+285.9 kJ/mol
O2��g��=H2O��l������H=+285.9 kJ/mol
D.H2��g��+ ![]() O2��g��=H2O��l������H=+241.8 kJ/mol
O2��g��=H2O��l������H=+241.8 kJ/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ������AlCl3 ��Һ����μ���NaOH��Һ�����ɳ���Al��OH��3������NaOH�������ı仯��ϵ��ͼ��ʾ���������������ڶ�Ӧ����Һ��һ���ܴ���������ǣ� �� 
A.a���Ӧ����Һ�У�K+��NH4+��I����CO32��
B.b���Ӧ����Һ�У�Na+��H+��S2����Cl��
C.c���Ӧ����Һ�У�NH4+��H+��NO3����SO42��
D.d���Ӧ����Һ�У�Na+��K+��SO42����HCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾװ����ȡ������������(�ƾ��Ƶ���ͼ�о�����ȥ)������գ�

(1)�Թ�a����Ҫ����Ũ���ᡢ��������Ҵ���2 mL����ȷ�ļ���˳������_________________��
(2)Ϊ��ֹa�е�Һ����ʵ��ʱ�������У��ڼ���ǰӦ��ȡ�Ĵ�ʩ��____________________��
(3)ʵ���м����Թ�a��Ŀ���ǣ�
��__________________________________��
��__________________________________��
(4)�Թ�b�м��б���Na2CO3��Һ����������______________________��
(5)��Ӧ���������Թ�b�����á��۲쵽��������_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1989������������֯����ȷ��ΪʳƷ��ȾԴ֮һ�����Կ���ʹ�á���������Ӧ��ʱӦ���Կ��Ƶ���
�������Ͻ� ���Ƶ��� ���ƴ��� ��������ˮ ���������մ���ʳƷ���ɼ�
�������������������ӹ���θ��ƽҩƬ �������� ���װ�ǹ���СʳƷ
A. �ۢݢߢ� B. �ޢߢ� C. �ۢݢ� D. �ۢܢݢޢߢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݸ���Ҫ�����
��1����������ά��һ�����Ϳɽ���ĸ߷��Ӳ��ϣ���Ҫ�����ס�С����˵Ⱥ����۵�ũ��ƷΪԭ�ϣ���ˮ��Ϊ�����ǣ�����������������پ����ۺ����ڷ�˿�Ƴɣ���������Ϸ���������������ˮ�У���ˮ������ᣬ���������ÿɷֽ�Ϊ������̼��ˮ�����û�ѧ����ʽ��ʾ�������������̵Ļ�ѧ��Ӧ��
����ĽṹΪ��![]()
��
��
��
��
��
����������Ҳ�������в��䣩
��2����֪CH3Cl+2Na+CH3Cl��CH3��CH3+2NaCl������CH3CH2Br��CH3CHBrCH3�Ļ����������Ʒ�Ӧ���ܵõ������Ľṹ��ʽ�������ǣ�
��
��
��
��
����������Ҳ�������в��䣩
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵�����ʾ��ȷ���ǣ� ��
A.�����ʵ������������������ֱ���ȫȼ�գ����߷ų�������
B.���ʷ�����ѧ�仯ʱһ������������������������
C.ϡ��Һ�У�H+��aq��+OH����aq��=H2O��l������H=��57.3kJ/mol��������0.5molH2SO4��Ũ�����뺬l mol NaOH����Һ��ϣ��ų�����������57.3kJ
D.��25��101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������H2ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��l������H=��285.8kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com