
【题目】如图三条曲线表示 C、Si 和 P 元素的前四级电离能变化趋势。下列说法正确的是

A. 元素电负性:c>b>aB. 最简单氢化物的稳定性:c>a>b
C. 最简单氢化物的相对分子质量:a>b>cD. 第五电离能 I5:a>c>b
【答案】D
【解析】
同主族自上而下第一电离能减小,P元素3p能级为半满状态,较稳定,第一电离能高于同周期相邻Si和S元素,故Si的第一电离能最小,由图中第一电离能c最小,c为Si,P原子第四电离能为失去4s2能中1个电子,为全满稳定状态,与第三电离能相差较大,可知b为P、a为C,据此解答。
同主族自上而下第一电离能减小,P元素3p能级为半满稳定状态,第一电离能高于同周期相邻元素的,故Si的第一电离能最小,由图中第一电离能可知,c为Si,P原子第四电离能为失去4s2能中1个电子,为全满稳定状态,与第三电离能相差较大,可知b为P、a为C。
A、同周期自左而右电负性增大,同主族自上而下电负性减小,故Si的电负性最小,故A错误;
B、Si的非金属性最弱,非金属性越强,氢化物越稳定,故SiH4的稳定性最差,故B错误;
C、均形成分子晶体,没有氢键存在,相对分子质量越大,分子间作用力越强,沸点越高,故SiH4的沸点最高,CH4的沸点最低,故C错误;
D、碳、Si失去4个电子为ns2全满状态,能量更低,再失去1个电子时,第五电离能与第四电离能相差较大,P失去4个电子为3s1状态,第四电离能与第五电离能均失去3s能级电子,二者能量相差不大,故第五电离能C>Si>P,故D正确;
故选D。


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案科目:高中化学 来源: 题型:
【题目】化学电源的发明是化学对人类的一项重大贡献。
(1)将锌片、铜片按照如图所示装置连接,铜片做__极(填“正”或“负”),外电路电子的流向为__(填“Cu→Zn”或“Zn→Cu”)。

(2)若将装置中的稀H2SO4用CuSO4溶液替代,则相应原电池的总反应的化学方程式为__。
(3)下列化学反应通过原电池装置,可实现化学能直接转化为电能的是__(填序号)。
①NaOH+HCl=NaCl+H2O
②CH4+2O2![]() CO2+2H2O
CO2+2H2O
③Fe+Cu2+=Cu+Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,FeS的Ksp=6.3×10-18,CuS的Ksp=1.3×10-36,ZnS的Ksp=1.3×10-24。下列有关说法中正确的是
A. 饱和CuS溶液中Cu2+的浓度为1.3×10-36 mol·L-1
B. 25℃时,FeS的溶解度大于CuS的溶解度
C. 向物质的量浓度相同的FeCl2、ZnCl2的混合液中加入少量Na2S,只有FeS沉淀生成
D. 向饱和ZnS溶液中加入少量ZnCl2固体,ZnS的Ksp变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家合成了一种新的化合物,其结构式如图所示。该物质中 W、X、Y、Z、M是短周期中常见元素,且原子序数依次增大;已知M元素原子核外电子总数是Y元素原子核外 电子总数的两倍。下列说法中错误的是
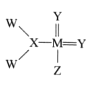
A.由X和Y两种元素形成的化合物有多种
B.W和Z元素位于周期表中同一主族
C.元素的非金属性强弱顺序为:Z>Y>X
D.Y、M元素的气态氢化物沸点高低为:Y>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取Ni2O3.已知草酸的钙、镁、镍盐均难溶于水。工艺流程图如图所示:
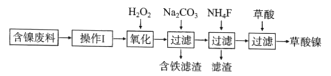
回答下列问题:
(1)“操作I”为“酸浸”,为了提高酸浸的效率,可以采取的措施为__________(写出两条)。
(2)加入H2O2发生的主要反应的离子方程式为________________
(3)加入碳酸钠溶液调pH至4.0~5.0,其目的是___________________
(4)将草酸镍(NiC2O4·2H2O)在热空气中干燥脱水,再采用高温煅烧,可制得Ni2O3,同时获得混合气体,该混合气体的主要成分为水蒸气和_________________
(5)工业上还可用电解法制取Ni2O3用NaOH溶液调 NiCl2,溶液的pH至7.5,加入适量Na 2SO4后利用惰性电极电解。电解过程中产生的Cl2,有80%在弱碱性条件下生成CIO-,再把二价镍氧化为三价镍。CIO-氧化Ni(OH)2生成Ni2O3的离子方程式为_______________________amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为_______mol.
(6)以Al和NiO(OH)为电极,NaOH溶液为电解液组成原电池,放电时NiO(OH)转化为Ni(OH)2,则放电时负极的电极反应式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是合成抗病毒药品洛匹那韦的一种重要中间体。其合成路线如下(其中Ph表示苯基):

回答下列问题:
(1)物质A的化学名称是_______________
(2)反应①所需的试剂和条件是 ______________;反应⑤所属的反应类型为__________________
(3)F中含氧官能团的名称是_______________
(4)反应②的化学反应方程式为______________
(5)有机物X是C的同分异构体,写出满足下列条件的X结构简式为_______________
①苯环上有三个取代基
②分子结构中含有硝基
③核磁共振氢谱有4组峰,峰面积之比为6:2:2:1
(6)写出以![]() 和CH3CN为原料,制备
和CH3CN为原料,制备 的合成路线(无机试剂任选)。_______________
的合成路线(无机试剂任选)。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M为海洋天然产物(一)-PavidolideB不对称全合成的中间体之一,结构简式如下图。下列有关M的说法不正确的是

A. 分子式为C10H14O
B. 可发生取代反应加成反应、聚合反应
C. 分子中所有碳原子都在同一平面上
D. 苯环上连有-OH和-C4H9的M的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为__________,该晶体中原子之间的作用力是_____________。
(2)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(如图)的结构相似,该晶体储氢后的化学式应为______.

(3)立方BP(磷化硼)的晶胞结构如图所示,晶胞中含B原子数目为_____________ 。
(4)科学家把C60和K掺杂在一起制造出的化合物具有超导性能,其晶胞如图所示。该化合物中的K原子和C60分子的个数比为_____________________ 。


(5)铁有γ、δ、α三种同素异形体,γ晶体晶胞中所含有的铁原子数为________,δ、α两种晶胞中铁原子的配位数之比为__________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com