
常温下,浓度均为0.1mol/L的三种溶液:①CH3COOH溶液②NaOH溶液③CH3COONa溶液,下列说法中正确的是(忽略混合前后溶液体积变化)
| A.溶液的pH值:②>③>① |
| B.水电离出的c(OH-):③>①=② |
| C.①和③等体积混合后的溶液:c(CH3COOH)+ c(CH3COO-)=0.1mol/L |
| D.②和③等体积混合后的溶液:c(Na+)=c(CH3COOH)+c(CH3COO-) |
AC
解析试题分析:浓度相同的情况下,碱性越强pH越大,所以强碱>水解呈碱性的盐>酸,A正确;酸碱均抑制水的电离,而水解盐促进水的电离,所以CH3COONa溶液中水电离的氢氧根浓度最大,又浓度相同的情况下强酸强碱对水的抑制强于弱酸弱碱,所以水电离出的c(OH-):③>①>②,B错误;①和③等体积混合后各溶质浓度减半,所以物料守恒式c(CH3COOH)+ c(CH3COO-)=0.1mol/L,C正确;②和③等体积混合后的溶液物料守恒式子应为c(Na+)=2c(CH3COOH)+2c(CH3COO-),所以D错误;故选AC。
考点:本题考查的是离子浓大小的比较,充分运用弱电解质电离的知识和三大守恒解题。


 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:单选题
常温时,下列叙述正确的是 ( )
| A.稀释pH=3的醋酸,溶液中所有离子的浓度均降低 |
B.一定浓度的CH3COOH和NaOH混合,溶液呈中性,则混合液中 |
| C.pH均为11的NaOH和Na2CO3溶液中,水的电离程度相同 |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中一定正确的是
| A.任何浓度溶液的酸碱性都可用pH试纸测定 |
| B.某温度下,pH=6.2的纯水显酸性 |
| C.25℃时,pH=1的醋酸溶液中c(H+)是pH=2的盐酸溶液中c(H+)的10倍 |
| D.25℃时,pH=12的NaOH溶液中的n(OH-)=10-2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是( )
| A.均存在电离平衡和水解平衡 |
| B.存在的粒子种类相同 |
| C.c(OH-)前者大于后者 |
D.分别加入NaOH固体,恢复到原温度,c(C )均增大 )均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
50℃时,下列各溶液中,离子的物质的量浓度关系正确的是( )
| A.pH=4的醋酸中:c(H+)=4.0 mol·L-1 |
| B.饱和小苏打溶液中:c(Na+)=c(HCO3—) |
| C.饱和食盐水中:c(Na+)+c(H+)=c(Cl-)+c(OH-) |
| D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知常温下CH3COOH的电离平衡常数为Ka。常温下,向20 mL 0.1 mol·L-1 CH3COOH溶液中逐滴加入0.1 mol·L-1 NaOH溶液,其pH变化曲线如图所示(忽视温度变化)。下列说法中错误的是( )
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液中c(CH3COO-)>c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中 相等 相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )。
A.0.1 mol·L-1的醋酸溶液加水稀释, 减小 减小 |
| B.体积、pH均相同的醋酸和盐酸完全溶解等量的镁粉(少量),后者用时少 |
| C.向水中加入少量固体硫酸氢钠,c(H+)增大,KW变大 |
| D.常温下,V1 L pH=11的NaOH溶液与V2 L pH=3的HA溶液混合,若混合液显中性,则V1≤V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关说法中正确的是( )
| A.常温下,将1 L pH=12的氨水加水稀释为10 L后溶液的pH=11 |
| B.有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V (乙)>10V(甲) |
C.向浓度均为0.1 mol·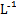 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| D.水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com