
【题目】纯水中c(H+ )=5.0×10﹣7 mol/L,则此时纯水中的c(OH﹣)=;若温度不变,滴入稀硫酸使c(H+)=5.0×10﹣3mol/L,则c(OH﹣)=;在该温度时,往水中滴入NaOH溶液,溶液中的c(OH﹣)=5.0×10﹣2 mol/L,则溶液中c(H+ )= .
【答案】5.0×10﹣7mol/L;5.0×10﹣11mol/L;5.0×10﹣12mol/L
【解析】解:纯水显示中性,c(OH﹣)=c(H+)=5.0×10﹣7mol/L; 此温度下,水的离子积为:Kw=5.0×10﹣7×5.0×10﹣7=2.5×10﹣13 ,
若温度不变,滴入稀硫酸使c(H+)=5.0×10﹣3mol/L,硫酸溶液中氢离子浓度c(H+)=5.0×10﹣3mol/L,c(OH﹣)= ![]() mol/L=5.0×10﹣11 mol/L,
mol/L=5.0×10﹣11 mol/L,
在该温度时,往水中滴入NaOH溶液,溶液中的c(OH﹣)=5.0×10﹣2mol/L,则溶液中c(H+)= ![]() mol/L=5.0×10﹣12mol/L,
mol/L=5.0×10﹣12mol/L,
所以答案是:5.0×10﹣7mol/L;5.0×10﹣11mol/L;5.0×10﹣12mol/L.


科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是

A.a点对应的溶液中:Na+、AlO2-、SO42-、NO3-
B.b点对应的溶液中:Ba2+、K+、NO3-、Cl-
C.c点对应的溶液中:Na+、Ag+、Mg2+、NO3-
D.d点对应的溶液中:Cl-、NO3-、Fe2+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,反应装置略去).
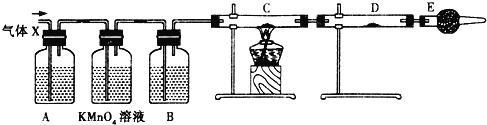
注:C中为氧化铜粉末,试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为:________________________________;
(2)乙同学认为还可能产生氢气的理由是:____________________________________;
(3)丙同学在安装好装置后,必不可少的一步操作是:__________________________;
(4)A中试剂是______,D中试剂是______;
(5)E装置的作用是_________________________;
(6)可以证明气体X中含有氢气的实验现象是:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组的同学为探究和比较SO2和氯水的性质,设计了如下的实验装置。
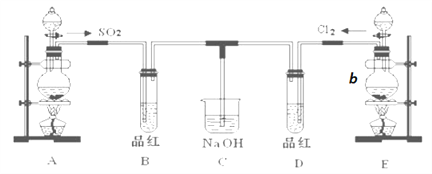
(1)实验室用装置A制备SO2。试剂组合最好是________。
a.稀 H2SO4+Cu b.浓HNO3+Na2SO3 c.70% H2SO4+K2SO3
(2)实验室用装置E制备Cl2,仪器b中装有MnO2粉末。写出仪器b的名称_______,该实验制备Cl2的化学方程式 ___________________________。若该反应消耗8.7g氧化剂,则参加反应的还原剂的物质的量为_____________mol;
(3)反应开始一段时间后,观察到B试管中的品红溶液出现的现象是:_____________;完全反应后,停止通气,再给D试管加热,D试管现象是__________________。
(4)C装置的作用是_______________________。
(5)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在进行中和热的测定中,下列操作错误的是( )
A.测量溶液的温度计要一直插在溶液中
B.应该向酸(碱)中慢慢滴加碱(酸)
C.反应前需要用温度计测量酸(碱)温度
D.反应中酸或碱应适当过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液M中含有MgCl2、KCl和AlCl3,某小组用下图所示过程对其进行处理以获得较纯净的AlCl3溶液。已知:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,请回答:
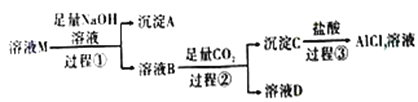
(1)沉淀A的化学式为_______,过程①中Al3+发生反应的离子方程式为_______。
(2)上述过程中的氢氧化钠溶液_____(填“能”或“不能”)用氨水代替,原因是_______。
(3)溶液B中大量存在的阳离子是______,过程③反应的离子方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华民族有着光辉灿烂的发展史。下列过程不涉及元素化合价变化的是
A. 用铁矿石炼铁 B. 黑火药爆炸
C. 石胆(石胆是硫酸铜)化铁为铜 D. 点制豆腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应14CuSO4 +5FeS2 +12H2O=7Cu2S +5FeSO4+12H2SO4,下列结论正确的是
A. FeS2既不是氧化剂,又不是还原剂
B. Cu2S 既是氧化产物,又是还原产物
C. 被氧化的硫和被还原的硫质量比是7∶3
D. 被CuSO4氧化的硫占全部被氧化的硫的2/3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com