
【题目】如图,下列关于新型镁锂双离子二次电池的说法不正确的是
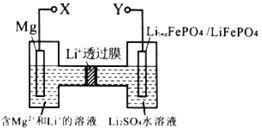
A.充电时,外加电源的正极与 Y 相连
B.充电时,导线上每通过 lmole—,理论上左室电解液质量减轻12 g
C.放电时,Li十由左向右移动
D.放电时,正极的电极反应式为 Li1- xFePO4 +xLi ++xe—=LiFePO4
【答案】B
【解析】
放电时,左边镁为负极失电子发生氧化反应,反应式为Mg-2e-=Mg2+,右边为正极得电子发生还原反应,反应式为![]() ,电解质溶液中锂离子透过锂离子交换膜移向正极;充电时,外加电源的正极与正极相连,阳极上LiFePO4失电子发生氧化反应,负极与负极相连,结合电子转移进行计算解答。
,电解质溶液中锂离子透过锂离子交换膜移向正极;充电时,外加电源的正极与正极相连,阳极上LiFePO4失电子发生氧化反应,负极与负极相连,结合电子转移进行计算解答。
A. 左边镁失电子、为负极,右边电极上得电子、发生还原反应、为正极,即X为负极接线柱、Y为正极接线柱,充电时,外加电源的正极与电池正极相连,负极与电池负极相连,故A正确;
B. 充电时,导线上每通过1mole,左室得电子发生还原反应,反应式为![]() ,但右侧将有1molLi+移向左室,所以溶液质量减轻127=5g,故B错误;
,但右侧将有1molLi+移向左室,所以溶液质量减轻127=5g,故B错误;
C. 放电时,电解质溶液中锂离子透过锂离子交换膜移向正极,即放电时,Li+由左向右移动,故C正确;
D. 右边为正极、得电子、发生还原反应,电极反应式为![]() ,故D正确;
,故D正确;
故答案选:B。


科目:高中化学 来源: 题型:
【题目】几种晶体的晶胞如图所示;所示晶胞从左到右分别表示的物质是
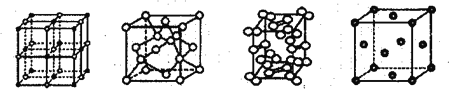
A. 碘、铜、氯化钠、金刚石 B. 氯化钠、金刚石、碘、铜
C. 氯化钠、铜、碘、金刚石 D. 铜、氯化钠碘、金刚石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
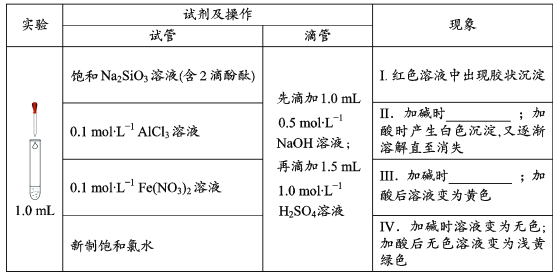
(1)用离子方程式解释现象Ⅰ中出现胶状沉淀的原因:___。
(2)Ⅱ中加碱时出现的现象是___,此现象说明溶液中发生反应的离子方程式是___。
(3)Ⅲ中加碱时出现的现象是___。
(4)滴加试剂顺序的变化,会影响溶液中的现象和发生的反应,请继续分析以下实验。

①探究加酸时Fe(NO3)2溶液中是否发生了反应:
向1.0mL0.1mol/LFe(NO3)2溶液中__,溶液立即变血红,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。
②推测溶液中产生Fe3+的可能原因有两种:
a.酸性条件下,0.1mol/LFe(NO3)2溶液中的Fe2+被NO3-氧化;
b.__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 °C时,MOH的Kb=10-7。该温度下,在20.00 mL0.1 mol· L-1 MCl溶液中滴入0.1 mol·L-1NaOH溶液,溶液的pH与所加NaOH溶液的体积关系如图所示。下列说法错误的是
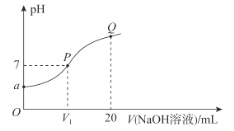
A.a=4B.V1=10
C.溶液中水的电离程度:P>QD.Q点溶液中c(Na+)<2c(M+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物 a(![]() )、b(
)、b(![]() ) 、c(
) 、c(![]() )的说法正确的是
)的说法正确的是
A.a、b 互为同系物
B.C 中所有碳原子可能处于同一平面
C.b 的同分异构体中含有羧基的结构还有 7 种(不含立体异构)
D.a 易溶于水,b 、c 均能使酸性高猛酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下用过量铁块与稀硫酸反应制取氢气,采取下列措施:①将铁块换为等质量的铁粉;②加入少量![]() 溶液;③加入少量
溶液;③加入少量![]() 固体;④加入少量水;⑤加热⑥将稀硫酸换为
固体;④加入少量水;⑤加热⑥将稀硫酸换为![]() 的硫酸,其中可提高
的硫酸,其中可提高![]() 的生成速率的措施有
的生成速率的措施有
A.①③④B.①③⑤C.②④⑤D.②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种形状酷似一条小狗的有机物,化学家 Tim Rickard 将其取名为“doggycene”,有关 doggycene的说法正确的是( )
A.该有机物属于苯的同系物
B.“doggycene”可以使溴水褪色
C.该物质常温下为气态
D.1mol 该物质在氧气中完全燃烧生成 CO2 和水物质的量之比为 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛在木材加工、医药等方面有重要用途。甲醇直接脱氢是工业上合成甲醛的新方法,制备过程涉及的主要反应如下:
反应I:CH3OH(g)![]() HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
HCHO(g)+H2(g) △H1=+85.2kJ·mol-1
反应II:CH3OH(g)+1/2O2(1)![]() HCHO(g)+H2O(g) △H2
HCHO(g)+H2O(g) △H2
反应III:H2(g)+1/2O2(g)![]() H2O(g) △H3=-241.8kJ·mol-1
H2O(g) △H3=-241.8kJ·mol-1
副反应:
反应IV:CH3OH(g)+O2(g)![]() CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
CO(g)+2H2O(g) △H4=-393.0kJ·mol-1
(1)计算反应Ⅱ的反应热△H2=____________________________________________。
(2)750K下,在恒容密闭容器中,发生反应CH3OH(g)![]() HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
HCHO(g)+H2(g),若起始压强为P0,达到平衡转化率为α,则平衡时的总压强P平=___________(用含P0和α的式子表示);当P0=101kPa,测得α=50.0%,计算反应平衡常数Kp=___________kPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
(3)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下:
历程i:CH3OH→H+·CH2OH
历程ⅱ:·CH2OH→·H+HCHO
历程ⅲ:·CH2OH→3·H+CO
历程iv:·H+·H→H2
下图表示一定条件下温度对碳酸钠催化脱氢性能的影响,回答下列问题:
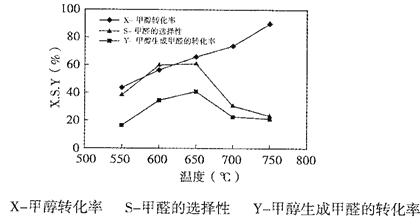
①从平衡角度解析550℃-650℃甲醇生成甲醛的转化率随温度升高的原因___________;
②反应历程i的活化能___________(填“>、“<”或“=”)CH3OH(g)![]() HCHO(g)+H2(g)活化能。
HCHO(g)+H2(g)活化能。
③650℃~750℃,反应历程ii的速率___________(填“>”、“<”或“=”)反应历程ⅲ的速率。
(4)吹脱是处理甲醛废水的一种工艺,吹脱速率可用方程v=0.0423c(mg·L-1·h-1)表示(其中c为甲醛浓度),下表为常温下甲醛的浓度随吹脱时间变化数据。
浓度(mg/L) | 10000 | 8000 | 4000 | 2000 | 1000 |
吹脱时间(h) | 0 | 7 | 23 | 39 | 55 |
则当甲醛浓度为2000mg/L时,其吹脱速率v=___________ mg·L-1·h-1,分析上表数据,起始浓度为10000mg/L,当甲醛浓度降为5000mg/L,吹脱时间为___________h。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com