

���� ��ͭ�Ͻ��ڿ����������������к�������ͭ��������������ϡ���ᣬ���˺�õ�����ͭ��Һ��������ͭ��Һ�м�����������ϡ����������Һ����С����˵õ�Al��OH��3��CuO�����տɵõ�CuAlO2����������Ag���������ʱ������Ϊ�������������ϵõ������ɵõ��ᴿ��Ŀ�ģ�
��1�����ݵ��ԭ�������жϣ���ɫ��NO�ڳ�����������е�O2Ѹ�ٻ������ɺ���ɫN02��
��2��δ���֮ǰ��Cu��OH��2��Al��OH��3��Cu��OH��2�ֽ���¶�Ϊ80���жϲ������������������������Ӧ��
��3�����ݻ��ϼ�������������Լ�ԭ���غ�����ƽ��
��4������ͭԪ���غ㽨����ϵʽ��Cu��CuAlO2�����㣻������Ԫ���غ㽨����ϵʽ��Al2��SO4��3��2CuAlO2�����㣻
��5�����ݿ��������ʴ���Һ����������ķ�����
��� �⣺��ͭ�Ͻ��ڿ����������������к�������ͭ��������������ϡ���ᣬ���˺�õ�����ͭ��Һ��������ͭ��Һ�м�����������ϡ����������Һ����С����˵õ�Al��OH��3��CuO�����տɵõ�CuAlO2����������Ag���������ʱ������Ϊ�������������ϵõ������ɵõ��ᴿ��Ŀ�ģ�
��1����Ʒ�������ʱ������Ϊ����������Ϊ������������ʧ���ӱ�����ӽ�����Һ�ˣ�Ag-e-=Ag+�����������ӵõ������γɵ�������Ag++e-=Ag����ɫ��NO�ڳ�����������е�O2Ѹ�ٻ������ɺ���ɫN02��2NO+O2=2NO2��
�ʴ�Ϊ��Ag++e-=Ag��2NO+O2=2NO2��
��2��δ���֮ǰ��Cu��OH��2��Al��OH��3��Al��OH��3��Cu��OH��2��ʼ�ֽ���¶ȷֱ�Ϊ450���80�棬��к�Cu��OH��2�ֽ��������ͭ����֪BΪAl��OH��3��CuO��������������������Ӧ��Al��OH��3+NaOH=NaAlO2+2H2O��
�ʴ�Ϊ��Al��OH��3��CuO��Al��OH��3+OH-=AlO2-+2H2O��
��3����ӦǰCuΪ+2�ۣ���Ӧ��Ϊ+1�����ϼ۽���1��Al���ϼ�û�б仯��������Ԫ�صĻ��ϼ����ߣ�������������Ӧǰ��Ϊ-2�ۣ���Ӧ��Ϊ0�����ϼ�����2�����ߵ���С��������2���ٸ���ԭ���غ�ã�4CuO+2Al2O3=4CuAlO2+O2����
�ʴ�Ϊ��4��2��4��O2����
��4���ɹ�ϵʽ��Cu��CuAlO2��n��CuAlO2��=$\frac{5000g��63.5%}{64g/mol}$=50.0mol����CuAlO2Ϊ50.0mol��
�ɹ�ϵʽ��Al2��SO4��3��2CuAlO2��Al2��SO4��3=n��CuAlO2����$\frac{1}{2}$=25.0mol��������Ҫ���Ϊ$\frac{25mol}{1mol/L}$
=25.0L��
�ʴ�Ϊ��50��25��
��5����CuSO4��Һ���CuSO4•5H2O���壬��Ҫ��������Ũ������ȴ�ᾧ����ᾧ�������˵Ȳ�����
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
���� ���⿼�����ʵ��Ʊ���Ϊ�߿��������ͣ�������ѧ���ķ����������ʵ�������Ŀ��飬ע��������ʵ������Լ�ʵ������������Ϣ����������غ㶨����ɸ��⣬�Ѷ��еȣ�


 ����������������ϵ�д�
����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��100mL 3mol•L-1������李�NH4Al��SO4��2����Һ����μ���1mol•L-1Ba��OH��2��Һ��
��100mL 3mol•L-1������李�NH4Al��SO4��2����Һ����μ���1mol•L-1Ba��OH��2��Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | һ���¶ȡ�ѹǿ�£�һ���������κ����ʵ�����������ƽ������������ | |
| B�� | ����������һ���ǽ�����������������ﲻһ���Ǽ��������� | |
| C�� | ���ݻ������к�����Ŀ�Ķ��٣��ѻ������ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ��� | |
| D�� | ǿ�������Һ�ĵ�������һ��ǿ�����������Һ�ĵ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǽ�����P��S | |
| B�� | H3PO4��Һ�ĵ�����������H2SO4��Һ | |
| C�� | Na3PO4��Һ�ʼ��ԣ�Na2SO4��Һ������ | |
| D�� | H2SO4��Һ��Na3PO4��Ӧ��������H3PO4��Na2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
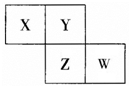 X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����֪Wԭ�ӵ��������������ڲ��������3 ��������˵����ȷ���ǣ�������
X��Y��Z��W��Ϊ������Ԫ�أ�������Ԫ�����ڱ������λ����ͼ��ʾ����֪Wԭ�ӵ��������������ڲ��������3 ��������˵����ȷ���ǣ�������| A�� | �������Ӧˮ��������W��Zǿ | |
| B�� | Y������Z���⻯��ˮ��Һ��Ӧ���г������� | |
| C�� | X����������ǿ��Y���� | |
| D�� | �����ӵİ뾶��Z��W |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ֤�������ԣ�H2O2��Fe3+ǿ | �������ữ��H2O2��Һ����Fe��NO3��2��Һ�У���Һ���ɫ |
| B | ������������NO2 | �ֱ�ͨ����������Һ�У���������ɫ�������������� |
| C | ֤������ˮ�������ȷ�Ӧ | �ڴ�������Һ�е����̪��Һ�����Ⱥ��ɫ���� |
| D | ֤����������ڳ����ܽ�ƽ�� | ����ɫ����������PbI2��ˮ��������ȡ�ϲ���Һ���� NaI���������ɫ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����������������ȡ����Ӧ�����ò���ֻ��һ�� | |
| B�� | ����ˮ������ղ���һ���������� | |
| C�� | ���ۺ���ά�ص���ɶ������ã�C6H10O5��n��ʾ���������Ǽ���ͬϵ������ͬ���칹�� | |
| D�� | ��֬��ʳ������е���Ҫ���֣�Ҳ�Dz���������ߵ�Ӫ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
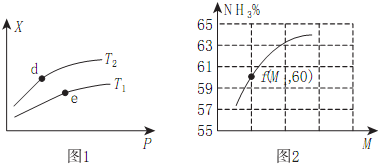 ��֪�й��Ȼ�ѧ����ʽΪ����4NH3��g��+5O2��g��4NO��g��+6H2O��g����H=-905kJ/mol����3H2��g��+N2��g��2NH3��g����H=-92.4kJ/mol����2H2��g��+O2��g��=2H2O��g����H=-483.6kJ/mol����N2��g��+O2��g��=2NO��g����H=QkJ/mol����Ӧ�����йػ�ѧ���ļ��ܣ�kJ/mol�����£�H-O��463��H-N��391��O=O��497
��֪�й��Ȼ�ѧ����ʽΪ����4NH3��g��+5O2��g��4NO��g��+6H2O��g����H=-905kJ/mol����3H2��g��+N2��g��2NH3��g����H=-92.4kJ/mol����2H2��g��+O2��g��=2H2O��g����H=-483.6kJ/mol����N2��g��+O2��g��=2NO��g����H=QkJ/mol����Ӧ�����йػ�ѧ���ļ��ܣ�kJ/mol�����£�H-O��463��H-N��391��O=O��497�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com