
【题目】下列过程仅克服离子键的是( )
A.NaHSO4溶于水B.HCl溶于水C.氯化钠熔化D.碘升华
科目:高中化学 来源: 题型:
【题目】对于下列事实的解释正确的是
A. 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性
B. 浓硝酸在光照下颜色变黄,说明浓硝酸具有挥发性
C. 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D. 氨气可以完成喷泉实验,说明氨气极易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属元素(M)的单质及其化合物说法不正确的是
A. 随核电荷数递增单质的熔点依次降低、硬度依次减小
B. 化合物中M的化合价均为+1价
C. 单质在空气中都剧烈反应,生成M2O2
D. 随核电荷数递增单质与水反应的剧烈程度变强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是关于“外界因素对化学平衡移动影响的实验研究”的课题,回答问题:
(1)影响化学平衡因素的界定:化学平衡发生移动的本质原因是________,所以影响化学平衡的因素可以从分析影响的因素入手.
a. v(正)≠v(逆) ![]() .v(正)和v(逆)都增大
.v(正)和v(逆)都增大 ![]() v(正)和v(逆)都减小
v(正)和v(逆)都减小
(2)研究的思路与方法
①研究对象的选择,现有以下可逆反应:
![]() .
.![]()
![]() .
.![]()
其中,![]() 适合于研究_______对平衡的影响,
适合于研究_______对平衡的影响,![]() 适合于研究_______对平衡的影响.
适合于研究_______对平衡的影响.
![]() .浓度
.浓度![]() .温度
.温度![]() .压强
.压强![]() .催化剂
.催化剂
②研究方法:采用控制其他因素不变,改变其中一个因素的方法,并进行对比实验.
(3)单一因素对化学平衡移动影响的实验研究:
![]() .浓度:将
.浓度:将![]() 与
与![]() 反应后所得的混合液分为
反应后所得的混合液分为![]() 等份,分别加入浓
等份,分别加入浓![]() 溶液、浓
溶液、浓![]() 溶液和
溶液和![]() 固体,观察现象.现象:加入浓
固体,观察现象.现象:加入浓![]() 溶液后的混合溶液红色________,加入
溶液后的混合溶液红色________,加入![]() 固体后,混合溶液红棕色________.
固体后,混合溶液红棕色________.
![]() .温度:将密封并相互连通的盛有
.温度:将密封并相互连通的盛有![]() 的两个玻璃球,一个放人热水中,另一个放入冷水中.
的两个玻璃球,一个放人热水中,另一个放入冷水中.
现象:放入热水中的球内红棕色________;放入冷水中的球内红棕色________.
(4)综合(3)能得出的影响化学平衡移动的原因是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光刻胶的一种合成路线如下:
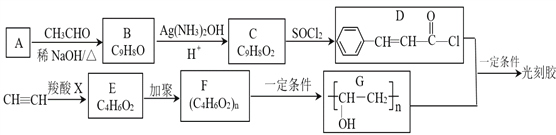
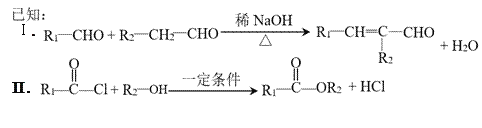
Ⅲ.RCOOH+CH![]() CH
CH![]() RCOOCH=CH2
RCOOCH=CH2
回答下列问题:
(1)A的名称是_______。C中所含官能团的名称是______。
(2)C→D的反应类型是___________,X的结构简式为___________。
(3)D+G→光刻胶的化学方程式_______________________________。
(4)T是C的同分异构体,T具有下列性质或特征:
①能发生水解反应和银镜反应;
②能使溴水褪色;
③属于芳香族化合物。则T的结构有_________种。其中核磁共振氢谱为5组峰,且峰面积比为1∶1∶2∶2∶2的结构简式为___________________________。
(5)根据已有知识并结合相关信息,写出以CH3CH2OH为原料制备CH3CH2CH2COOH的合成路线流程图(无机试剂任用)_________________________。
(合成路线流程图示例如下:![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-53.7kJmol-1 I
CH3OH(g)+H2O(g) △H1=-53.7kJmol-1 I
CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2 II
CO(g)+H2O(g) △H2 II
某实验室控制CO2和H2初始投料比为1︰2.2,在相同压强下,经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[备注]Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJmol-1和-285.8kJmol-1。
②H2O(l)=H2O(g) △H3=+44.0kJmol-1
请回答(不考虑温度对△H的影响):
(1)反应I的平衡常数表达式K=______;反应II的△H2=______kJmol-1.
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有__________。
A.使用催化剂Cat.1 B.使用催化剂Cat.2
C.降低反应温度 D.投料比不变,增加反应物的浓度
E.增大 CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___________________________。
(4)在如图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程-能量”示意图_________。

(5)研究证实,CO2也可在酸性水溶液中通过电解生成甲醇,则生成甲醇的反应发生在______极,该电极反应式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某强酸性溶液X中可能含有Fe2+、A13+、NH4+、CO32ˉ、SO32ˉ、SO42ˉ、C1ˉ中的若干种,现取X溶液进行连续实验,实验过程及产物如下:下列说法不正确的是( ) 
A.气体A是NO
B.X中不能确定的离子是 A13+和C1ˉ
C.溶液E和气体F能发生化学反应
D.X中肯定存在Fe2+、A13+、NH4+、SO42ˉ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com