
������16�֣���ҵ���ð���ʯ�Ʊ��ߴ�����þ�Ĺ����������£�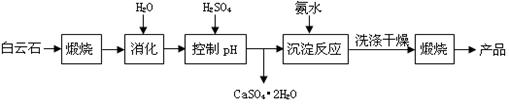
��֪��.����ʯ��Ҫ�ɷֿɱ�ʾΪ��CaO 32.50%��MgO 20.58%��Fe2O3 2.18%��SiO2 0.96%������ 43.78%��
��1��Ϊ����߰���ʯ������Ч�������Բ�ȡ�Ĵ�ʩ�ǽ���ʯ ������ʵ���������հ���ʯ����Ҫ���������ƾ��ơ����ż����⣬����Ҫ ������ţ���
A�������� B������ C�������� D��ʯ����
��2������H2SO4����pHʱ���յ�pH�Բ�Ʒ��Ӱ����ͼ8��ʾ������ͼʾ�ɵõ��Ľ��ۼ�ԭ���ǣ�
��pH���ᵼ��___________________________�½�����ԭ����_______________________
��pH���ͻ�����____________________________ ����ԭ�������__________(�����)
A.Fe2O3����H2SO4����ʹ��Ʒ�������� B.SiO2����H2SO4����ʹ��Ʒ��������
C.���Թ�ǿ���γɿ��ܵ�Ca(HSO4)2������ʹ��Ʒ���к��Ƶ�����
��3����֪MgSO4��CaSO4���ܽ�����±���
| �¶ȣ��棩 | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
| pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
| ��ɫ | ��ɫ | ��ɫ | ��ɫ |
32. �𰸣�16�֣�
��1������ ��2�֣�BC ��2�֣�
��2����þ�����ʽ��ͣ�1�֣�Mg(OH)2��MgOδ��ȫ�ܽ⣨1�֣�
�ڲ�Ʒ�����½���1�֣�AC ��1�֣�
��3�����½ᾧ�����ȹ��� ��2�֣���1�֣���
��4��Mg2+ +2NH3.H2O = Mg(OH)2��+ 2NH4+��2�֣�
��5��(NH4)2SO4��2�֣�
��6����ɫ ��2�֣�
������������� ��1����߿�ʯ����Ч���Ĵ�ʩͨ���ǶԿ�ʯ���з��鴦����������Ӧ�ĽӴ�������Ӷ��ӿ췴Ӧ���ʣ�ʹ���ո��ӳ�֡�����ʵ�������հ���ʯ��������Ҫ������װ���оƾ��ơ����żܡ��������������ᡢ��ǯ�ȣ����Դ˴�����ѡBC��
��2����ͼ�������������ߣ�������ʾ�����ϴ�ڵ����þ���������ߣ����������ź������յ�pH�������ֳ����½������ƣ��ҵ�pH>6ʱ���������½���Խ��Խ�죻�������ϴ�С�����������þ�Ĵ��ȣ��ô������ź������յ�pH��������ֳ���������ƣ����ǽϲ�ͬ���ǣ���ʼ����Ѹ�٣���pH>6ʱ������þ�Ĵ����������ԡ����Ԣ�pH���ᵼ��þ�Ľ����ʽ��ͣ�ԭ���Ǽ������ܽ�ʱ����pH���ߣ��������MgO������ȫ�ܽ⡣
��pH���ͻ������Ƶõ�����þ�Ĵ���ƫ�ͣ�ԭ���ǰ���ʯ�е�����������Fe2O3��CaO�����������ᣬ�������ɿ��ܵ����ʣ�����AC���п��ܣ�ѡAC��
��3���ɱ������ݿ�֪������þ������ˮ���ܽ�����¶����߶����ߣ��������������ˮ�������¶������ܽ�Ȼ������䣬�������ö����ܽ���ϵIJ��죬��Ҫ��������ƾ����������Բ�ȡ�Ĵ�ʩ�����½ᾧ�����ȹ��ˡ�
��4�����������з�Ӧ���е���ҪΪþ���ӣ����Լ��백ˮ����ˮ��þ���ӽ�����ɳ���������þ���������ӷ���ʽ��Mg2+ +2NH3.H2O = Mg(OH)2��+ 2NH4+ ��ע�ⰱˮ���ܲ�
��5����������������Mg(OH)2 ����Һ��ʣ��NH4+ ��SO4 2-�����Կ������ô�ʣ����Һ�Ƶø���Ʒ(NH4)2SO4 �������������ʡ�
��6�����͵�������þ��Һ����Mg(OH)2 ��s��= Mg2+��aq�� + 2 OH-��aq���ܽ�ƽ�⣬2c��Mg2+��= c��OH -�������ܶȻ�Ksp= c��Mg2+��c2��OH -��=5.6��10-12 ���ɴ˿��Եó�c��OH -��=3.6��10-4 ������pH>9.6�����Լ���������ָʾ������Һ����ɫ��
���㣺���⿼����ǻ�ѧ�������̡�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���з�Ӧ����������ԭ��Ӧ���� (����)
| A��CaCO3��2HCl===CaCl2��CO2����H2O | B��CO2��H2O===H2CO3 |
| C��2H2O2���� 2H2O��O2�� | D��CaCO3 CaO��CO2�� CaO��CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ����
| A����Ȼ��֬�ķ����к����������������� |
| B��ú��������Ϊ����ȼ�ϵĹ������������仯 |
| C��A12O3������ˮ��Ӧ�õ����Ӧˮ���� Al(OH)3 |
| D�������ü���ʹ�����ʱ��Եķ��������ᴿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�ϵ�������Ⱦ�����������ܵ���ע�����д����ϵ�ص���ҪĿ����
| A������ʯī�缫 |
| B�����յ����ǵĽ������� |
| C����ֹ�������й�ĵ��Һ��ʴ������Ʒ |
| D����ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ����Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
��16�֣��Ի�����Ϊԭ��������������������к�Fe2O3��SiO2��Al2O3��MgO�ȣ����������Ʊ����죨Fe2O3���Ĺ������£�
��1�����ܹ�����Fe2O3��ϡ���ᷴӦ�Ļ�ѧ����ʽΪ ��
������A����Ҫ�ɷݵĻ�ѧʽΪ ��
��2����ԭ�����м���FeS2��Ŀ���ǽ���Һ�е�Fe3 +��ԭΪFe2 +��������������ΪH2SO4������ɸ÷�Ӧ�����ӷ���ʽ��FeS2 + 14Fe3 + + H2O="=" 15Fe2 + + SO42- + ��
��3�����������У�O2��NaOH��Fe2+��Ӧ�����ӷ���ʽΪ ��
��4��Ϊ��ȷ�����������������������Ҫ������Һ��pH�ķ�Χ�� ���������ӳ�����pH���±�������ҺB���Ի��յ������У�д��ѧʽ�� ��
| ������ | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| ��ʼ����pH | 2.7 | 3.8 | 7.6 | 9.4 |
| ��ȫ����pH | 3.2 | 5.2 | 9.7 | 12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
ij����С���������Լس�ʯ��K2O?Al2O3?6SiO2)Ϊԭ�ϣ���ȡA12O3��K2CO3�����ʣ������������£�
��1�������ա������������·�Ӧ������
�ټس�ʯ�еĹ�Ԫ����CaCO3������ת��ΪCaSiO3��д��SiO2ת��ΪCaSiO3�Ļ�ѧ����ʽ_____________________��
�ڼس�ʯ�еļ�Ԫ�غ���Ԫ����Na2CO3������ת��Ϊ�����Ե�NaAlO2��KAlO2��д��Al2O3ת��ΪNaAlO2�Ļ�ѧ����ʽ____________________________��
��2����֪NaAlO2��KAlO2�������·�Ӧ��AlO2��+2H2O Al(OH)3+OH����
Al(OH)3+OH����
����ȡ��ʱ��Ӧ������Һ��______�ԣ���ᡱ���������ȡ��ʱ���Ͻ����Ŀ����______________��
��3����ת����ʱ����NaOH����Ҫ������_______ (�����ӷ���ʽ��ʾ����
��4�����������п���ѭ�����õ���Ҫ������_______��_______��ˮ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
����ѧѡ��2����ѧ�뼼������15�֣���ҵ������������ʱ����ͬʱ������һ�ֳ�������Ҫ������������Ư����������(NaClO2)���乤���������£�
��֪����NaHSO4�ܽ�����¶ȵ����߶������ʵ� �����¿ɽᾧ������
�ڸ�����������Ϊֹ������֪���е���ǿ�ᣬ�е�90 �档
��ش��������⣺
��Ӧ�����з�����Ӧ�Ļ�ѧ����ʽΪ ����ȴ��Ŀ���� ��������������������ԭ���� ��
��2)��Ӧ�����з�����Ӧ�����ӷ���ʽΪ ��
��3��ͨ�뷴Ӧ�����е�SO2��H2O2����ͬ��������NaClO2�����Ҫ˵��˫��ˮ�ڷ�Ӧ���ܴ���SO2��ԭ���� ��
��4��Ca(ClO)2��ClO2��NaClO2�Ⱥ��Ȼ����ﶼ�dz��õ���������Ư��������Ϊ���Ƕ����� ����д����ҵ����������NaOH��Һ����������NaClO�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
A��B��C��D��E��FΪǰ�����ڵ�Ԫ�ء����У�AԪ�غ�BԪ�ص�ԭ�Ӷ���һ��δ�ɶԵ��ӣ�A3+��B-��һ�����Ӳ㣬Bԭ�ӵ�һ�����Ӻ�3p���ȫ������Cԭ�ӵ�p�������3��δ�ɶԵ��ӣ�����̬�⻯����ˮ�е��ܽ�����ͬ��Ԫ�����γɵ��⻯�������D������ϼ�����ͻ��ϼ۴�����Ϊ4��������������Ӧ��ˮ�������������ȡըҩ������Ǧ���أ�EԪ�صĻ�̬ԭ�Ӻ����������˶�״̬�ĵ��ӣ�FԪ�صĵ���Ϊ�Ϻ�ɫ���壬��ͨ����ʪ��ұ�𡱶��á���ش��������⣺
��1��CB3��������ԭ�ӵ��ӻ������� ��
��2��FԪ�ص�ԭ�ӵ���Χ�����Ų�ʽΪ ����ͼ��ʾΪF��Au��3��1�γɵĺϽ�ͼ����ͼ�е�������д����Ӧ��Ԫ�ط��š�
��3��B��DԪ������������Ӧ��ˮ���������ǿ���� �� ���ѧʽ����
��4���õ��߽�A��F�ĵ������ɵĵ缫�������������뵽ʢ��C������������ˮ�����Ũ��Һ�й���ԭ��أ���д���ڵ���A���淢����Ӧ�ĵ缫��Ӧʽ��_____��
��5������R����CԪ������Ԫ���γɵ�18���ӷ��ӣ�R�ĵ���ʽΪ ��
��6��24 g E�ĵ�����33.6 L��������״������ȼ�գ�����Ӧ��ȫ���ľ����ų�x kJ��������1mol E��O2��Ӧ����E�ĵͼ�������ʱ���Ȼ�ѧ����ʽΪ ����֪��E��ȼ����Ϊy kJ/mol����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
(15 ��)
���ĵð������������ಡ��ҩ�����������һ�ֺϳ�·��(���巴Ӧ�����Ͳ����Լ���)��
�ش��������⣺
��1���Լ�a�� ���Լ�b�Ľṹ��ʽΪ ��b�й����ŵ������� ��
��2���۵ķ�Ӧ������ ��
��3���ĵð��ķ���ʽΪ ��
��4���Լ�b���ɱ��龭������Ӧ�ϳɣ�
��Ӧ1���Լ�������Ϊ ��
��Ӧ2�Ļ�ѧ����ʽΪ ��
��Ӧ3�ķ�Ӧ������ ��(����������Ҳ����)
��5�����㻯����D��1�����ӵ�ͬ���칹�壬������������������ţ��ܷ���������Ӧ��D�ܱ�KMnO4������Һ������E( C2H4O2) �ͷ��㻯����F (C8H6O4)��E��F��̼��������Һ��Ӧ���ܷų�CO2���壬F�����ϵ�һ��������ֻ��һ�֡�D�Ľṹ��ʽΪ ��
��F����һ��������Ļ�ѧ����ʽΪ ��
��������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com