
| 1.92g |
| 64g/mol |
| 1.12L |
| 22.4L/mol |
| 1.92g |
| 64g/mol |
| 1.12L |
| 22.4L/mol |
| 0.03mol×2 |
| 4 |


科目:高中化学 来源: 题型:

2- 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH3CH2OH
| |||
B、CH3CHBrCH3+NaOH
| |||
C、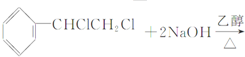  | |||
D、2CH3OH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于0.6mol |
| B、等于1mol |
| C、0.6mol<n(CO2)<1mol |
| D、大于1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、m+2、10+n |
| B、m、n |
| C、3、7 |
| D、m-2、10-n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、布朗运动是胶体微粒特有的运动方式,只用肉眼就可以把胶体和溶液、浊液区别开来 |
| B、向Fe(OH)3胶体中加入少量H2SO4溶液,会生成红褐色沉淀 |
| C、可利用丁达尔效应区分胶体与溶液 |
| D、胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HOCH2COOH |
| B、HO-CH2CH2-CHO |
| C、HOOC-COOH |
| D、CH3COOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com