
| A、清晨,在树林中,常看到从枝叶间透过的一道道光柱,这是胶体产生的丁达尔效应 |
| B、某固体A能导电,一定是金属 |
| C、由同种元素组成的物质肯定属于纯净物 |
| D、由氯化铵溶液呈弱酸性可知氯化铵是弱电解质 |


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
| A、要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水 |
| B、向FeCl2溶液中加入氨水,最终会看到红褐色沉淀 |
| C、保存硫酸亚铁溶液时常在其中加颗铁钉 |
| D、氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①③④⑤⑥ |
| C、②③⑥ | D、②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向氯化铝溶液中加入过量的氨水:3NH3?H2O+A13+═3NH4++Al(OH)3↓ |
| B、NaOH溶液吸收少量CO2:OH-+CO2═HCO3- |
| C、向氯化铁溶液中加入铜粉发生的反应:Cu+Fe3+═Cu2++Fe2+ |
| D、Na2O2与水的反应:Na2O2+H2O═2Na++2OH-+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O2的电子式: | ||
| B、氯气的结构式:Cl-Cl | ||
C、CO2的比例模型: | ||
D、原子核内有20个中子的氯原子:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
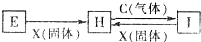 有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )
有关物质的转化关系如图所示(部分物质和条件已省去),C、X均是单质,H溶液呈浅绿色,I溶液呈棕黄色.下列有关判断正确的是( )| A、X固体可能是碘单质 |
| B、图中所示反应均为氧化还原反应 |
| C、1mol C与E溶液完全反应转移电子数为NA(NA为阿伏加德罗常数) |
| D、E、H、I溶液配制时,均需加酸防止其水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com