
【题目】自然界氮的循环过程如图.回答下列问题。
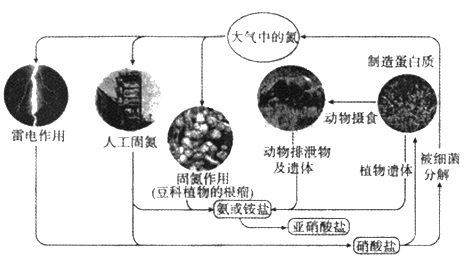
(1)上图中包含了_____种氮的固定方式,写出属于雷电作用固氮的化学方程式________。
(2)合成氮反应常用铁触媒催化剂,下列关于催化剂的说法不正确的是______。
A.可以加快反应速率 B.可以改变反应热
C.可以减少反应中的能耗 D.可以增加活化分子的数目
(3)氮的循环中,亚硝酸盐是重要的一环,利用化合价可推知亚硝酸盐具有_____性和_____性,亚硝酸盐和酸性高锰酸钾反应的离子方程式为__________________。
(4)某同学加热Fe(NO3)2时,发现得到了红色固体和红色气体,且所得气体被水充分吸收后体积少于原体积的l/3,Fe(NO3)2热分解的化学方程式为_______________。
【答案】 3 N2+O2![]() 2NO B 氧化 还原 5NO2-+2MnO4-+6H+=2Mn2++5NO3-+3H2O 4Fe(NO3)2
2NO B 氧化 还原 5NO2-+2MnO4-+6H+=2Mn2++5NO3-+3H2O 4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑
2Fe2O3+8NO2↑+O2↑
【解析】(1)图中包含了三种氮的固定方式,即人工固氮、自然固氮和根瘤菌固氮;放电条件下氮气转化为NO,NO与氧气化合生成NO2,NO2溶于水生成硝酸,因此雷电作用固氮的化学方程式为N2+O2![]() 2NO。(2)A.催化剂可以加快反应速率,A正确;B.催化剂不能改变反应热,B错误;C.催化剂能降低活化能,因此可以减少反应中的能耗,C正确;D. 催化剂能降低活化能,可以增加活化分子的数目,D正确,答案选B。(3)亚硝酸盐中氮元素是+3价,处于中间价态,因此可推知亚硝酸盐具有氧化性和还原性;高锰酸钾具有强氧化性,亚硝酸盐和酸性高锰酸钾反应的离子方程式为5NO2-+2MnO4-+6H+=2Mn2++5NO3-+3H2O。(4)某同学加热Fe(NO3)2时,发现得到了红色固体和红色气体,分别是氧化铁和NO2,所得气体被水充分吸收后体积少于原体积的l/3,这说明反应中还有氧气生成,所以Fe(NO3)2热分解的化学方程式为4Fe(NO3)2
2NO。(2)A.催化剂可以加快反应速率,A正确;B.催化剂不能改变反应热,B错误;C.催化剂能降低活化能,因此可以减少反应中的能耗,C正确;D. 催化剂能降低活化能,可以增加活化分子的数目,D正确,答案选B。(3)亚硝酸盐中氮元素是+3价,处于中间价态,因此可推知亚硝酸盐具有氧化性和还原性;高锰酸钾具有强氧化性,亚硝酸盐和酸性高锰酸钾反应的离子方程式为5NO2-+2MnO4-+6H+=2Mn2++5NO3-+3H2O。(4)某同学加热Fe(NO3)2时,发现得到了红色固体和红色气体,分别是氧化铁和NO2,所得气体被水充分吸收后体积少于原体积的l/3,这说明反应中还有氧气生成,所以Fe(NO3)2热分解的化学方程式为4Fe(NO3)2![]() 2Fe2O3+8NO2↑+O2↑。
2Fe2O3+8NO2↑+O2↑。


科目:高中化学 来源: 题型:
【题目】芳香化合物A是一种基本化工原料,可以从煤和石油中得到。OPA是一种重要的有机化工中间体.A、B、C、D、E、F和OPA的转化关系如下所示:

回答下列问题:
(1)A的化学名称是____________;
(2)由A生成B 的反应类型是____________,在该反应的副产物中,与B互为同分异构体的化合物的结构简式为____________;
(3)写出C所有可能的结构简式____________;
(4)D(邻苯二甲酸二乙酯)是一种增塑剂.请用A、不超过两个碳的有机物及合适的无机试剂为原料,经两步反应合成D。用结构简式表示合成路线____________;
(5)OPA的化学名称是____________,OPA经中间体E可合成一种聚酯类高分子化合物F,由E合成F的反应类型为____________,该反应的化学方程式为____________;(提示![]() )
)
(6)芳香化合物G是E的同分异构体,G分子中含有醛基、酯基和醚基三种含氧官能团,写出G所有可能的结构简式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据叙述判断下列各元素一定属于主族元素的是
A. 元素的原子最外层电子数为2 B. 元素的原子最外层电子数为6
C. 位于元素周期表中ⅡA族右边的元素 D. 阴离子RO4—中R元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Na、Na2O,Na2O2的混合物与足量的水反应,在标准状况下得到672mL混合气体,将混合气体通电后恰好完全反应,则Na、Na2O,Na2O2的物质的量之比为( )
A.4:3:2
B.1:2:1
C.2:1:1
D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】夏天用食醋调凉拌菜时,醋酸的作用:①使凉拌菜味美可口;②增进食欲、帮助消化;③抑菌杀菌、预防肠道疾病;④增加糖类等营养成分的吸收。其中说法正确的是( )
A. 只有① B. ①和② C. ①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组热化学方程式中化学反应的ΔH前者大于后者的是( )
①C(s)+O2(g)=CO2(g) ΔH1 C(s)+![]() O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)=SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+![]() O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
O2(g)=H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO+H2O(l)===Ca(OH)2(s) ΔH8
A. ①③④ B. ②③④ C. ①④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把煤作为燃料可通过下列两种途径:
途径Ⅰ C(s) + O2(g) = CO2(g);ΔH = -393.15 kJ·mol-1 ①
途径Ⅱ 先制成水煤气:
C(s) + H2O(g) = CO(g) + H2(g); ΔH2 ②
再燃料水煤气:
2CO(g) + O2(g) = 2CO2(g); ΔH= -566kJ·mol-1 ③
2H2(g) + O2(g) = 2H2O(g);ΔH= -484 kJ·mol-1 ④
请回答下列问题:
(1)途径Ⅰ放出的热量理论上_________(填“大于”“等于”或“小于”)途径Ⅱ放出的热量。
(2)ΔH2=_______________。
(3)煤燃烧的烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)==NO2(g)+O2(g) ΔH=-200.9kJ·mol-1
NO(g)+![]() O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
O2(g)==NO2(g) ΔH=-58.2kJ·mol-1
SO2(g)+O3(g)==SO3(g)+O2(g) ΔH=-241.6kJ·mol-1
反应3NO(g)+O3(g)==3NO2(g)的ΔH=________kJ·mol-1。
(4)已知下列各组热化学方程式
① Fe2O3(s)+3CO(g)=2Fe(s)+3CO2 △H=-25kJ/mol
② 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47kJ/mol
③ Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________________________。
(5)在标准状况下的11.2L甲烷完全燃烧生成CO2 和液态水放出444.8kJ热量(298K),其燃烧热的热化学方程式______________________________________________________; 已知断裂下列1mol化学键需要吸收的能量分别为:C=O:745kJ/mol , O=O:496kJ/mol , C-H:414kJ/mol 则断裂1molH-O键需要提供的能量为____________________ kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支50mL酸式滴定管中盛盐酸,液面恰好在a mL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( )
A.a mLB.(50-a) mLC.大于(50-a)mLD.大于a mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com