
铁是人类较早使用的金属之一。运用所学知识,回答下列问题。
(1)鉴别Fe(OH)3胶体和FeCl3溶液的方法是 。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式: 。
(3)某研究性学习小组为测定FeCl3腐蚀铜后所得溶液的组成,进行了如下实验:
①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是 ;②溶液组成的测定:取50.0mL待测溶液,加入足量的AgNO3溶液,得21.525g白色沉淀。则溶液中c(Cl-)= mol·L-1。
③验证该溶液中含有Fe2+,正确的实验方法是 。
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若褪色,证明含有Fe2+
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显血红色,证明原溶液中含有Fe2+
(4)工程师欲从制造印刷电路板的废水中回收铜,并获得FeCl3溶液,设计如下方案: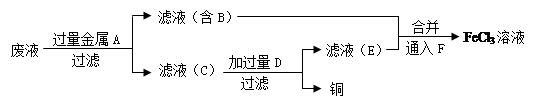
①滤渣C的化学式为 。
②加过量D发生反应的离子方程式为 。
③通入F发生反应的化学方程式为 。
(1)用平行光照射两种分散系(或丁达尔现象)
(2)2Fe3++Cu=2Fe2++Cu2+
(3)①Fe3+、Fe2+、Cu2+ ②3 ③B
(4)①Fe、Cu ②Fe+2H+=Fe2++H2↑ ③2FeCl2+Cl2=2FeCl3
解析试题分析:(1)胶体会产生丁达尔效应,但是溶液不能。因此鉴别Fe(OH)3胶体和FeCl3溶液的方法是用平行光照射两种分散系(或丁达尔现象)。(2)FeCl3有氧化性,能把铜氧化为Cu2+。反应的离子方程式为:2Fe3++Cu=2Fe2++Cu2+。(3)①取少量待测溶液,滴入KSCN溶液呈红色,则待测液中含有的金属阳离子是Fe3+;由于发生了反应2Fe3++Cu=2Fe2++Cu2+,所以溶液中还含有Fe2+、Cu2+。②n(AgCl)= n(Cl-)=21.525g÷143. 5g/mol="0.15mol." 则溶液中c(Cl-)=n(Cl-)÷V=0.15mol÷0.05L=3mol/L。③A.因为溶液中含有Fe3+,Fe3+的黄色要比Fe2+的浅绿色深,所以无法看出该现象。错误。B.Fe2+有还原性,容易被酸性高锰酸钾溶液氧化而使之褪色。因此若看到溶液褪色,证明含有Fe2+。正确。C.原溶液中含有Fe3+,所以无论是否滴入氯水,都会发生该现象。错误。因此正确选项为B。(4)向反应后的溶液中加入过量的金属Fe,发生反应:Fe+CuCl2=FeCl2+Cu,,然后过滤得到滤液B中含有FeCl2;滤渣C中含有Fe、Cu。向滤渣中加入过量的盐酸,发生反应:Fe+2HCl= FeCl2+ H2↑. 离子方程式为:Fe+2H+= Fe2++H2↑。滤液E中含有FeCl2,将其与滤液B混合,然后向该溶液中滴加新制的过量的氯水,发生反应2FeCl2+Cl2=2FeCl3。最后得到FeCl3溶液。
考点:考查铁三角的关系、Fe3+\Fe2+的检验、化学方程式、离子方程式的书写的知识。


科目:高中化学 来源: 题型:单选题
现有①氧气;②空气;③碱式碳酸铜;④氯酸钾;⑤硫;⑥水;⑦氧化镁;⑧氯化钠等物质,其中属于单质的有(填序号) ;属于化合物的有 ,属于混合物的有 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中,正确的是
| A.CO、NO都是大气污染物,在空气中都能稳定存在 |
| B.SiO2是酸性氧化物,能与NaOH溶液反应 |
| C.溶液、胶体和悬浊液的本质区别是分散质微粒是否带电荷 |
D.日本核泄漏产生了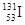 原子,其中子数比 原子,其中子数比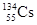 的中子数少2 的中子数少2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
无机化合物可根据其组成和性质进行分类。
(1)如图所示的物质分类方法是 。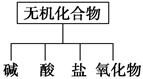
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥的后面。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ② | ③ ④Ba(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(18分)⑴有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融硝酸钾;⑥乙醇; ⑦稀硫酸; ⑧金刚石; ⑨二氧化硫 ; ⑩冰醋酸。
其中能导电的有 ;属于非电解质的有 ;属于强电解质的有 ;(填序号)
⑵常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈 性,溶液中c(NH4+)与c(Cl-)的大小关系是:c(NH4+) c(Cl-);
⑶常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和 14,常温下,pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和 14(填>,<或=)
⑷用物质的量浓度为0.04 mol·L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol·L-1的氨水溶液20mL,消耗盐酸12.5mL,则此氨水物质的量浓度为 mol·L-1;电离度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列十种物质:
①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
请根据如图所示回答下列问题:
(1)纳米是________单位,1纳米等于________米。纳米科学与技术是研究结构尺寸在1至100纳米范围内材料的性质与应用。它与________分散系的粒子大小一样。
(2)世界上最小的马达,只有千万分之一个蚊子那么大,如图,这种分子马达将来可用于消除体内垃圾。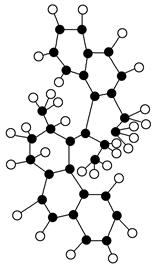
①该图是马达分子的____________模型。
②该分子中含有的组成环的原子是____________元素的原子,分子中共有____________个该原子。
③纳米产品以其优异的性能令人向往,下列关于纳米用品的说法中错误的是________。
a.现代家庭普遍使用的电冰箱大多都是“纳米冰箱”,它耗电少且无污染
b.现代商场里的高档衣服都是“纳米衣服”,它冬暖夏凉且无污染
c.专供幼儿、学生饮用的“营养强化牛奶”是“纳米牛奶”,它能使人增强记忆力
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有下列物质:①Na2CO3 ②铜 ③氯化氢 ④CO2 ⑤NaHSO4 ⑥Ba(OH)2 ⑦氢氧化铁胶体 ⑧氨水 ⑨稀硝酸 ⑩KI
(1)按物质的分类方法填写表格的空白处(填物质编号)
| 分类标准 | 电解质 | 盐 | 非电解质 | 混合物 |
| 属于该类 的物质 | | | | |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
向含有0.2 mol NaOH和0.1 mol Ba(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为8.96L(0℃,1.01×105 Pa)时立即停止,则这一过程中,溶液中离子的物质的量与通入CO2气体的体积关系图象正确的是(不考虑气体的溶解和离子与水反应) ( )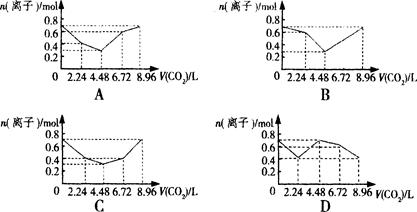
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com