
����Ŀ�����ͪ�������ɱ�淽���ر�Զ����нϺõ�ɱ�����ã��ҹ���ѧ���о���һ�����ͪ�����ĺϳ�·�����£�

�ش��������⣺
(1)A�Ļ�ѧ����Ϊ ______��
(2) B�к��������ŵ�������_____��
(3) B��C�ķ�Ӧ������_____��
(4)д��C����������������Һ��Ӧ�Ļ�ѧ����ʽ_____��
(5) D�Ľṹ��ʽΪ_____��
(6)д����B��Ϊͬ���칹�����ʹFe3+��ɫ���ܷ���ˮ�ⷴӦ�Ļ�����Ľṹ��ʽ(�˴Ź�������Ϊ����壬�������Ϊ1 : 2 : 2 : 3) _____��
(7)������ɱ��Ӻ������Ϊ��ʼԭ���Ʊ�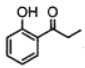 �ĺϳ�·��(���Լ���ѡ) _____��
�ĺϳ�·��(���Լ���ѡ) _____��
���𰸡��䱽���� �ǻ����ʻ� ȡ����Ӧ 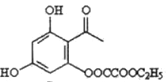 +5NaOH
+5NaOH![]()
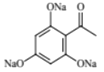 +NaOOCCOONa+C2H5OH+3H2O
+NaOOCCOONa+C2H5OH+3H2O 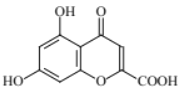
 ��
�� CH3CH2CH2Br
CH3CH2CH2Br![]() CH3CH2CH2OH
CH3CH2CH2OH![]() CH3CH2CHO
CH3CH2CHO![]() CH3CH2COOH
CH3CH2COOH![]()
��������
���A�ķ���ʽ����B�Ľṹ���ƿ�֪A��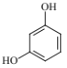 ��A��CH3COOH��ZnCl2����ʱ������ȡ����Ӧ����B��
��A��CH3COOH��ZnCl2����ʱ������ȡ����Ӧ����B��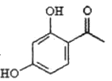 ��B��H5C2OOCCOOC2H5��CH3CH2OH��CH3CH2ONa�����·���ȡ����Ӧ����C:
��B��H5C2OOCCOOC2H5��CH3CH2OH��CH3CH2ONa�����·���ȡ����Ӧ����C:  ��C��ϡ������Һ�м��ȣ�������Ӧ����D������D��NH2CH3��Ӧ������E�ṹ���ƿ�֪D��
��C��ϡ������Һ�м��ȣ�������Ӧ����D������D��NH2CH3��Ӧ������E�ṹ���ƿ�֪D��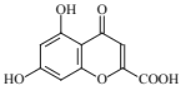 ��B�ṹΪ
��B�ṹΪ ������ʽ��C8H8O3������ӵ�ͬ���칹����ʹFe3+��ɫ˵�����з��ǻ����ܷ���ˮ�ⷴӦ˵���������������ݺ˴Ź�������Ϊ����壬�������Ϊ1 : 2 : 2 : 3�ƶ�����ܵĽṹ��(7)1-�������NaOH��ˮ��Һ���ȷ�Ӧ����1-������ʹ1-����������Ϊ��ȩ����ȩ�������������ᣬ�����뱽����ZnCl2����ʱ����ȡ����Ӧ����
������ʽ��C8H8O3������ӵ�ͬ���칹����ʹFe3+��ɫ˵�����з��ǻ����ܷ���ˮ�ⷴӦ˵���������������ݺ˴Ź�������Ϊ����壬�������Ϊ1 : 2 : 2 : 3�ƶ�����ܵĽṹ��(7)1-�������NaOH��ˮ��Һ���ȷ�Ӧ����1-������ʹ1-����������Ϊ��ȩ����ȩ�������������ᣬ�����뱽����ZnCl2����ʱ����ȡ����Ӧ����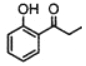 ��
��
(1)���A�ķ���ʽ����B�Ľṹ���ƿ�֪A�� ������Ϊ�䱽���ӣ���1��3-�����ӣ�
������Ϊ�䱽���ӣ���1��3-�����ӣ�
(2)B�ṹ��ʽΪ ����֪B�к��еĹ�����Ϊ���ǻ����ʻ���
����֪B�к��еĹ�����Ϊ���ǻ����ʻ���
(3) B�� ��B��H5C2OOCCOOC2H5��CH3CH2OH��CH3CH2ONa�����·���ȡ����Ӧ����C:
��B��H5C2OOCCOOC2H5��CH3CH2OH��CH3CH2ONa�����·���ȡ����Ӧ����C:  ��C2H5OH������B��C�ķ�Ӧ������ȡ����Ӧ��
��C2H5OH������B��C�ķ�Ӧ������ȡ����Ӧ��
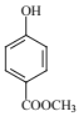
(4) CΪ �������к��з��ǻ�������������������������Һ�ڼ���ʱ���ǻ���������������Ӧ����Ӧ�Ļ�ѧ����ʽΪ
�������к��з��ǻ�������������������������Һ�ڼ���ʱ���ǻ���������������Ӧ����Ӧ�Ļ�ѧ����ʽΪ +5NaOH
+5NaOH![]()
 +NaOOCCOONa+C2H5OH+3H2O��
+NaOOCCOONa+C2H5OH+3H2O��
(5)D����ʽ��C10H6O6����NH2CH3������Ӧ����E�Ľṹ��ʽΪ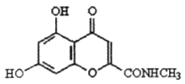 �����ƿ�֪D�ṹ��ʽΪ
�����ƿ�֪D�ṹ��ʽΪ ��
��
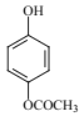
(6)B�ṹΪ ������ʽ��C8H8O3������ӵ�ͬ���칹����ʹFe3+��ɫ˵�����з��ǻ����ܷ���ˮ�ⷴӦ˵���������������ݺ˴Ź�������Ϊ����壬�������Ϊ1 ��2 ��2 ��3��˵���ǻ��������ڱ����Ķ�λ��������ܵĽṹΪ��
������ʽ��C8H8O3������ӵ�ͬ���칹����ʹFe3+��ɫ˵�����з��ǻ����ܷ���ˮ�ⷴӦ˵���������������ݺ˴Ź�������Ϊ����壬�������Ϊ1 ��2 ��2 ��3��˵���ǻ��������ڱ����Ķ�λ��������ܵĽṹΪ�� ��
�� ��
��
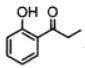
(7)1-�������NaOH��ˮ��Һ���ȷ�Ӧ����1-������ʹ1-����������Ϊ��ȩ����ȩ�������������ᣬ�����뱽����ZnCl2����ʱ����ȡ����Ӧ���� �������ɱ��Ӻ������Ϊ��ʼԭ���Ʊ�
�������ɱ��Ӻ������Ϊ��ʼԭ���Ʊ� �ĺϳ�·��ΪCH3CH2CH2Br
�ĺϳ�·��ΪCH3CH2CH2Br![]() CH3CH2CH2OH
CH3CH2CH2OH![]() CH3CH2CHO
CH3CH2CHO![]() CH3CH2COOH
CH3CH2COOH![]()
 ��
��


 ������ȫ��������ϵ�д�
������ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ϊ��Ҫ�������ϣ��ڻ���������й㷺��Ӧ�á�
��1����̬Asԭ�ӵļ۲���ӵĵ���������ͼ��״Ϊ_____________������ͬ���ڵ�����Ԫ�صĻ�̬ԭ���У���һ����������Ϊ_____________����Ԫ�ط��š���
��2��Na3AsO3�����ڵ����������
��Na+����ɫ��Ӧ�ʻ�ɫ������Ԫ���ܲ�����ɫ��Ӧ����ԭ��Ϊ__________________________��
��Na3AsO3�����������ӵ����幹��Ϊ_____________��д��һ�����以Ϊ�ȵ�����ķ��ӣ�_____________���ѧʽ����
��3�� �����ںϳ�Ni2+�����壬M��Cԭ�ӵ��ӻ���ʽΪ___________��������
�����ںϳ�Ni2+�����壬M��Cԭ�ӵ��ӻ���ʽΪ___________��������![]() ������������Ŀ֮��Ϊ___________��
������������Ŀ֮��Ϊ___________��
��4��Ni��Ca����ͬһ���ڣ��Һ����������ӹ�����ͬ��������Ni���۵�ͷе���Ƚ���Ca�ĸߣ���ԭ��Ϊ___________�����־���Ni�ͷǾ���Ni����ɿ��Ŀ�ѧ����Ϊ___________��
��5��ij�����Ͻ�ľ����ṹ����ͼ��ʾ���谢���ӵ�������ֵΪNA����þ�����ܶ���=___________g��cm-3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g��+ 5O2��g��![]() 4NO��g��+ 6H2O��g��������������ȷ����
4NO��g��+ 6H2O��g��������������ȷ����
A. �ﵽ��ѧƽ��ʱ��4������O2��= 5������NO��
B. ����λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬
C. �ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ��������
D. ��ѧ��Ӧ���ʹ�ϵ�ǣ�2������NH3��= 3������H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��298Kʱ����0.1000mol/L NaOH��Һ�ζ�20.00mLͬŨ�ȵļ�����Һ��������ҺpH��NaOH��Һ����Ĺ�ϵ��ͼ��ʾ(��֪��HCOOH��Һ��Ka=l.0��10-4.0)

�����й�������ȷ����
A. �õζ�����Ӧ��ѡ�������Ϊָʾ��
B. ͼ��a��b�����ĵ���̶ȣ�b>a
C. ������10.00mL NaOH��Һʱ����Һ�У�c(HCOO)>c(H+)>c(Na+)>c(OH)
D. ������20.00mL NaOH��Һʱ����ҺpH>8.0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1 mol��L��1��HA��Һ��c(H��)/c(OH��)��1010�������й�˵������ȷ���ǣ� ��
A. ��Һ��pH��4
B. ������ˮϡ�ͺ�c(HA)/c(A��)��С
C. �������pH����ȵ�HA��Һ�������м�������п�������в����������
D. ��NaA��Һ�д���Ũ�ȹ�ϵ��c(H��)��c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����
A. ��֪�����ۻ���Ϊ6.0kJ��mol��1�������������Ϊ20kJmol��1������ÿĦ��������2mol��������ۻ�����ȫ���ڴ��Ʊ�������������ֻ���ƻ�����15%�����
B. ��֪һ���¶��£�������Һ�����ʵ���Ũ��Ϊc�������Ϊa��Ka=(ca)2/c(1��a)������ˮϡ�ͣ�����CH3COOH![]() CH3COO��+H+�����ƶ���a����Ka����
CH3COO��+H+�����ƶ���a����Ka����
C. ����ı�ȼ����Ϊ��890.3kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+2H2O(l) ��H=��890.3kJ��mol��1
D. 500����30MPa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3kJ�����Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)![]() 2NH3(g) ��H=��38.6kJ��mol��1
2NH3(g) ��H=��38.6kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϣ��ڴ��������£���NH3��Ϊ��ԭ���������е�NOx��ԭ������������ˮ����Ӧ����ʽ�ɱ�ʾΪ��2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)
(1)һ�������£����ݻ�Ϊ2L�������ڽ��и÷�Ӧ��20minʱ�ﵽƽ�⣬����N2 0.4mol����ƽ����Ӧ����v(NO)=___________________���ɴӻ���������ɫ�仯�ж�������Ӧ�Ƿ�ﵽƽ�⣬��������_______________________________________________��
(2)��ҵ��Ҳ�ð�ˮ����SO2β�������յõ�(NH4)2SO4��(NH4)2SO4��Һ��c(NH4+)��c(SO42-)֮��____2:1(ѡ����>������<������=��)�������ӷ���ʽ������ԭ��______________________��
(3)��Cl2��Ƚϣ�ClO2����ˮʱ����ԭ��Cl-���������л��ȴ�����к����ʡ���ҵ�Ͽ����������ƺ�ϡ����Ϊԭ���Ʊ�ClO2����Ӧ���£�NaClO2+HCl��ClO2��+NaCl+_____(û����ƽ)
(4)��ȫ����ʽ����ƽ���������ת�Ʒ������Ŀ_________________________ ��
(5)�÷�Ӧ���������ͻ�ԭ�������ʵ���֮����___________��������0.2molClO2��ת�Ƶ�����Ϊ_____����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ļ������ڹ�ũҵ�����������о�����ҪӦ�á���ش��������⣺
(1)���������г���N2H4��Ϊ����������ȼ����N2H4�백�����ƣ���һ�ּ������壬������ˮ����������N2H4��H2O���õ��뷽��ʽ��ʾN2H4��H2O�Լ��Ե�ԭ���ǣ�____________________________________________��
(2)�ں��������£�1 mol NO2������C������Ӧ2NO2(g)+2C(s)![]() N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��B�����Ũ��ƽ�ⳣ����ϵ��Kc(A) ___________Kc(B)(�<����>����=��)
��A��B��C������NO2��ת������ߵ���___________(�A����B����C��)�㡣
������C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��Kp=___________MPa(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)��֪��������(HNO2)���ʺ��������ƣ�������һ�����ᡣ������������ĵ���ƽ�ⳣ��Ka=5.1��10��4��H2CO3��Ka1=4.2��10��7��Ka2=5.61��10��11���ڳ���������2mol̼���Ƶ���Һ�м���1mol��HNO2������Һ��CO32����HCO3����NO2��������Ũ���ɴ�С��˳����______________________��
(4)��֪�������¼װ�(CH3NH2)�ĵ��볣��ΪKb����pKb=��lgKb=3.4ˮ��Һ����CH3NH2+H2OCH3NH3++OH������������CH3NH2��Һ�μ�ϡ������c(CH3NH2)=c(CH3NH3+)ʱ������ҺpH=_______��
(5)һ��ú̿������������Ԫ����CaSO4���γɹ̶���������������CO�ֻ���CaSO4������ѧ��Ӧ����ص��Ȼ�ѧ����ʽ���£�
��CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) ��H=+210.5kJ�� mol��1
��CaSO4(s)+4CO(g) CaS(s)+ 4CO2(g) ��H=��189.2 kJ�� mol��1
��ӦCaO(s)+3CO(g)+SO2(g) CaS(s)+3CO2(g) ��H=___________ kJ�� mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǹ��ɿ������ʯ����Ҫ�ɷ֣����ʹ輰�仯������й㷺����;�����������գ�
��1��ijЩ�����ξ���ɸѡ���ӵĹ��ܡ�һ�ֹ����ε����Ϊ��M2O��R2O3��2SiO2��nH2O����֪Ԫ��M��R��λ��Ԫ�����ڱ��ĵ�3���ڣ���Ԫ��ԭ�ӵ�������֮��Ϊ24��
��д��Mԭ�Ӻ���������ߵĵ��ӵĵ����Ų�ʽ��___________��
�ڳ����£�������R���ʷ�����Ӧ����_______��ѡ����ţ���
a��CuCl2��Һ b��Fe2O3 c��Ũ���� d��NaOH��Һ e��Na2CO3����
��2�������裨Si3N4���մɲ���Ӳ�ȴ��۵�ߡ��������з�Ӧ�Ƶã�SiO2+C+N2![]() Si3N4+CO
Si3N4+CO
��Si3N4�е�Ԫ�صĻ��ϼ�Ϊ-3�������Si3N4�е�Ԫ�ػ��ϼ�Ϊ���۵�ԭ��__________________��
��C3N4�Ľṹ��Si3N4���ƣ���Ƚ϶����۵�ߵͣ���˵�����ɣ�______________________��
����ƽ������Ӧ�Ļ�ѧ����ʽ�����������ת�Ƶ���Ŀ�ͷ���_______________��
��3��һ���ù�ҵ�裨����������ͭ�Ƚ�����������Ʊ�Si3N4����Ҫ�������£�

�ٽ���ҵ������Ŀ����______________________________��
��������H2��Ϊ���ž��豸�еĿ�������H2�ڸ�����Ҳ�ܻ�ԭ��ҵ���е�ijЩ�������![]() ������______��ѡ������ᡱ�����ᡱ�����ᡱ����������_____________________��
������______��ѡ������ᡱ�����ᡱ�����ᡱ����������_____________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com