
【题目】已知:
药品名称 | 熔点/℃ | 沸点(℃) | 密度g/cm3 | 溶解性 |
丁醇 | ﹣89.5 | 117.7 | 0.8098 | 微溶于水、溶于浓硫酸 |
1﹣溴丁烷 | ﹣112.4 | 101.6 | 1.2760 | 不溶于水和浓硫酸 |
根据题意完成填空:
(一)制备1﹣溴丁烷粗产品:在下图装置的圆底烧瓶中依次加入NaBr,10mL正丁醇,2粒沸石,分批加入1:1的硫酸溶液,摇匀,加热30min.化学方程式:NaBr+H2SO4+CH3CH2CH2CH2OH→CH3CH2CH2CH2Br+NaHSO4+H2O
(1)图1反应装置中加入沸石的目的是 . 配制体积比为1:1的硫酸所用的定量仪器为(选填编号) a.天平 b.量筒 c.容量瓶 d.滴定管
(2)冷凝管的进水方向为 , 这样选择的原因是 .
(3)图2装置中,能代替上图中最后收集装置的是(填序号).
(4)若用浓硫酸进行实验,有机层中会呈现棕黄色,除去其中杂质的正确方法是选填编号). a.蒸馏 b.氢氧化钠溶液洗涤 c.用四氯化碳萃取 d.用亚硫酸钠溶液洗涤
(5)(二)制备精品:将得到的粗1﹣溴丁烷依次用浓硫酸、水、10% 碳酸钠、水洗涤后加入无水氯化钙进行干燥,然后再将1﹣溴丁烷按图3装置蒸馏. 收集产品时,控制的温度应在℃ 左右;
(6)实验制得的1﹣溴丁烷的质量为10.895g,则正丁醇的产率为 .
【答案】
(1)防止暴沸;b
(2)下进上出;能更充分冷凝
(3)ABD
(4)d
(5)101.6
(6)72.7%
【解析】解:(1)反应装置中加入沸石的目的是防止暴沸;用量筒量取相同量的硫酸和水进行混合,故定量仪器为量筒; 所以答案是:防止液体暴沸;bcd;(2)冷凝管是下管进水,上管出水,这样冷却充分,冷凝效果好;
所以答案是:下进上出; 能更充分冷凝;(3)图1中最后的收集装置是防倒吸装置,ABD装置也可用于防倒吸;
所以答案是:ABD;(4)若用浓硫酸进行实验,由于浓硫酸具有强氧化性会使部分溴离子氧化为溴单质;
a.蒸馏也会使部分原料物挥发出来,无法除去其中杂质,故a错误;
b.氢氧化钠溶液洗涤,会使卤代烃发生水解,造成损失,故b错误;
c.由于溴和卤代烃都能溶于四氯化碳,用四氯化碳无法萃取,故c错误;
d.用亚硫酸钠溶液洗涤可和溴发生氧化还原反应,再通过分液操作即可分离,故d正确;
所以答案是:d;(5)根据表中1﹣溴丁烷的沸点可知收集产品时,控制的温度应在101.6℃左右;
所以答案是:101.6;(6)原料正丁醇的质量为lOmL×0.8098g/cm3=8.098g,参加反应的正丁醇的质量为m,
Br+H2SO4+ | CH3CH2CH2CH2OH→ | CH3CH2CH2CH2Br+NaHSO4+H2O |
74 | 137 | |
m | 10.895g |
![]() =
= ![]() 解得:m=5.8849g
解得:m=5.8849g
正丁醇的转化率为 ![]() ×100=72.7%;
×100=72.7%;
所以答案是:72.7%.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、K+、OH﹣、NO3﹣、CO32﹣、SO42﹣ . 为了进一步确认,对该溶液进行实验检测:
①仔细观察,该溶液呈无色、透明、均一状态.
②向100mL溶液中滴入稀硫酸,有23.3g白色沉淀产生,再加稀硝酸,白色沉淀不消失.回答下列问题:由此可知,除了含有Na+、Mg2+、Cl﹣外,该溶液中肯定还含有的离子及其物质的量浓度为 , 肯定没有的离子是 , 可能含有的离子是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在材料应用与发现方面,中华民族有着卓越的贡献。下列说法错误的是
A.黏土烧制成陶器过程中发生了化学变化B.区分真丝产品与纯棉织物可以用灼烧法
C.离子交换法净化水为物理方法D.“玉兔号”月球车帆板太阳能电池的材料是单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中错误的是
A. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
D. 萃取操作时,在选择萃取剂时,要求萃取剂和原溶剂不互溶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于粗盐提纯的下列说法正确的是
A.溶解粗盐时,应多加水尽量使溶液稀些,防止食盐溶解不完全
B.滤去不溶性杂质以后,将滤液移至坩埚内加热浓缩
C.当蒸发到有大量晶体析出,剩有少量溶液时,停止加热,利用余热将液体蒸干
D.当制得的晶体转移到新制过滤器中用大量水进行洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是
选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | NO |
C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
D | NaOH | HCl | CaF2 | Na2O2 | SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.实验室需要0.1molL﹣1NaOH溶液500mL.根据溶液的配制情况回答下列问题.
(1)在如图所示仪器中,配制上述溶液肯定不需要的是(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 . 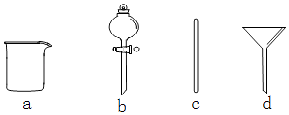
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次) .
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1cm~2cm处
(3)实验两次用到玻璃棒,其作用分别是:先用于、后用于 .
(4)关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水.这些叙述中正确的是
A.①②③④
B.②③
C.①②④
D.②③④
(5)根据计算用托盘天平称取的质量为g.
(6)Ⅱ.若配制1mol/L的稀硫酸溶液500mL
则需要质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为mL(计算结果保留一位小数).如果实验室有10mL、25mL、50mL量筒,应选用mL规格的量筒最好.
(7)下面操作造成所配稀硫酸溶液浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各图的说法,正确的是( ) 
A.①中阳极处能产生使湿润淀粉KI试纸变蓝的气体
B.②中待镀铁制品应与电源正极相连
C.③中钢闸门应与外接电源的正极相连,称为牺牲阳极的阴极保护法
D.④中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com