
【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.已知CO(g)+H2O(g)H2(g)+CO2(g)的平衡常数随温度的变化如表:下列叙述正确的是( )
温度/℃ | 400 | 500 | 830 | 1 000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
A.该反应的正反应是吸热反应
B.该反应达到平衡后,保持容器体积不变升高温度,正反应速率不变,容器内混合气体的压强不变
C.830℃时,在恒容反应器中按物质的量比n(CO):n(H2O):n(H2):n(CO2)=2:4:6:1投入反应混合物发生上述反应,初始时刻υ正<υ逆
D.830℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是60%
【答案】D
【解析】解:A.由表格数据可知,温度越高,K越小,则升高温度,平衡逆向移动,则正反应为放热反应,故A错误; B.升高温度,增大反应速率,由选项A可知,平衡逆向移动,故B错误;
C.按物质的量比n(CO):n(H2O):n(H2):n(CO2)=2:4:6:1,Qc= ![]() =0.75<K=1.0,平衡正向移动,则初始时刻υ正>υ逆 , 故C错误;
=0.75<K=1.0,平衡正向移动,则初始时刻υ正>υ逆 , 故C错误;
D.830℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,则
CO(g)+ | H2O(g) | H2(g)+ | CO2(g) | |
起始 | 2 | 3 | 0 | 0 |
转化 | x | x | x | x |
平衡 | 2-x | 3-x | x | x |
![]() =1.0,解得x=1.2,则CO的转化率是
=1.0,解得x=1.2,则CO的转化率是 ![]() ×100%=60%,故D正确;
×100%=60%,故D正确;
故选D.
【考点精析】通过灵活运用化学平衡的计算,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%即可以解答此题.


 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种黄色难溶于水的固体,受热易分解,是生产锂电池、涂料、着色剂以及感光材料的原材料。
Ⅰ、草酸亚铁晶体的制备:

(1)步骤①硫酸亚铁铵晶体加稀硫酸溶解的原因是___________________。
(2)步骤2倾析的作用是使固液分离,具体操作是静置后,将沉淀上部的溶液倾入另一容器,从而获得固体。倾析法与普通的过滤相比,明显的优点是____________________。
(3)硫酸亚铁铵俗称莫尔盐,在空气中比一般的亚铁盐稳定,较难被氧化,其水溶液的性质与组成它的简单盐的混合溶液没有区别。设计简单实验证明硫酸亚铁铵比硫酸亚铁更稳定______________________。
Ⅱ、测定草酸亚铁的纯度:
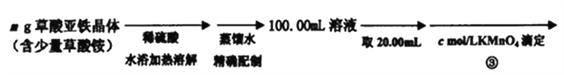
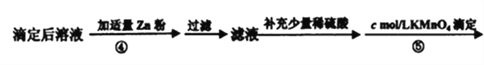
(4)在步骤③的溶液中除发生反应MnO4-+8H++5Fe2+=5Fe3++Mn2++4H2O 外,还有另一氧化还原反应,写出该反应的离子方程式__________________ ;用KmnO4标准溶液滴定至终点的现象是_____________________。
(5)步骤④加入适量锌粉的目的是________________。
(6)相同条件下,重复滴定三次,步骤③平均消耗KmnO4标准溶液V1mL,步骤⑤平均消耗V2mL,则mg固体样品的纯度计算式为______________。(用相关字母表示,不必化简)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法,即保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体,Fe(OH)3胶体具有吸附作用,可吸附水中的污物而使其沉淀下来,起到净水的作用,其原理如图所示。下列说法正确的是( )
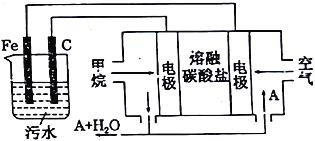
A. 石墨电极上发生氧化反应
B. 通空气的电极反应式为O2+4e-=2O2-
C. 通甲烷的电极反应式:CH4+4CO32--8e-=5CO2+2H2O
D. 甲烷燃料电池中CO32-向空气一极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表,下列说法错误的是( )
实验编号 | HA物质的量浓度(molL-1) | NaOH物质的量浓度(molL-1) | 混合溶液的pH |
甲 | 0.2 | 0.2 | a |
乙 | c1 | 0.2 | 7 |
丙 | 0.2 | 0.1 | 7 |
丁 | 0.1 | 0.1 | 9 |
A. 若a=7,HA为强酸;若a>7,HA为弱酸
B. 单从乙组情况分析,c1不一定等于0.2molL-1,混合溶液中离子浓度c(A-)=c(Na+)
C. 从丙组实验结果分析,HA是弱酸,混合溶液中离子浓度c(Na+)=c(A-)>c(OH-)=c(H+)
D. 丁组实验所得混合溶液中由水电离出的c(OH-)=1×10-5 molL-1,c(OH-)-c(HA)= 1×10-10molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机化合物X中各元素的质量分数分别为C﹣﹣﹣60%,H﹣﹣﹣13.3%,O﹣﹣﹣26.7%. 请填空:
(1)有机物X的实验式为 . 若0.1molX在足量氧气中充分燃烧需消耗氧气10.08L(标准状况),则X的分子式为 .
(2)实验表明:X能与金属钠反应产生H2 . X分子的核磁共振氢谱中有4个吸收峰,且面积之比为3:2:2:1,则X分子中含有的官能团的名称为 , X的结构简式为 .
(3)X有两种同分异构体Y和Z,其中Y能与金属钠反应产生H2 , 而Z不能.则Y、Z的结构简式分别为、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L恒容密闭容器中,发生反应 2NO(g)+O2(g)2NO2(g). 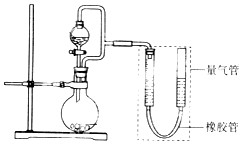
(1)某温度时,按物质的量比2:1充入NO和O2开始反应,n(NO)随时间变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
0~4s内以O2浓度变化表示的反应速率1~5s内以NO浓度变化表示的反应速率(选填“小于”、“大于”、“等于”).
(2)该反应的平衡常数表达式为K=.能说明该反应已达到平衡状态的是 . A.气体颜色保持不变 B.气体平均相对分子质量保持不变
C.υ逆(NO)=2υ正(O2)D.气体密度保持不变
(3)已知:K300℃>K400℃.下列措施能使该反应的反应速率增大且平衡向正反应方向移动的是 .
A.升高温度
B.充入Ar使压强增大
C.充入O2使压强增大
D.选择高效催化剂
(4)将amolNO和bmolO2发生反应,要使反应物和生成物物质的量之比为1:2,则a/b的取值范围是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(16分)雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

(1)装置Ⅰ中的主要离子方程式为 。
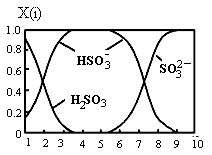 (2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
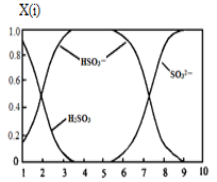
①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下反应的离子方程 式 , 。
(4)装置Ⅲ还可以使Ce4+再生,其原理如图所示。①生成Ce4+从电解槽的 (填字母序号)口流出。②写出阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g·L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据外媒报道,WirthResearch公司公布了其用轻型氢燃料电池作为主要能源的无人空中系统(UAS)的设计,该轻型氢燃料电池比普通理离子电池具有更高的能量密度(能量密度是指单位体积或重量可以存储的能量多少)。用吸附了H2的碳纳米管等材料制作的二次电池的原理如下图所示。该电池的总反应为H2+2NiO(OH) ![]() 2Ni(OH)2,已知:6NiO(OH)+NH3+H2O+OH-=6Ni(OH)2+NO2-。下列说法不正确的是
2Ni(OH)2,已知:6NiO(OH)+NH3+H2O+OH-=6Ni(OH)2+NO2-。下列说法不正确的是
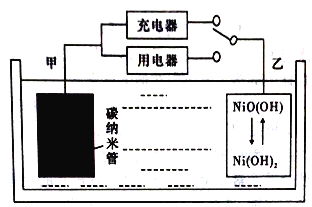
A. 碳纳米管吸附H2的密度越大,电池的能量密度越高
B. 电池可以用KOH溶液、氨水等作为电解质溶液
C. 放电时.乙电极反应为NiO(OH)+H2O+e-=Ni(OH)2+OH-
D. 充电时,电池的碳电极与直流电源的负极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com