
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/(mol?L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
| A、500 s内N2O5分解速率为2.96×10-3mol?L-1?s-1 | ||
| B、T1温度下的平衡常数K1=125(mol?L-1)3,平衡时N2O5的转化率为50% | ||
| C、T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 | ||
D、达平衡后其他条件不变,将容器的体积压缩到原来的
|
| 1 |
| 2 |
| 1.48mol/L |
| 500s |
| [O2]?[NO2]4 |
| [N2O5]2 |
| 5-2.5 |
| 5 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
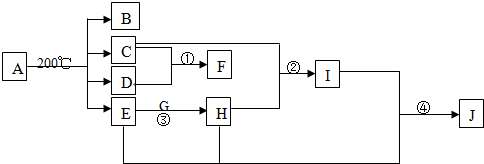
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素或原子 | 元素的性质或原子的结构的描述 |
| Ⅰ | 原子核内只有一个质子 |
| Ⅱ | 最外层电子数是次外层的2倍 |
| Ⅲ | 地壳中含量最多的元素 |
| Ⅳ | 原子失去一个电子后为单核10电子的阳离子 |
| Ⅴ | 原子得到一个电子后,与氩原子的电子层结构相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②③ | C、③⑤ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
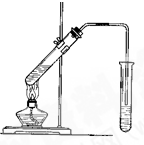 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯.查看答案和解析>>
科目:高中化学 来源: 题型:
| 应量取盐酸体积/mL | 应选用容量瓶的规格/mL | 除容量瓶外还需要的其它仪器 |
查看答案和解析>>
科目:高中化学 来源: 题型:
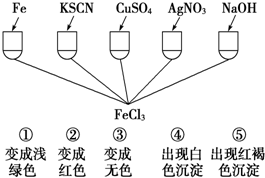 阅读下列材料后,回答相应问题.
阅读下列材料后,回答相应问题.| A |
| B |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用水可区分苯和溴苯 |
| B、蛋白质和油脂都属于高分子化合物,一定条件下都能水解 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①③ | C、②③ | D、②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com