

 ,所以B是
,所以B是 ,A分子中有三个甲基,所以A的结构简式为:
,A分子中有三个甲基,所以A的结构简式为: ,
, 反应生成
反应生成 ,
, 和银氨溶液反应生成D,D的结构简式为:
和银氨溶液反应生成D,D的结构简式为: ,酸性条件下,D反应生成E
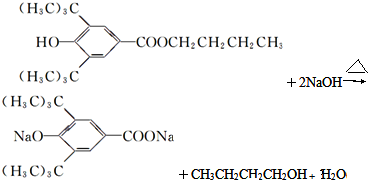
,酸性条件下,D反应生成E ,A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基,F的结构简式为:CH3CH2CH2CH2OH,E和F发生酯化反应生成P,P的结构简式为:
,A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基,F的结构简式为:CH3CH2CH2CH2OH,E和F发生酯化反应生成P,P的结构简式为: ,据此答题.
,据此答题. ,所以B是
,所以B是 ,A分子中有三个甲基,所以A的结构简式为:
,A分子中有三个甲基,所以A的结构简式为: ,
, 反应生成
反应生成 ,
, 和银氨溶液反应生成D,D的结构简式为:
和银氨溶液反应生成D,D的结构简式为: ,酸性条件下,D反应生成E
,酸性条件下,D反应生成E ,A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基,F的结构简式为:CH3CH2CH2CH2OH,E和F发生酯化反应生成P
,A和F互为同分异构体,A分子中有三个甲基,F分子中只有一个甲基,F的结构简式为:CH3CH2CH2CH2OH,E和F发生酯化反应生成P .
. ,
, .
.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
| A、标准状况下,22.4L CCl4含有C-Cl键的数目为4NA |
| B、取50mL 14.0mol/L浓硝酸与足量铜片反应,生成气体分子的数目为0.35NA |
| C、反应NH4N3?2N2↑+2H2↑,标准状况下每生成22.4L N2,转移电子的数目为2NA |
| D、电解精炼铜时,若转移的电子数为NA个,则阳极质量减少32g |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、原子半径:W>Z |
| B、最高价氧化物的水化物的酸性:R>W |
| C、气态氢化物的稳定性:X>W |
| D、单质与水(或酸)反应的剧烈程度:Y>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 化学式 | 20℃ | 60℃ | 100℃ |
| Na2SO4 | 19.5 | 45.3 | 42.5 |
| Na2Cr2O7 | 183 | 269 | 415 |
| Na2CrO4 | 84 | 115 | 126 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com