
【题目】实验室以苯甲醛为原料制备间溴苯甲醛(实验装置见下图)。其实验步骤为:
步骤1:将三颈瓶中的一定配比的无水AlCl3、1,2-二氯乙烷和苯甲醛充分混合后,升温至60℃,缓慢滴加经浓硫酸干燥过的液溴,保温反应一段时间,冷却。
步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%NaHCO3溶液洗涤。
步骤3:经洗涤的有机相加入适量无水MgSO4固体,放置一段时间后过滤。
步骤4:减压蒸馏有机相,收集相应馏分。

下列说法错误的是
A. 甲同学认为步骤1中使用1,2-二氯乙烷的目的是做催化剂,加快反应速率
B. 乙同学认为可在该实验装置的冷凝管后加接一只装有无水MgSO4的干燥管,实验效果可能会更好
C. 丙同学认为步骤2中有机相使用10%NaHCO3溶液洗涤可除去大部分未反应完的Br2
D. 丁同学认为步骤4中减压蒸馏有机相是因为间溴苯甲醛高温下容易氧化或分解
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如下所示,该“84消毒液”通常稀释100倍(体积之比)后使用.请回答下列问题: 84消毒液
[有效成分]NaClO
[规格]1000mL
[质量分数]25%
[密度]1.19gcm﹣3
(1)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=molL﹣1 .
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制80mL含NaClO质量分数为25%的消毒液,需要称量NaClO固体的质量为g;所用到的玻璃仪器有玻璃棒、烧杯、量筒和 .
(3)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84gcm﹣3)的浓硫酸配制2000mL2.3molL﹣1的稀硫酸用于增强“84消毒液”的消毒能力. ①所配制的稀硫酸中,H+的物质的量浓度为molL﹣1 .
②需用浓硫酸的体积为mL.
(4)配置一定物质的量浓度的稀硫酸时,下列操作会使所配溶液物质的量浓度偏低的是 .
A.定容时俯视容量瓶刻度线
B.用量筒量取浓硫酸时俯视刻度线
C.容量瓶用蒸馏水洗涤干净后没有干燥就移入所配置溶液
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线.
E.加水时超过刻度线,用胶头滴管吸出.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如下图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法不正确的是( )

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:X>W>Z
C. 最简单气态氢化物的热稳定性:Y>X>W>Z
D. 元素X、Z、W的最高化合价分别与其主族序数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,水作为氧化剂的是( )
A. NaOH+HCl= NaCl+H2O B. CaO+H2O = Ca(OH)2
C. 2Na+2H2O= 2NaOH+H2↑ D. Cl2+H2O = HCl + HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确表示下列反应的离子方程式的是( )
A. 氢氧化钠溶液与盐酸反应:H++OH-=H2O B. 铁溶于氯化铁溶液:Fe3++Fe=2Fe2+
C. 碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O D. 钠与水反应:Na+2H2O=Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2作为资源再利用是重要的研究课题,工业上用CO2产生燃料甲醇的化学方程式:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)。回答下列问题:
CH3OH(g)+H2O(g)。回答下列问题:
(1)由CO2制备甲醇过程涉及反应如下:
反应Ⅰ:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1
反应Ⅱ:CO2(g)+H2(g)![]() CO(g)+H2O(g) △H2
CO(g)+H2O(g) △H2
反应Ⅲ:CO(g)+2H2(g)![]() CH3OH(g) △H3
CH3OH(g) △H3
已知反应Ⅰ、反应Ⅱ、反应Ⅲ的化学平衡常数分别为K1、K2、K3,则K1_______(用K2、K3表示)
(2)一定条件下,在3L恒容密闭容器中充入一定量的H2和CO2,研究反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H1,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线如下图所示。
CH3OH(g)+H2O(g) △H1,实验测得反应物在不同起始投入量下,反应体系中CO2的平衡转化率与温度的关系曲线如下图所示。
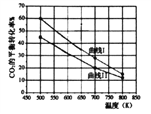
①H2和CO2的起始的投入量以A和B两种方式投入:
A:n(H2)=3mol,n(CO2)=1.5mol,
B:n(H2)=3mol,n(CO2)=2mol
曲线Ⅱ代表______(填“A”或“B”)投入方式反应的△H1________0(填“﹥”或“<”)
②在温度为500K的条件下,充入3molH2和1.5molCO2,该反应5min时达到平衡,此温度下的平衡常数为_______(mol·L-1)-2
③500K时,若在此容器中开始充入0.3molH2和0.9molCO2、0.6molCH3OH、0.6molH2O,则反应向______方向进行(“正反应”或“逆反应”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学键的说法正确的是( )
A. 离子化合物中一定存在离子键,可能存在共价键 B. 非极性键只存在于双原子单质分子中
C. 由金属元素和非金属元素形成的化学键一定是离子键 D. NH4Cl是一种共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在课外活动实验中,某学生用蔗糖、碳酸氢铵、生石灰和硫酸4种药品从AgNO3(内含少量Fe3+和Al3+)废液中提取银。

(1)写出下列物质的名称①______________,⑤________________,⑥______________。
(2)写出下列物质的化学式:②______________;③________________;④________________。
(3)写出下列反应的化学方程式及反应类型:
⑤→⑥:____________________________,反应类型________。
③+⑥→Ag:____________________,反应类型________。
(4)在③+⑥的反应中,若未出现Ag,其原因可能是______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com