
| A. | 按照有机物系统命名法,化合物 的名称为:3,3-二乙基戊烷 的名称为:3,3-二乙基戊烷 | |
| B. | 甲醇、乙二醇、丙三醇都为饱和醇,熔沸点依次递增 | |
| C. | 甘氨酸H2N-CH2COOH、丙氨酸CH3CH(NH2)COOH、谷氨酸HOOCCH2CH2CH(NH2)COOH一定条件下形成链状三肽的结构最多有33种 | |
| D. | 分子式为C5H10O2的所有酯类的同分异构体共有9种 |
分析 A、 为烷烃,最长碳链为5,据此命名即可;
为烷烃,最长碳链为5,据此命名即可;
B、甲醇、乙二醇、丙三醇相对分子质量逐渐增大,氢键数目增多;
C、氨基酸为三种,但是谷氨酸有2个羧基,形成的肽键不同;
D、分子式为C5H10O2的酯为饱和一元酯,形成酯的羧酸与醇的碳原子总数为5,讨论羧酸与醇含有的碳原子,进行书写判断.
解答 解:A、 为烷烃,最长碳链为5,在3号碳上含有2个乙基,正确命名为:3,3-二乙基戊烷,故A正确;
为烷烃,最长碳链为5,在3号碳上含有2个乙基,正确命名为:3,3-二乙基戊烷,故A正确;
B.甲醇、乙二醇、丙三醇相对分子质量逐渐增大,氢键数目增多,则甲醇、乙二醇、丙三醇的沸点依次升高,故B正确;
C、氨基酸为三种,但是谷氨酸有2个羧基,形成的肽键不同,故形成的肽键多余27种,C错误;
D、若为甲酸和丁醇酯化,丁醇有4种,形成的酯有四个:
HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3;
若为乙酸和丙醇酯化,丙醇有2种,形成的酯有2个:CH3COOCH2CH2CH3、CH3COOCH(CH3)2;
若为丙酸和乙醇酯化,丙酸有1种,形成的酯有1个:CH3CH2COOCH2CH3;
若为丁酸和甲醇酯化,丁酸有2中,形成的酯有2个:CH3CH2CH2COOCH3、(CH3)2CHCOOCH3.
故有9种,故D正确;故选C.
点评 本题考查同分异构体的书写与判断,难度中等,关键是形成酯的羧酸与醇的同分异构体的判断.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l),△H2 | |
| B. | S(g)+O2(g)=SO2(g),△H1; S(s)+O2(g)=SO2(g),△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g),△H1; C(s)+O2(g)=CO2(g),△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氨水与亚硫酸溶液混合:NH3•H2O+H+═NH4++H2O | |
| B. | 将少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=2HClO+CaSO3↓ | |
| C. | 足量铁屑溶于稀硫酸:2Fe+6H+=2Fe3++3H2↑ | |
| D. | 将Cl2通入FeSO4溶液中:Cl2+2Fe2+═2Fe3++2 Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 图为一个原电池,完成下列问题:
图为一个原电池,完成下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
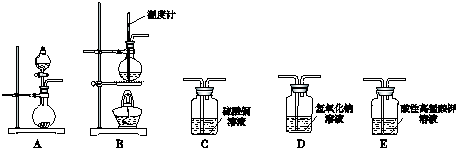
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | B→D→E | CH3-CH2-OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O |
| (2) | 乙炔 | A→C→E | CaC2+2H2O→CH≡CH↑+Ca(OH)2 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
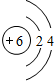 .
. ;写出C2B2的电子式
;写出C2B2的电子式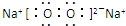 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com