
(5分)卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的___________区;
(2)氟的电子排布图为___________________;
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是______________;

(4)已知碘酸HIO3和高碘酸H5IO6的结构分别如图I、图II所示:

请比较二者酸性强弱:HIO3_________H5IO6(填“>”“<”或“=”);
(5)下图为碘晶体晶胞结构。下列说法中正确的是_________.

A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以8配位数交替配位形成层状结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(1)p (2)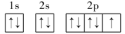 (3)碘 (4)> (5)D
(3)碘 (4)> (5)D
【解析】
试题分析:(1)卤族元素位于元素周期表的第17纵行,属于p区;(2)9号元素氟的电子排布图为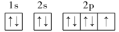 ;(3)元素的原子的第一电离能越小,则原子越容易失去电子,形成单核阳离子的可能性就越大,所以根据元素的第一电离能的大小数据可知:碘元素的第一电离能最小,所以碘元素最有可能生成较稳定的单核阳离子;(4)碘酸HIO3是中强酸,而高碘酸H5IO6则是五元弱酸,所以酸性:HIO3>H5IO6;(5)A.碘分子的排列有2种不同的取向,每个碘分子的配位数是(3×8)÷2=12,错误;B.用均摊法可知平均每个晶胞中有的碘分子个数是:(8×1/8)+6×1/2=4个,所以含有8个碘原子,错误;C.碘晶体为分子晶体,不是原子晶体,错误;D.由于碘分子是单质分子,所以在碘晶体中存在的相互作用有非极性键和范德华力,正确。
;(3)元素的原子的第一电离能越小,则原子越容易失去电子,形成单核阳离子的可能性就越大,所以根据元素的第一电离能的大小数据可知:碘元素的第一电离能最小,所以碘元素最有可能生成较稳定的单核阳离子;(4)碘酸HIO3是中强酸,而高碘酸H5IO6则是五元弱酸,所以酸性:HIO3>H5IO6;(5)A.碘分子的排列有2种不同的取向,每个碘分子的配位数是(3×8)÷2=12,错误;B.用均摊法可知平均每个晶胞中有的碘分子个数是:(8×1/8)+6×1/2=4个,所以含有8个碘原子,错误;C.碘晶体为分子晶体,不是原子晶体,错误;D.由于碘分子是单质分子,所以在碘晶体中存在的相互作用有非极性键和范德华力,正确。
考点:考查卤素在周期表中的位置、原子的电子排布图、物质酸性强弱的比较、均摊法在晶体中的应用。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源:2015届辽宁省高三上学期10月月考试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.常温常压下,由x g NO2和y g N2O4组成的混合气体中原子总数为3NA,,则x + y =46
B.1 mol氯气参加氧化还原反应,一定得到NA 或2NA个电子
C.1升0.1 mol·L-1 NaBr溶液中,HBr和Br-总和为0.1NA个
D.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省大连市高三10月月考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.光导纤维的主要成分是硅
B.NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体
C.Na2O2与水反应,红热的Fe与水蒸气反应均能反应生成碱
D.Na和Cs属于第IA族元素,Cs失去电子能力比Na强
查看答案和解析>>
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的数值。下列说法正确的是
A.1mol甲苯含有6NA个C-H键
B.18gH2O含有10NA个质子
C.标准状况下,22.4L氨水含有NA个NH3分子
D.56g铁片投入足量浓硫酸中生成NA个SO2分子
查看答案和解析>>
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
某物质熔融状态可导电,固态可导电,将其投入水中溶液也可导电,推测该物质可能是
A.金属 B.非金属 C、可溶性碱 D、可溶性盐
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:填空题
(9分)砷(As)广泛分布与自然界,砷与氮同主族,比氮多两个电子层。
(1)砷位于元素周期表中_____周期________族,其气态氢化物的稳定性比NH3_______(填“强”或“弱”);
(2)砷的常见酸性氧化物有As2O3和As2O5,请根据图中信息写出As2O3分解为As2O5的热化学方程式:________________________;

(3)已知:将酸滴入砷酸盐与KI混合的溶液中发生反应:AsO43-+2I―+2H+=AsO33-+I2+H2O.某研究性学习小组同学欲利用该反应原理,设计实验装置探究原电池原理,请你配合他们绘制原电池装置图,并回答下列问题:
若以石墨为电极,正极上发生的反应为______________.该电池工作时,当外电路中转移5mol电子时,则有_________molI2生成.
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
在密闭容器中A与B反应生成C,其反应速率分别为 、
、 、
、 表示。已知: 2
表示。已知: 2 =3
=3 ,3
,3 =2
=2 ,则此反应可表示为( )
,则此反应可表示为( )
A.2A+3B=2C B.A+3B=2C C.3A+B=2C D.A+B=C
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
为减缓足量的镁和一定量盐酸的反应速率,又不影响氢气的总量,可采用的措施是( )
A.加固体NaOH B.加固体硝酸钠 C.加固体醋酸钾 D.加硫酸
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在溶液中一定能大量共存的是
A.pH=12的溶液:K+、Na+、CH3COO—、CO23—
B.0.1 mol/L的NaNO3溶液:H+、Fe2+、Cl—、SO42—
C.与铝反应产生大量氢气的溶液:Mg2+、K+、HCO3—、NO3—
D.由水电离产生的c(H+)=10-13mol/L的溶液:NH4+、Ca2+、SO32—、Cl—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com