

| n(H2) |
| n(CH3OH) |
| ������Ũ��ϵ���ݴη� |
| ��Ӧ��Ũ��ϵ���ݴη� |
| ������Ũ��ϵ���ݴη� |
| ��Ӧ��Ũ��ϵ���ݴη� |
| [CO2]8 |
| [O2]7 |
| [CO2]8 |
| [O2]7 |
| ||
| tA |
| nA |
| 2tA |
| n(H2) |
| n(CH3OH) |
| 1-a+3-3a+a+a |
| 1+3 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


 ��5�����й��ڻ�����I��II��V��VI��˵����ȷ����
��5�����й��ڻ�����I��II��V��VI��˵����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
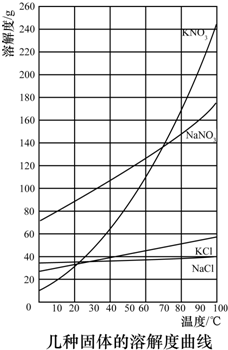
| 2 |
| 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
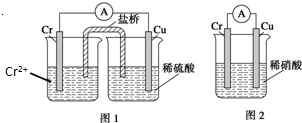 �������������ڹ�ҵ�϶�����Ҫ����;����֪��������ϡ���ᷴӦ�����������������Ǹ���CrSO4����
�������������ڹ�ҵ�϶�����Ҫ����;����֪��������ϡ���ᷴӦ�����������������Ǹ���CrSO4�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1 mol?L-1 NaHCO3��Һ�У�c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� |
| B����0.1 mol?L-1 Na2CO3��Һ�У�c��OH-��-c��H+��=c��HCO3-��+2c��H2CO3�� |
| C����0.2 mol?L-1 NaHCO3��Һ�м�������0.1 mol?L-1 NaOH��Һ��c��CO32-����c��HCO3-����c��OH-����c��H+�� |
| D��CH3COONa��CH3COOH�����Һһ�����ڣ�c��Na+��=c��CH3COO-��=c��CH3COOH����c��H+��=c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
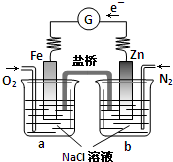
| A�����ձ�a�м�������K3[Fe��CN��6]��Һ������ɫ�������� |
| B���ձ�a�з�����ӦO2+4H++4e-=2H2O����ҺpH���� |
| C�����Ӵ�Zn������������Fe���������Żص�Zn�� |
| D���ձ�b�з�����ӦΪZn-2e-=Zn2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
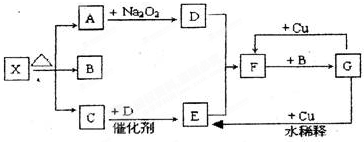
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com