
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的( )
A.加入Al能放出H2的溶液中:ClO﹣、HCO ![]() 、SO
、SO ![]() 、NH
、NH ![]()
B.pH=2的溶液中:Fe2+、Na+、Mg2+、NO ![]()
C.能使KSCN溶液变红的溶液中:Na+、I﹣、NO ![]() 、HCO
、HCO ![]()
D.由水电离出的c(OH﹣)=1.0×10﹣13mol?L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣
科目:高中化学 来源: 题型:
【题目】氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 ![]() 和
和 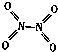 .实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
.实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
(1)写出N2O4转化NO2为的热化学方程式 .
(2)对反应N2O4(g)2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.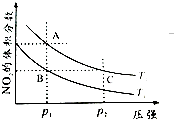
①A、C两点的反应速率v(A)v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是 .
④A点气体的颜色比C点(填“深”、“浅”或“相同”),原因是 .
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
①在上述条件下,从反应开始直至20s时,v(NO2)=molL﹣1s﹣1 .
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用下面实验装置设计实验制备SO2,并进行相关探究活动。
(已知:酸性强弱为H2SO3>H2CO3>HClO)
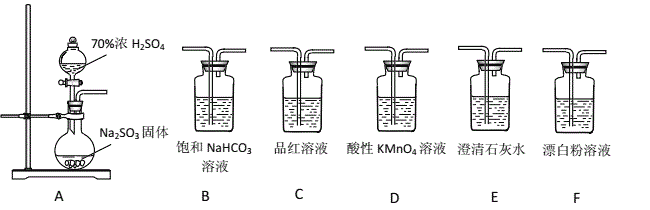
(1)装置A中反应的化学方程式为_________________________________________。
(2)甲同学从上面装置中选择合适的装置验证亚硫酸与碳酸的酸性强弱,其中用到了C、D装置。
①C装置的作用是___________________________。
②通过___________________________________________________(填实验现象)即可证明亚硫酸酸性强于碳酸。
(3)乙同学认为利用上述装置也可以证明亚硫酸的酸性强于次氯酸,请写出正确的装置连接顺序:A→( )→( ) → C → F 。____________
(4)丙同学将A中产生的足量的SO2通入下图装置G中,G中有白色沉淀生成。该沉淀的化学式为_________。
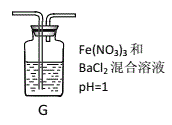
I.推测产生沉淀的原因可能是(不考虑空气的影响)
原因一:SO2在酸性条件下被NO3-氧化;
原因二:SO2被Fe3+氧化;
原因三:_____________________________________________。
II.如果丙同学认为是因为“原因二”产生了白色沉淀。
①请你写出SO2被Fe3+氧化的离子方程式:_________________________________
②假如Fe3+恰好完全反应,请你设计实验证明其还原产物,并简要叙述实验过程、现象及结论。
___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:M+N﹣→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到30℃时,完成反应的10%需要的时间为( )
A.9 min
B.27 min
C.13.5 min
D.3 min
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某温度下,将H2和I2各1mol的气态混合物充入1L的密闭容器中,发生反应:H2(g)+I2(g)2HI(g)△H<0;5min后达到平衡状态,测得c(H2)=0.9molL﹣1 , 则下列结论中,不能成立的是( )
A.平衡时H2、I2的转化率相等
B.从反应开始至平衡的过程中,v(HI)=0.04molL﹣1min﹣1
C.其他条件不变再向容器中充入少量H2 , I2的转化率提高
D.若将容器温度提高,其平衡常数K一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( ) 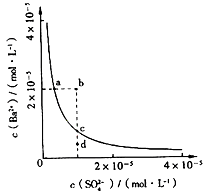
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中,各组离子可能大量共存的是( )
A.由水电离出的c(H+)=10﹣13 mol?L﹣1的溶液中:Al3+、K+、NO ![]() 、SO
、SO ![]()
B.强酸性溶液中:Cu2+、ClO﹣、Cl﹣、Ba2+
C.0.1 mol?L﹣1 的NaHCO3溶液中:K+、Al3+、Fe3+、NO ![]()
D.pH=7的溶液中:K+、Fe3+、Cl﹣、NO ![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com