
【题目】氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是 ![]() 和
和 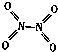 .实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
.实验测得N﹣N键的键能为167kJmol﹣1 , NO2中氮氧键的键能为 466kJmol﹣1 , N2O4中氮氧键的键能为438.5kJmol﹣1 .
(1)写出N2O4转化NO2为的热化学方程式 .
(2)对反应N2O4(g)2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.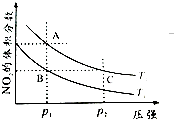
①A、C两点的反应速率v(A)v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是 .
④A点气体的颜色比C点(填“深”、“浅”或“相同”),原因是 .
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
①在上述条件下,从反应开始直至20s时,v(NO2)=molL﹣1s﹣1 .
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是molL﹣1 .
【答案】
(1)N2O4(g)?2NO2(g)△H=+57 kJ?mol﹣1
(2)<;=;加热;浅;A点到C点时压强增大,即体积减小,平衡逆移,NO2的体积分数减小,但平衡时C点c(NO2)比A点大
(3)0.0025;0.10
【解析】解:(1)根据化学反应的反应热=反应物的总键能﹣生成物的总键能,所以N2O4(g)2NO2(g)的反应热△H=438.5kJmol﹣1×4+167kJmol﹣1﹣466 kJmol﹣1×4=+57 Kj,mol﹣1 , 所以N2O4转化为NO2的热化学方程式为:N2O4(g)2NO2(g)△H=+57kJmol﹣1 , 故答案为:N2O4(g)2NO2(g)△H=+57kJmol﹣1;(2)①C点压强大于A点,所以C点的反应速率快,即:v(A)<v(C),故答案为:<;②B、C两点的二氧化氮体积分数相同,为等效平衡,则气体的平均相对分子质量相同,即:M(B=M(C),故答案为:=;③B的二氧化氮体积分数小于A点,该反应是吸热反应,温度升高,平衡正向移动,二氧化氮的体积分数增大,所以T2>T1 , A、B压强相同,则由状态B到状态A,可以用加热的方法,故答案为:加热;④A、C点温度相同,C的压强增大,体积缩小,气体颜色加深,尽管平衡逆向移动,但最终气体的颜色比原平衡时深,则A浅、C深,即:A点气体的颜色比C点浅,故答案为:浅;A点到C点时压强增大,即体积减小,平衡逆移,NO2的体积分数减小,但平衡时C点c(NO2)比A点大;(3)①在上述条件下,该反应为2NO2(g)N2O4(g),从反应开始直至20 s时,N2O4(g)的物质的量增加0.05mol,则二氧化氮的物质的量减少0.1mol,浓度减少 ![]() =0.05mol/L,二氧化氮的平均反应速率为:
=0.05mol/L,二氧化氮的平均反应速率为: ![]() =0.0025mol(Ls)﹣1 , 故答案为:0.0025;②若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,即为等效平衡状态,则将0.4mol的二氧化氮完全转化为四氧化二氮的物质的量是0.2mol,则四氧化二氮的起始浓度为:
=0.0025mol(Ls)﹣1 , 故答案为:0.0025;②若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,即为等效平衡状态,则将0.4mol的二氧化氮完全转化为四氧化二氮的物质的量是0.2mol,则四氧化二氮的起始浓度为: ![]() =0.10mol/L, 故答案为:0.10.
=0.10mol/L, 故答案为:0.10.
(1)化学反应的反应热=反应物的总键能﹣生成物的总键能,注明物质的聚集状态与放热反应书写热化学方程式;(2)①压强越高,反应速率越快;
②B、C两点的二氧化氮体积分数相同,为等效平衡;
③B的二氧化氮体积分数小于A点,该反应是吸热反应,温度升高,平衡正向移动,二氧化氮的体积分数增大,所以T2>T1;
④A、C点温度相同,C的压强增大,体积缩小,气体颜色加深;(3)①从反应开始直至20 s时,N2O4(g)的物质的量增加0.05mol,则二氧化氮的物质的量减少0.1mol,浓度减少 ![]() =0.05mol/L,再根据v=
=0.05mol/L,再根据v= ![]() 计算v(NO2);
计算v(NO2);
②若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,即为等效平衡状态,则将0.4mol的二氧化氮完全转化为四氧化二氮的物质的量是0.2mol.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃时,水的电离达到平衡:H2OH++OH﹣△H>0,下列叙述正确的是( )
A.向水中加入氨水,平衡逆向移动,c(OH﹣)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置图的叙述中,正确的是( ) 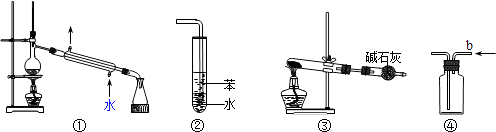
A.装置①可用于分离苯和溴苯的混合物
B.装置②可用于吸收HCl或NH3气体
C.装置③可用于分解NH4Cl制备NH3
D.装置④b口进气可收集CO2或NO气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关安全措施不恰当的是( )
A. 实验室使用电器时,不能用湿手接触电器
B. 实验结束后,应关好水龙头、排气扇及切断电源
C. 未经老师允许,可以带食物进实验室,可以边做实验边吃东西
D. 酒精灯里的酒精不准带出实验室
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用废铅蓄电池的铅泥(PbO、Pb及PbSO4等)可制备精细无机化工产品﹣3PbOPbSO4H2O (三盐),主要制备流程如下:
(1)步骤①PbSO4转化为难溶PbCO3的离子方程式为 .
(2)滤液1和滤液3经脱色、蒸发、结晶可得到的副产品为(写化学式).
(3)步骤③酸溶时,其中的铅与硝酸生成Pb(NO3)2及NO的离子方程式为;滤液2中溶质主要成分为(写化学式).
(4)步骤⑥合成三盐的化学方程式为 .
(5)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是 ( )
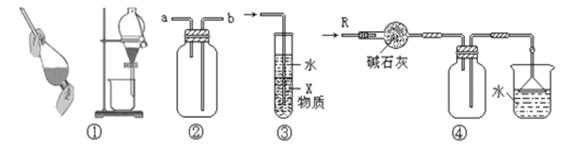
A. 装置①可用于分离酒精和水的混合物
B. 装置②可用于收集NH3、Cl2、SO2、NO2等气体
C. 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
D. 装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl样品中混有少量的CaCl2和NaBr,按下列程序操作可制得纯净的NaCl.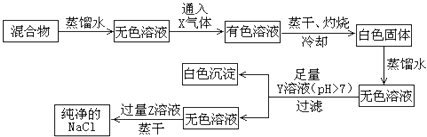
(1)X气体是 , Y溶液是 , Z溶液是 .
(2)过滤时,除漏斗外还需要的玻璃仪器有 .
(3)加入Y溶液的目的是;若在不使用pH试纸的情况下,检验Y溶液是否足量的方法是(简要回答操作过程及现象) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的( )
A.加入Al能放出H2的溶液中:ClO﹣、HCO ![]() 、SO
、SO ![]() 、NH
、NH ![]()
B.pH=2的溶液中:Fe2+、Na+、Mg2+、NO ![]()
C.能使KSCN溶液变红的溶液中:Na+、I﹣、NO ![]() 、HCO
、HCO ![]()
D.由水电离出的c(OH﹣)=1.0×10﹣13mol?L﹣1的溶液中:Na+、Ba2+、Cl﹣、Br﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com