
【题目】(1)在化学反应中,如果反应前后元素化合价发生变化,就一定有_______ 转移,这类反应属于________ 反应,元素化合价降低,表明该元素的原子______ 电子,含该元素的物质发生________ 反应,这种物质是________ 剂。
(2)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________________。
(3)B元素的正三价离子的3d亚层为半充满,则B的元素符号为_____,其基态电子排布式为_________________________________。
科目:高中化学 来源: 题型:
【题目】反应 Fe(s)+CO2(g)FeO(s)+CO(g) △H1,平衡常数为 K1,反应 Fe(s)+H2O(g)FeO(s)+H2(g) △H2,平衡常数为 K2;在不同温度时 K1、K2 的值如表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
(1) 反应 CO2(g)+H2(g)CO(g)+H2O(g)的反应热为△H ,平衡常数为 K,则△H= ____________(用△H1 和△H2 表 示), K= _______________ (用 K1 和 K2 表示),且由上述计算可知,反应CO2(g)+H2(g)CO(g)+H2O(g)是______________________________反应(填“吸热”或“放热”)。
(2) 现有反应:mA(g)+nB(g) pC(g)达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则:
①该反应的逆反应为反应___________(填“吸热”或“放热”,且 m+n___p(填“>"“=或“<”)
②减压使容器容积增大时,A的质量分数____________(填“增大”“减小”或“不变”,下同)。
③若容积不变加入B,则A的转化率_______________, B的转化率 ______________
④ 若加入催化剂,平衡时气体混合物的总物质的量____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有机物 用系统命名法命名:__。
用系统命名法命名:__。
(2)写出4—甲基—2—乙基—1—戊烯的结构简式:__。
(3)下列物质中属于同系物的是__。
①CH3CH2Cl②CH2=CHCl③CH3CH2CH2Cl④CH2ClCH2Cl⑤CH3CH2CH2CH3⑥CH3CH(CH3)2
A.①② B.①④ C.①③ D.⑤⑥
(4)0.1mol某烷烃燃烧,其燃烧产物全部被碱石灰吸收,碱石灰增39g。该烃的分子式为___;若它的核磁共振氢谱共有3个峰,则该烃可能的结构简式为___。(写出其中一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备Cu2(OH)2CO3,其工艺流程如下:
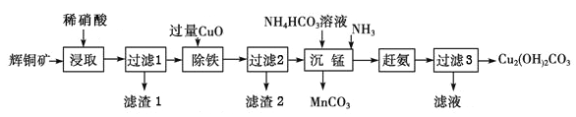
(1)“酸浸”过程中,将矿石粉碎,其目的是__________;加热能加快矿石粉“酸浸”速率,但温度不宜过高,其原因是__________。
(2)Cu2S和硝酸反应,其还原产物为NO。已知1 mol Cu2S完全反应时转移10 mol电子。写出该反应的离子方程式:_____________________。
(3)“除铁”中加入过量氧化铜发生反应的离子方程式为___________________。
(4)从过滤3得到的滤液中可提取一种肥料,它的化学式为__________;滤渣1的主要成分是__________(填化学式)。
(5)设计实验确认过滤2得到的滤液中是否有Fe3+:___________________________。
(6)取wg辉铜矿经上述流程转化,加入agCuO,滤渣2含bgCuO,最终得cmolCu2(OH)2CO3不考虑铜元素损失)。原辉铜矿含Cu2S的质量分数为____________。(用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | C | N | O | F | Ne | |||
3 | Na | Al | P | S | Cl |
(1)单质的化学性质最不活沷的元素是__________;
(2)氧的原子结构示意图是__________;
(3)形成化合物种类最多的元素是__________;
(4)HF和H2O中,热稳定性较强的是__________;
(5)N和P中,原子半径较小的是__________;
(6)常温下,会在浓硫酸中发生钝化的金属是_________;
(7)元素最高价氧化物对应水化物中,碱性最强的是___(填化学式),酸性最强的是_____(填“H2SO4”或“ HClO4”);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属Co、Ni性质相似,在电子工业以及金属材料上应用十分广泛.现以含钴、镍、铝的废渣(含主要成分为CoO、Co2O3、Ni、少量杂质Al2O3)提取钴、镍的工艺如下:
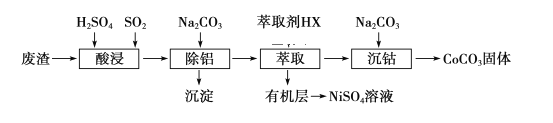
(1)酸浸时SO2的作用是___________________________________。
(2)除铝时加入碳酸钠产生沉淀的离子反应_________________________________。
(3)用CoCO3为原料采用微波水热法和常规水热法均可制得H2O2分解的高效催化剂CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价).如图是用两种不同方法制得的CoxNi(1-x)Fe2O4 在10℃时催化分解6%的H2O2 溶液的相对初始速率随x 变化曲线.

①H2O2 的电子式_________________________________。
②由图中信息可知:_________________________________法制取的催化剂活性更高。
③Co2+ 、Ni2+ 两种离子中催化效果更好的是_________________________________。
(4)已知煅烧CoCO3时,温度不同,产物不同.在400℃充分煅烧CoCO3,得到固体氧化物的质量2.41g,CO2的体积为0.672L(标况下),则此时所得固体氧化物的化学式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产中具有重要作用.
(1)某小组进行工业合成氨![]() 的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2,实验
的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2,实验![]() 、
、![]() 、
、![]() 中
中![]() 随时间
随时间![]() 的变化如图所示.
的变化如图所示.
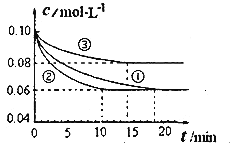
实验![]() 从开始到达到平衡状态的过程中,用
从开始到达到平衡状态的过程中,用![]() 表示的平均反应速率为 ___________.与实验
表示的平均反应速率为 ___________.与实验![]() 相比.实验
相比.实验![]() 所采用的实验条件可能为 ___________
所采用的实验条件可能为 ___________![]() 填字母
填字母![]() ,实验
,实验![]() 所采用的实验条件可能为 ___________
所采用的实验条件可能为 ___________![]() 填字母
填字母![]() .
.
![]() 增大压强
增大压强 ![]() 减小压强
减小压强 ![]() 升高温度
升高温度 ![]() 降低温度
降低温度 ![]() 使用催化剂
使用催化剂
(2)![]() 可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+ NO(g)+ NO2(g)
可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+ NO(g)+ NO2(g)![]() 2N2(g)+ 3H2O(g) △H<0,欲提高废气中氮氧化物的转化率,可采取的措施是 ___________
2N2(g)+ 3H2O(g) △H<0,欲提高废气中氮氧化物的转化率,可采取的措施是 ___________![]() 填字母
填字母![]()
![]() 升高温度
升高温度 ![]() 增大压强 c,增大
增大压强 c,增大![]() 的浓度
的浓度
(3)![]() 遇水发生水解反应,生成
遇水发生水解反应,生成![]() 的同时得到 ___________
的同时得到 ___________![]() 填化学式
填化学式![]() 是广谱高效消毒剂,制备原理为
是广谱高效消毒剂,制备原理为![]() 若转移1mol电子,则制取
若转移1mol电子,则制取![]() 的质量为 ___________.
的质量为 ___________.
(4)![]() 时,将
时,将![]() 的氨水与
的氨水与![]() 盐酸等体积混合,反应后溶液恰好显中性,则a ___________
盐酸等体积混合,反应后溶液恰好显中性,则a ___________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 用a、b表示
用a、b表示![]() 的电离平衡常数为 ___________.
的电离平衡常数为 ___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述不正确的是( )


A.用图①装置实现铁上镀铜,a极为铜,电解质溶液可以是CuSO4溶液
B.图②装置盐桥中KCl的Cl-移向右烧杯
C.图③装置中钢闸门应与外接电源的负极相连获得保护
D.图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报导,我国已研制出“可充室温钠—二氧化碳电池”,电极材料为钠金属片和碳纳米管,电解液为高氯酸钠四甘醇二甲醚,电池总反应为:4Na+3CO2![]() 2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
2Na2CO3+C,生成固体Na2CO3沉积在碳纳米管上。下列叙述不正确的是
A. 放电时钠金属片发生氧化反应
B. 放电时吸收CO2,充电时释放CO2
C. 放电时Na+向碳纳米管移动
D. 放电时的负极反应为2Na-2e-+CO32-=Na2CO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com