
| Ԫ�ش��� | �����Ϣ |
| X | ����һ�ֺ��ص�ԭ�Ӻ���û������ |
| Y | ����ɺܶ������ʲ�ͬ�ĵ��ʣ�Ҳ���γɻ�������������һ��Ԫ�� |
| Z | ��̬ԭ�ӵ����������Ų�ʽΪnsnnpn+1 |
| W | ����Ԫ����������ֻ������Щ��������ˮ��Ӧ�����ɼ����ƽ������W3����Ϊ�����������ɡ�� |
| T | ��Ҫ���ϼ���+1��+2�ۣ������������ˮ��Һ�г���ɫ |
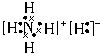 ��
��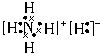 ��
��
| ||
| ||


 ѧ���������ν��Ͼ���ѧ������ϵ�д�
ѧ���������ν��Ͼ���ѧ������ϵ�д� Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
Happy holiday���ּ��������ҵ�㶫���������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��C+O2
| ||||
B��CaCO3
| ||||
C��2KMnO4
| ||||
| D��Zn+H2SO4=ZnSO4+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ӣ�Cd�������Ȼ��ܣ�CoCl2����Һ�У�������Ӧ�����ӷ���ʽΪ��Co2+��aq��+Cd��s��=Co��s��+Cd2+��aq����aq��ʾ��Һ�����罫�÷�Ӧ���Ϊ����ͼ��ԭ��أ�������˵��һ��������ǣ�������
���ӣ�Cd�������Ȼ��ܣ�CoCl2����Һ�У�������Ӧ�����ӷ���ʽΪ��Co2+��aq��+Cd��s��=Co��s��+Cd2+��aq����aq��ʾ��Һ�����罫�÷�Ӧ���Ϊ����ͼ��ԭ��أ�������˵��һ��������ǣ�������| A��Cd��������Co������ |
| B��ԭ��ع���ʱ�����ӴӸ����ص����������� |
| C��������������ԭ���������е������������׳أ��� �� |
| D���׳���ʢ�ŵ���CdCl2��Һ���ҳ���ʢ�ŵ���CoCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeSO4�ڷ�Ӧ���������� |
| B���÷�Ӧ��ˮ��Һ�н��� |
| C��Na2O2�������������ǻ�ԭ�� |
| D��Na2FeO4����Ԫ��+3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| ������kJ�� | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| n(NH3) |
| n(CO2) |
| n(H2O) |
| n(CO2) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2.2mol/L |
| B��4mol/L |
| C��5mol/L |
| D��6.25mol/L |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com