
下列离子方程式正确的是( )
A.碳酸氢钠水【解析】
HCO3-+ H2O H3O+ + CO32-
H3O+ + CO32-
B.醋酸铵溶于水:CH3COONH4 + H2O CH3COOH + NH3·H2O
CH3COOH + NH3·H2O
C.硫酸钙悬浊液中加入碳酸钠:CaSO4(s) + CO32- (aq) CaCO3(s) + SO42- (aq)
CaCO3(s) + SO42- (aq)
D.硫酸氢钠溶液中滴入氢氧化钡溶液呈中性:H++ SO42-+ Ba2++OH- ====BaSO4↓+ H2O
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源:2014年化学高考总复习单元检测 第四章非金属及其化合物练习卷(解析版) 题型:选择题
一定温度下,将Cl2缓慢通入水中。当通入的Cl2体积为V1时达到饱和,溶液中c(H+)变化如图中曲线a。已知Cl2的溶解度随温度升高而迅速降低,下列叙述中正确的是( )

A.将饱和氯水升温,继续通入Cl2时,溶液中c(H+)变化如曲线b
B.在饱和氯水中通入SO2气体,溶液中c(H+)变化如曲线c
C.降温,继续通入Cl2时,溶液中c(H+)的变化曲线如b
D.在饱和氯水中加入NaOH使pH=7,所得溶液中存在c(Na+)>c(ClO-)>c(Cl-)
>c(HClO)
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第六、七章化学反应与能量速率平衡卷(解析版) 题型:选择题
在容积可变的密闭容器中存在如下反应:2A(g)+2B(g) C(g)+3D(g) ΔH<0。该可逆反应的反应速率-时间、转化率-时间关系图如下:
C(g)+3D(g) ΔH<0。该可逆反应的反应速率-时间、转化率-时间关系图如下:

下列分析中不正确的是( )
A.图Ⅰ可体现t0时升高温度对反应速率的影响
B.图Ⅱ可体现t0时增大压强(缩小体积)或使用催化剂对反应速率的影响
C.图Ⅲ可体现催化剂对化学平衡的影响,且甲使用了催化剂
D.图Ⅲ可体现温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第八章水溶液中的离子平衡练习卷(解析版) 题型:选择题
常温下,Ksp(CaSO4)=9×10-6,常温下CaSO4在水中的沉淀溶解平衡曲线见图。下列说法正确的是( )
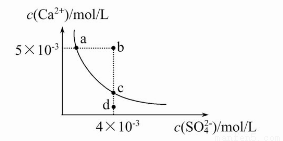
A.CaSO4在稀硫酸中的溶解性比在纯水中的溶解性强
B.b点将有沉淀生成,平衡后溶液中c(SO42-)一定等于3×10-3 mol/L
C.d点溶液通过蒸发可以变到c点
D.a点对应的Ksp等于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第八章水溶液中的离子平衡练习卷(解析版) 题型:选择题
常温下,pH=12的氨水中存在以下电离平衡:
NH3·H2O NH4+ +OH- 。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
NH4+ +OH- 。往其中加入少量0.01 mol·L-1NaOH溶液,保持不变的是( )
A. c(NH4+) B. c(OH-) C. c(NH3·H2O) D.c(NH4+)·c(OH-)
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第五章物质结构、元素周期律练习卷(解析版) 题型:填空题
短周期元素A、B、C、D、E的原子序数依次增大,其元素特征信息如表:

(1)D原子结构示意图为 _______ ,A在周期表中的位置为 。
(2)B和C形成的化合物的电子式为 。
(3)B和D简单离子的半径大小为 。
(4)元素非金属性强弱比较有很多方法,其中B和E的非金属性强弱的研究方案中不可行的是 (填序号)。
a.比较两种单质的颜色
b.比较两种单质与H2化合的难易程度
c.依据两元素在周期表中的位置
d.比较对应阴离子的还原性
e.比较最高价氧化物对应水化物的酸性
(5)E元素能与另外四种元素中的一种元素形成共价化合物,分子中的原子个数比为1∶3,相对分子质量为120.5,则该物质的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第五章物质结构、元素周期律练习卷(解析版) 题型:选择题
X、Y、Z是三种短周期的主族元素,在周期表中的位置如图所示,X原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )

A.原子半径:Y>Z>X
B.气态氢化物的热稳定性:X<Z
C.Y和Z的最高价氧化物对应水化物均为强酸
D.若Z的最高正价为+m,则X的最高正价也一定为+m
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第二章化学物质及其变化练习卷(解析版) 题型:选择题
下列离子方程式书写不正确的是( )
A.AlCl3溶液与烧碱溶液反应,当n(OH-)∶n(Al3+)=7∶2时, 2Al3++7OH-=Al(OH)3↓+ 
B.Cl2与FeBr2溶液反应,当n(Cl2)∶n(FeBr2)=1∶1时,2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
C.Ca(OH)2溶液与NaHCO3溶液反应,当
n[Ca(OH)2]∶n(NaHCO3)=1∶2时,
D.Fe与稀硝酸反应,当n(Fe)∶n(HNO3)=1∶2时,
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第三章金属及其化合物练习卷(解析版) 题型:填空题
阅读以下内容,回答问题。
冶炼金属一般有下列四种方法:①焦炭法;②水煤气(或H2,或CO)法;③活泼金属置换法;④电解法。四种方法各有优缺点,在工业上均有应用。
(1)一种无色气体A与红热的炭反应,得到另一种无色气体B,B与灼热的氧化铜反应,又得到A,则A、B分别为_______(填序号)。
A.O2、CO2 B.O2、CO C.CO2、CO D.CO、CO2
(2)下列说法错误的是_______(填序号)。
A.对废旧金属的最好处理方法是回收再利用
B.提炼金属要经过矿石的富集、冶炼、精炼三步
C.活泼金属的冶炼都是通过电解其盐溶液制得
D.热还原法中还原剂有焦炭、一氧化碳、氢气或活泼金属等
(3)钛(Ti)有“未来钢铁”之称。工业上常以:TiCl4+2Mg Ti+2MgCl2获得海绵状钛。该反应在下列哪种环境中进行_______ (填序号)。
Ti+2MgCl2获得海绵状钛。该反应在下列哪种环境中进行_______ (填序号)。
A.稀有气体中 B.空气中 C.氮气中 D.CO2气体中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com