
【题目】七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3)和铝矿渣(主要含Al2O3和SiO2)制备七铝十二钙的工艺如下:
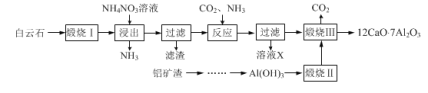
已知“煅烧Ⅲ”时发生反应为:12CaCO3+7Al2O3![]() 12CaO·7Al2O3+12CO2↑
12CaO·7Al2O3+12CO2↑
(1)写出“浸出”过程中CaO与NH4NO3溶液反应的化学方程式:___。
(2)检验“浸出”过程中有NH3生成的方法是:___。
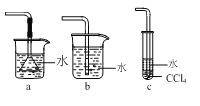
(3)如图所示装置中可用于实验室吸收NH3的是___(填字母)。
(4)溶液X中所含主要溶质的化学式为____。
(5)设计由铝矿渣制取Al(OH)3的方法,并简述过程:___。
【答案】CaO+2NH4NO3=Ca(NO3)2+2NH3↑+H2O 在“浸出”容器上方放一张湿润的红色石蕊试纸,试纸变蓝,证明有氨气生成(或用蘸有浓盐酸的玻璃棒放在“浸出”容器上方,看到白烟,证明有氨气生成) c NH4NO3 向铝矿渣中加入盐酸、搅拌,过滤得到AlCl3溶液,再向AlCl3溶液通入过量NH3、过滤、洗涤得到Al(OH)3
【解析】
白云石煅烧发生反应:CaCO3![]() CaO+CO2↑,在锻粉中加入适量的NH4NO3溶液后,CaO是碱性氧化物,能与水反应生成Ca(OH)2,由于反应放热,并且NH4NO3能与Ca(OH)2发生复分解反应生成Ca(NO3)2、NH3和H2O,NH3逸出,过滤得到Ca(NO3)2溶液,将CO2和NH3通入Ca(NO3)2溶液中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,过滤得到CaCO3固体和X,X主要成分为NH4NO3;
CaO+CO2↑,在锻粉中加入适量的NH4NO3溶液后,CaO是碱性氧化物,能与水反应生成Ca(OH)2,由于反应放热,并且NH4NO3能与Ca(OH)2发生复分解反应生成Ca(NO3)2、NH3和H2O,NH3逸出,过滤得到Ca(NO3)2溶液,将CO2和NH3通入Ca(NO3)2溶液中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,过滤得到CaCO3固体和X,X主要成分为NH4NO3;
盐酸溶解铝矿渣(主要含Al2O3和SiO2)得到AlCl3和SiO2,过滤除去SiO2得到AlCl3溶液,向AlCl3溶液通入过量NH3、过滤得到Al(OH)3,加热灼烧得到氧化铝,碳酸钙和氧化铝共混加热1500°C得到七铝十二钙,据此分析解答。
(1)CaO是碱性氧化物,能与水反应生成Ca(OH)2,由于反应放热,并且NH4NO3能与Ca(OH)2发生复分解反应生成Ca(NO3)2、NH3和H2O,所以总反应方程式为CaO+2NH4NO3=Ca(NO3)2+2NH3↑+H2O;
(2)NH3是碱性气体,可用湿润的红色石蕊试纸检验,石蕊试纸变蓝,方法为:在“浸出”容器上方放一张湿润的红色石蕊试纸,试纸变蓝,证明有氨气生成,或用蘸有浓盐酸的玻璃棒放在烧杯上方,看到白烟,证明有氨气生成;
(3)NH3极易溶于水,可用水吸收,但需要注意防倒吸,a、b两装置易出现倒吸现象,c能防倒吸,故答案为:c;
(4)将CO2和NH3通入Ca(NO3)2溶液中发生反应为:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,所以溶液X主要成分为NH4NO3;
(5)铝矿渣主要为Al2O3和SiO2,可用盐酸溶解,过滤除去SiO2、得到AlCl3溶液,向AlCl3溶液通入过量NH3、过滤得到Al(OH)3,
故答案为:向铝矿渣中加入盐酸、搅拌,过滤得到AlCl3溶液,再向AlCl3溶液通入过量NH3、过滤、洗涤得到Al(OH)3。


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)在医药、化工、民用等方面有广泛的应用。回答下面问题:
(1)最早制备H2O2使用的原料是易溶于水的BaO2和稀硫酸,发生反应的化学方程式是_____。BaO2的电子式为:__________。
(2)目前工业制备H2O2的主要方法是蒽醌法。反应流程如下:
![]()
已知:乙基蒽醌是反应中的催化剂。
①蒽醌法所用原料的物质的量之比为_____________。
②操作a是__________________。
③再生回收液的成分是______________________。
(3)测量过氧化氢浓度常用的方法是滴定法,某次测定时,取20. 00mL过氧化氢样品,加入过量硫酸酸化,用0. l000mol/L的KMnO4标准溶液滴定至终点,消耗10. 00mL,滴定时发生反应的离子方程式为____,该样品中H2O2的物质的量浓度为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g)其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=______________
(2)该反应为_______反应(选填吸热、放热);
(3)下列能使CO2的转化率增加的是___________________
(a)增大压强 (b)增加CO2的含量
(c)分离出产物H2O (d)升高温度
(4)830K时,若起始时:c(CO2)=2mol/L,c(H2)=3mol/L,平衡时CO2的转化率为60%,氢气的转化率为_________________
(5)能判断该反应是否达到化学平衡状态的依据是___________。
(a)容器中压强不变 (b)混合气体中 c(CO)不变
(c)v正(H2)=v逆(H2O) (d)混合气体的摩尔质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
有多种同分异构体,其中属于酯类且氯原子直接连接在苯环上的同分异构体有多少种(不考虑立体异构)
A.19种 B.9种 C.15种 D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在处理废水时某反应体系中有6种粒子:N2、HCO3-、ClO-、CNO-、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是( )

A. 在上述反应体系中,CNO-是氧化剂
B. 还原产物与氧化产物的物质的量之比为1∶3
C. 在标准状况下,产生4.48 L N2时转移0.8 mol电子
D. 上述反应中,只有两种元素化合价发生了变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿明洛芬属于苯丙氨酸类抗炎药。镇痛效果优于布洛芬。如图是阿明洛芬的一条合成路线。
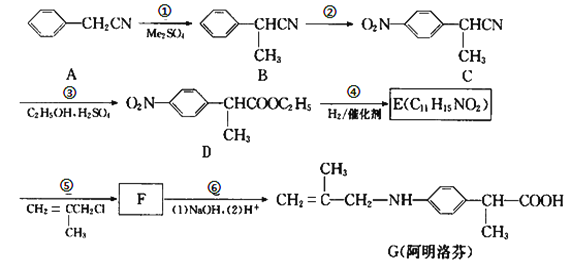
(1)反应①为取代反应,该步反应物Me2SO4中的“Me”表示___,D中官能团的名称是__。
(2)写出E的结构简式___。
(3)写出B到C这步反应的化学方程式___。
(4)G不能发生的反应类型是_____(填字母序号)。
A.水解反应 B.酯化反应 C.还原反应 D.加聚反应 E.缩聚反应
(5)写出F在NaOH溶液中反应的化学方程式_____。
(6)写出所有满足下列条件的B的同分异构体____。
①只含有一个环(即苯环)的芳香族化合物;
②核磁共振氢谱中氢峰的个数相比B的其它同分异构体最少。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)2,3—二乙基—1,3—戊二烯用H2完全加成后产物的名称:_________________________
(2)组成为C3H6Br2的卤代烃,同分异构体有_________种
(3)碳原子数小于10的烷烃中,一氯取代物没有同分异构体的烷烃共有_________种
(4)C4H10O的同分异构体中,属于醇类且含有“手性碳原子”的结构简式为__________。
(5)实验室制取乙炔的化学方程式:_______________________________________
(6)2—甲基—1,3—丁二烯加聚反应方程式:________________________________
(7)甲苯制取TNT的化学方程式:____________________________________________
(8)等物质的量的甲烷、乙烯、乙炔、苯等四种有机物分别完全燃烧,需要O2最多的是__;等质量的上述四种物质分别完全燃烧,需要O2最多的是____。
(9)写出间甲基苯乙烯的结构简式______________________________;
(10)与H2加成生成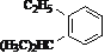 的炔烃的结构简式____________;
的炔烃的结构简式____________;
(11)写出4-甲基-2-乙基-1-戊烯的键线式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是()
编号 | 化学反应 | 离子方程式 | 评价 |
| 碳酸钙与醋酸反应 |
| 错误,碳酸钙是弱电解质,不应写成离子形式 |
| 向 |
| 错误,碱过量,应生成 |
|
|
| 正确 |
| 等物质的量的 |
| 正确 |
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
A. 含有NA个氧原子的氧气在标准状况下的体积约为22.4 L
B. 2 L 0.3 mol·L-1的硫酸钾溶液中钾离子浓度为0.6 mol·L-1
C. 常温常压下,32 g O2和O3的混合气体所含原子数为2NA
D. 25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com