
| A.从沸腾炉出来的炉气需净化,因为炉气中SO3会与杂质反应 |
| B.硫铁矿燃烧前需要粉碎,因为大块的不能燃烧 |
| C.SO3用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
| D.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源:不详 题型:填空题
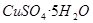 。
。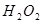 溶液,稍加热。
溶液,稍加热。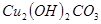 粉末至
粉末至 为
为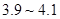 。
。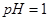 。
。 如下表:
如下表:| 物质 |  | 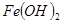 | 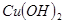 |
开始沉淀 | 2.7 | 7.6 | 4.7 |
完全沉淀 | 3.7 | 9.6 | 6.7 |
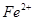 氧化为
氧化为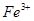 的目的是 。
的目的是 。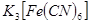 (铁氰化钾)验证II中
(铁氰化钾)验证II中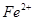 是否转化完全的现象是 。
是否转化完全的现象是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 |
| B.生产普通水泥的主要原料有石灰石、石英和纯碱 |
| C.工业上将粗铜进行精炼,应将粗铜连接在电源的正极 |
| D.在高炉炼铁的反应中,一氧化碳作还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
  压强 压强SO2的 转化率 温度 | 1×105 Pa | 5×105 Pa | 10×105 Pa | 50×105 Pa | 100×105 Pa |
| 450 ℃ | 97.5% | 98.9% | 99.2% | 99.6% | 99.7% |
| 550 ℃ | 85.6% | 92.9% | 94.9% | 97.7% | 98.3% |
 的空气是为了________。
的空气是为了________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
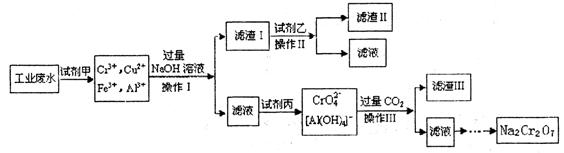
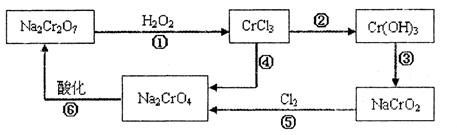
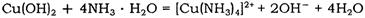
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
|
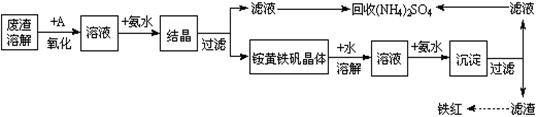
| A.氨水 | B.氢氧化钠 | C.盐酸 | D.硫酸 |
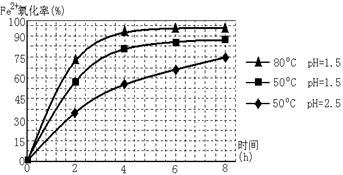
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 软锰矿制备高锰酸钾的一种工艺流程。
软锰矿制备高锰酸钾的一种工艺流程。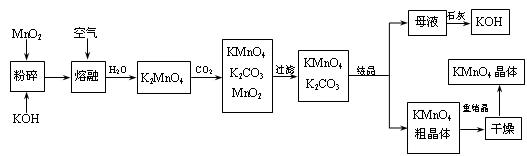
| A.75%酒精 | B.双氧水 | C.苯酚 | D.84消毒液(NaClO溶液) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
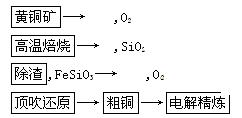
 到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
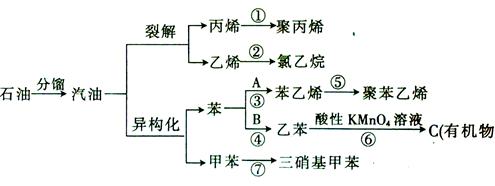
 ____________________________________________。
____________________________________________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com