
 ,则CH3+的电子式为
,则CH3+的电子式为 ,CH3-是缺电子的碳负离子,可以可作是甲基得到一个电子后的产物,CH3-的电子式为
,CH3-是缺电子的碳负离子,可以可作是甲基得到一个电子后的产物,CH3-的电子式为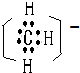 ,
,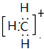 ;
;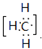 ;
; ;120°;
;120°;


科目:高中化学 来源: 题型:
| A、用水鉴别乙醇、甲苯和溴苯 |
| B、用燃烧法鉴别乙醇、苯和四氯化碳 |
| C、用酸性高锰酸钾溶液鉴别苯、环已烯和环己烷 |
| D、用碳酸钠溶液鉴别乙醇、乙酸和乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| X | ||
| Y | ||
| Z |
| A、X最外层电子数为2,处在ⅡA族 |
| B、Y的单质与氢气化合很容易 |
| C、Y的最高正价为+7,最低负价为-1 |
| D、Z是活泼的金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径/nm | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 | 0.102 | 0.143 |
| 最高或最低化合价 | -2 | +2 | +1 | +5 -3 | +7 -1 | +1 | +5 -3 | +3 | +6 -2 | +3 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X中肯定有碳碳双键 |
| B、X中可能有三个羟基和一个 一COOR官能团 |
| C、X中可能有两个羧基和一个羟基 |
| D、X中可能有三个羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有X、Y、Z三种元素,已知X、Y是元素周期表前20号元素,且X的原子序数比Y大4,元素Z形成的金属单质在日常生活中应用最广泛.请回答:
有X、Y、Z三种元素,已知X、Y是元素周期表前20号元素,且X的原子序数比Y大4,元素Z形成的金属单质在日常生活中应用最广泛.请回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com