
| A���������CeO2��Ce������������� | ||||||||
| B�������������Ļ�ѧ����ʽ�ɱ�ʾΪ��Ce+4HI�TCeI4+2H2�� | ||||||||
| C����Ce��SO4��2��Һ�ζ�����������Һ�������ӷ���ʽΪ��Ce4++2Fe2+=Ce3++2Fe3+ | ||||||||
D�������ȶ��ĺ���
|
136 58 |
138 58 |
140 58 |
142 58 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����к�̼Ԫ�صĻ����ﶼ���л��� |
| B��������л����������л��ܼ� |
| C���۵�͵Ļ��������л��� |
| D���л����г���̼Ԫ���⣬���������⡢����Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2��g��+Cl2��g��=2HCl��g����H=-184.6 kJ?mol-1 | ||
| B��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-802.3 kJ?mol-1 | ||
| C��2H2��g��+O2��g��=2H2O��l����H=-571.6 kJ?mol-1 | ||
D��CO��g��+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������һ��������������ΪH����λΪmol?L���Բ��� |
| B���ʱ���Ƿ�Ӧ�ȣ�����û������ |
| C����ʽ��H--T��S�еġ�H�Ƿ�Ӧ���ʱ� |
| D���ʱ��Hֻ�д�С��û������֮�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
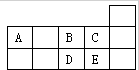 ���ΪԪ�����ڱ������ڵ�һ���֣������й�A��B��C��D��E����Ԫ�ص������У�����ȷ���ǣ�������
���ΪԪ�����ڱ������ڵ�һ���֣������й�A��B��C��D��E����Ԫ�ص������У�����ȷ���ǣ�������| A��A��B�γɵ������ӿ����У�AB32-��A2B42- |
| B��E���⻯��ķе��C���⻯��ķе�� |
| C��D�ڹ�����B��ȼ�յ���Ҫ����ΪDB3 |
| D����5��Ԫ���γ�ֻ�����Լ��ķǼ��Է��Ӷ���4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��4Q1+0.5Q3 |
| B��4Q1+0.5Q2 |
| C��4Q1+Q3 |
| D��4Q1+2Q2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3 |
| B��Cu2��OH��2CO3 |
| C��CH3CH2OH |
| D��Mg��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com