
【题目】有三种镁铝合金样品(组分比例不一定相同)①、②、③。小奉、小贤、小红三同学各取一种样品,对合金中镁的质量分数进行下列实验探究:
(1)小奉取样品①m1 g和过量的氢氧化钠溶液反应,然后过滤;再往滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,得到固体质量仍为m1 g。则合金中镁的质量分数为___________。(保留小数点后面2位)
(2)小贤取样品②m2 g和足量的稀硫酸反应,发现固体完全溶解,标准状况下得到气体体积为VL,则m2的取值范围是_________。(结果转化为最简分数)
(3)小红取不同质量的样品③分别和30 mL同浓度的盐酸反应,所取合金质量与产生气体的体积(标准状况下测定)如下所示:
实验序号 | a | b | c |
合金质量(g) | 0.51 | 0.765 | 0.918 |
气体体积(mL) | 560 | 672 | 672 |
求:I.盐酸的物质的量浓度_______
II.合金中镁的质量分数_______
III.要使c组实验后剩余合金中的铝恰好完全溶解,还需向容器中加入1.0 mol/L的氢氧化钠溶液多少mL_______?
【答案】47.06% 0.80V<m2<1.07V 2.0 mol/L 47.06% 78 mL
【解析】
(1)发生的反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑、NaAlO2+CO2+2H2O=NaHCO3+Al(OH)3↓、2Al(OH)3![]() Al2O3+3H2O,得到的固体是Al2O3,反应前后质量不变,说明氧化铝中的氧元素质量分数等于镁元素质量分数;
Al2O3+3H2O,得到的固体是Al2O3,反应前后质量不变,说明氧化铝中的氧元素质量分数等于镁元素质量分数;
(2)采用极限法计算固体质量范围;
(3)Ⅰ.先判断盐酸是否完全反应,若盐酸完全反应,根据氢气求出消耗的盐酸,再求出浓度;
Ⅱ.根据表中数据可知,a组中金属完全反应,根据金属的总质量和生成氢气的物质的量列方程组,计算;
Ⅲ.根据方程式中转化关系以及原子守恒计算。
(1)发生的反应为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑、NaAlO2+CO2+2H2O= NaHCO3+Al(OH)3↓、2Al(OH)3![]() Al2O3+3H2O,得到的固体是氧化铝,原固体为Mg、Al,反应后固体为Al2O3,反应前后固体质量不变,Mg的质量与Al2O3中O元素质量相等,则镁元素质量分数等于氧化铝中的氧元素质量分数,故合金中镁元素的质量分数=
Al2O3+3H2O,得到的固体是氧化铝,原固体为Mg、Al,反应后固体为Al2O3,反应前后固体质量不变,Mg的质量与Al2O3中O元素质量相等,则镁元素质量分数等于氧化铝中的氧元素质量分数,故合金中镁元素的质量分数=![]() ×100%=47.06%;
×100%=47.06%;
(2)假设全部是Mg,设镁的质量为x,Mg+2H+=Mg2++H2 ↑根据方程式可知24 gMg完全反应产生1 mol H2,其在标准状况下的体积为22.4 L,则x g Mg反应放出H2的体积为V,则![]() =
=![]() ,解得x=1.07V;
,解得x=1.07V;
假设合金全部是Al,设铝的质量是y,根据反应方程式2Al+6H+=2Al3++3H2↑可知:54 gAl完全反应产生3 mol H2,在标准状况下体积为67.2 L,y g Al反应产生H2的体积是V L,则![]() ,解得y=0.80V;
,解得y=0.80V;
因为是两种金属的合金,所以金属的质量介于0.80V与1.07V之间,即0.80V<m<1.07V;
(3)Ⅰ.b、c中生成的气体体积相同,c中金属的质量较大,则c中盐酸反应完全,n(H2)=![]() =0.03 mol,则n(HCl)=2n(H2)=0.06 mol,所以c(HCl)=
=0.03 mol,则n(HCl)=2n(H2)=0.06 mol,所以c(HCl)=![]() =2 mol/L;
=2 mol/L;
Ⅱ.a组合金完全反应,假设合金中Mg、Al的物质的量分别为x mol、y mol,则有:
24x+27y=0.510g,根据电子得失数目相等可知2x+3y=![]() ×2,解得x=0.01,y=0.01,则Mg的质量分数w(Mg)=
×2,解得x=0.01,y=0.01,则Mg的质量分数w(Mg)=![]() ×100%=47.06%;
×100%=47.06%;
Ⅲ.盐酸最终转化为NaCl,Al转化为NaAlO2,则由HCl~NaCl和Al~NaAlO2可知:
n(NaCl)=n(HCl)=2.0 mol/L×0.030 L=0.06 mol;
n(NaAlO2)=n(Al)=0.01 mol×![]() =0.018 mol;
=0.018 mol;
根据Na+守恒得:n(NaOH)= n(NaCl)+ n(NaAlO2)=0.06 mol+0.018 mol=0.078 mol
故V(NaOH)=![]() =0.078 L=78 mL。
=0.078 L=78 mL。


科目:高中化学 来源: 题型:
【题目】某兴趣小组为研究碳酸钠水解平衡与温度的关系,用数字试验系统测定一定浓度碳酸钠溶液的pH与温度的关系,得到曲线如图,下列分析不合理的是( )
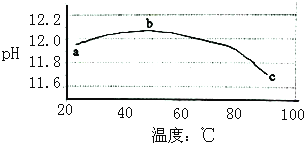
A.碳酸钠水解是吸热反应
B.ab段说明水解平衡向右移动
C.bc段说明水解平衡向左移动
D.水的电离平衡也对pH产生影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g)![]() C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是
C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是
①混合气体的密度 ②混合气体的压强 ③B的物质的量浓度 ④混合气体的总物质的量
A. ①② B. ②③ C. ①③ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置测定中和热的实验步骤如下:

①量取50mL 0.25mol/L H2SO4溶液倒入小烧杯中,测量温度;
②量取50mL 0.55mol/L NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)如图所示,仪器A的名称是_______________;
(2)NaOH溶液稍过量的原因 ______________。
(3)加入NaOH溶液的正确操作是_______(填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是 _________________________。
(5)实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)______
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是化工生产的主要原料之一,氨气的用途非常广泛。在一固定容积为2 L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,发生如下反应: N2(g)+3H2(g)![]() 2NH3(g)△H=-Q kJ/mol(Q>0)。
2NH3(g)△H=-Q kJ/mol(Q>0)。
(1)该反应所用的催化剂是_______(填写名称);该反应450℃时的平衡常数______500℃时的平衡常数(填“>”、“<”或“=”)。
(2)下列描述中能说明上述反应已达平衡的是_______
A. 3v正(H2)=2v逆(NH3) B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化 D.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2 mol计算从反应开始到平衡时,平均反应速率v(N2)为______________。
(4)在另一容积可变的容器内加入0.2 mol的N2和0.6 mol的H2,在相同条件下发生上述反应,则产生的NH3的物质的量比原平衡产生的NH3______(填“多”或“少”或”“一样”)。
(5)工厂生产的氨水稀释后可作肥料。稀释氨水时,随着水的增加溶液中减少的是_______
a.  b.
b. 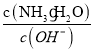 c.
c. 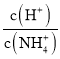 d.
d. 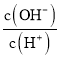
(6)液氨和水类似,也能电离:2NH3![]() NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____2×10-30(填“<”、“>”或“=”);
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____2×10-30(填“<”、“>”或“=”);
②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3-羟基丁酸(3-hydroxybutyrate)也称为β-羟基丁酸(beta-hydroxybutyrate),在工业中可用于合成可生物降解的塑料,如聚(3-羟基丁酸)。
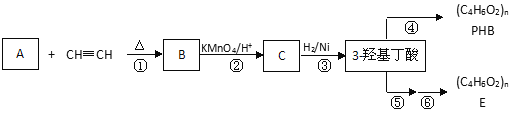
已知:i. 共轭二烯烃(如异戊二烯)与含有碳碳叁键的有机物作用时能形成环状化合物:
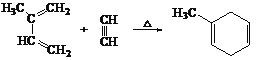
ii. 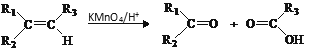
iii. 步骤②只有一种产物;E的结构中含有甲基
(1)A分子结构简式 _______;理论上B也可以由1,3-丁二烯与烃F来合成,则F的名称(系统命名法):_________;C中含有的官能团是_______(用符号表示)。
(2)写出反应类型:②_____________, ④_____________。
(3)PHB______(填“有”或“无”)固定熔沸点;它与E______(填“互为”或“不互为”)同分异构体。下列有机物具有类似共轭二烯烃性质的是__________(填序号);
a. ![]() b.
b. ![]()
c. ![]() d.
d. 
(4)写出反应⑤的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列有关叙述正确的是
A. 向0.1 mol·L1 Na2CO3溶液中通入适量CO2气体后:c(Na+)=2[c(![]() )+c(
)+c(![]() )+c(H2CO3)]
)+c(H2CO3)]
B. 常温下,pH=6的NaHSO3溶液中:c(![]() )c(H2SO3)=9.9×107 mol·L1
)c(H2SO3)=9.9×107 mol·L1
C. 等物质的量浓度、等体积的Na2CO3和NaHCO3混合:![]() <
<![]()
D. 0.1 mol·L1 Na2C2O4溶液与0.1 mol·L1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(![]() )+c(
)+c(![]() )+c(OH)=c(Na+)+c(H+)
)+c(OH)=c(Na+)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是一些物质的熔沸点数据(常压):
钾 | 钠 | Na2CO3 | 金刚石 | 石墨 | |
熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
沸点(℃) | 774 | 882.9 | 1850(完全分解产生CO2) | --- | 4250 |
金属钠和CO2在常压、890℃发生如下反应:4Na(g)+3CO2(g) ![]() 2Na2CO3(1)+C(s,金刚石);△H= —1080.9 kJ/mol
2Na2CO3(1)+C(s,金刚石);△H= —1080.9 kJ/mol
(1)上述反应的平衡常数表达式为________________;若4v正(Na)=3v逆(CO2),反应是否达到平衡________ (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,若反应时间为10min,金属钠的物质的量减少了0.2mol,则10min里CO2的平均反应速率为________________。
(3)高压下有利于金刚石的制备,理由_____________________________________________。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H= —357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(1)的热化学方程式:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式:
著名的蓝瓶子实验操作步骤如下:
①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色;
②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色;
③再打开瓶塞,振荡,溶液又变为蓝色;
④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。
试回答下列问题:

(1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________(填“A”或“B”);
(2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________(填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________(填“能”或“不能”);
(3)上述转化过程中,葡萄糖的作用是_________,亚甲基蓝的作用是_________;
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____;
(5)该实验中③、④操作能否无限次重复进行_________(填“能”或“不能”),理由是 _____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com