
 在实验室里,第一位同学取一小块金属钠做与水反应的实验.试完成下列问题:
在实验室里,第一位同学取一小块金属钠做与水反应的实验.试完成下列问题:分析 (1)钠暴露在空气中和氧气反应生成氧化钠而变暗;
(2)钠熔成小球,说明钠和水放出的热量使钠熔化;
(3)钠的密度小于水,钠的熔点较低,钠和水反应生成氢氧化钠和氢气且放出热量,钠和水反应生成氢氧化钠和氢气,随着反应的进行水的量减少,氢氧化钙溶液成为过饱和溶液,溶液中析出部分氢氧化钙,因为有氢氧化钠的存在,抑制氢氧化钙的溶解;
(4)钠能和氧气、水反应,和煤油不反应;
(5)氯气氧化碘离子为碘单质,碘遇淀粉变蓝色,氯气氧化碘离子为碘单质.
解答 解:(1)钠放置在空气中和氧气反应生成氧化钠而变暗,反应方程式为:4Na+O2═2Na2O,
故答案为:钠块表面由银白色变为暗灰色(或钠块表面变暗);4Na+O2═2Na2O;
(2)钠熔成小球,说明钠和水放出的热量使钠熔化,同时说明钠的熔点较低;
故答案为:钠与水反应放出热量;钠的熔点低;
(3)A.钠和水反应生成氢气,所以能观察到,故错误;
B.钠的熔点较低且钠和水反应放出大量的热使钠熔成小球,所以能观察到,故错误;
C.钙的活泼性大于钠,且钠、钙都易和水反应生成碱,所以钠不可能置换出钙,则看不到有金属钙生成,故正确;
D.因为有部分溶质析出而导致溶液成悬浊液,所以看到溶液变浑浊,故错误;
故答案为:C;
(4)根据以上知,钠能和氧气、水反应,和煤油不反应,且钠的密度大于煤油,所以钠可以保存在煤油中以隔绝空气和水,防止鈉变质,
故答案为:隔绝钠与空气中的氧气和水蒸气的接触,防止钠变质;
(5)氯气可氧化KI生成单质碘,淀粉遇碘变蓝色,则可用湿润淀粉碘化钾试纸检验,现象为试纸变蓝,反应的化学方程式为:Cl2+2KI=I2+2KCl,
故答案为:湿润淀粉碘化钾试纸变蓝,Cl2+2KI=I2+2KCl;
点评 本题考查了钠、氯气的性质,根据钠的物理性质和化学性质分析钠和水反应现象、钠的贮存,注意钠和饱和氢氧化钙溶液反应现象,氢氧化钙的溶解度随着温度的升高而降低,为易错点,题目难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题
| A. | BrCl和NaOH溶液反应生成NaCl、NaBrO两种盐 | |
| B. | BrCl具有较强的氧化性 | |
| C. | 能使润湿的淀粉碘化钾试纸变蓝 | |
| D. | BrCl与水反应中,BrCl既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
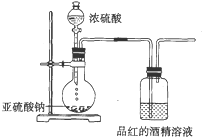 已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用.为了探究SO2的漂白作用到底是SO2本身具有的还是SO2与水作用的产物具有的,某学习小组设计了如图所示的装置来进行实验.请回答相关问题.
已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用.为了探究SO2的漂白作用到底是SO2本身具有的还是SO2与水作用的产物具有的,某学习小组设计了如图所示的装置来进行实验.请回答相关问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
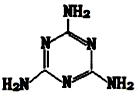 有机物三聚氰胺的结构如图所示:
有机物三聚氰胺的结构如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的质子数 | B. | 15N与14N是同种原子 | ||
| C. | 15N的核外电子数与中子数相同 | D. | 15N与14N互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 维生素A属于烃 | |
| B. | 维生素A能发生取代、加成、酯化反应 | |
| C. | 维生素A不能使酸性KMnO4溶液褪色 | |
| D. | 维生素A不能与金属钠反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤⑧ | B. | ②④⑥⑦⑨ | C. | ①③⑤⑥⑦ | D. | ①②④⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钢铁生锈,负极反应式为Fe-3e-═Fe3+ | |
| B. | 用石墨做电极电解硫酸铜溶液,有Cu和O2析出:2Cu2++OH-$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+2H2O | |
| C. | Na2CO3溶液滴加酚酞,溶液变红:CO32-+2H2O?H2CO3+2O2↑ | |
| D. | 酸性高锰酸钾溶液中加入草酸钠,溶液褪色:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com