
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含的离子如下表所示:
阳离子 | NH4+、Na+、Mg2+ |
阴离子 | OH-、NO3—、SO42— |
取等质量的三种化合物配制成相同体积的溶液,其溶质的物质的量浓度:c(甲)>c(乙)>c(丙)。
(1)甲是________,向AlCl3溶液中逐滴加入甲溶液,观察到的现象是________,对应的离子方程式为________。
(2)乙是______,设计实验确定乙的物质组成________(若乙已确定,则不填该空)。
(1)NaOH 先生成白色沉淀,继续滴加,白色沉淀消失 Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2—+2H2O
(2)(NH4)2SO4或NH4NO3 取乙溶液于小试管中,加入适量BaCl2溶液,若有白色沉淀析出,则乙是(NH4)2SO4,若无明显现象,则乙是NH4NO3
【解析】甲、乙、丙均是可溶性强电解质,则OH-只能与Na+组成NaOH,三种化合物不含相同离子,所以甲、乙、丙有两种组合(括号里数字表示相对分子质量),第一组:NaOH(40)、(NH4)2SO4(132)、Mg(NO3)2(148);第二组:NaOH(40)、NH4NO3(80)、MgSO4(120),根据溶质质量相等、溶液体积相等以及物质的量浓度大小关系判断,相对分子质量:Mr(丙)>Mr(乙)>Mr(甲),则乙可能是硫酸铵或硝酸铵。


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-4练习卷(解析版) 题型:填空题
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,熔点422
℃,沸点1366 ℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO42—等杂质)、Cu、稀硫酸、SO2等为原料合成CuCl的工艺流程如下:
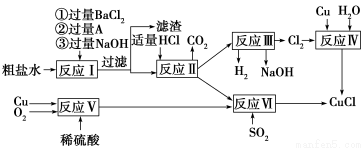
(1)A的化学式为________。
(2)写出反应Ⅴ的化学方程式______________________________________
(3)写出反应Ⅵ的离子方程式______________________________________
(4)本工艺中可以循环利用的物质是(用化学式表示)___________________________
(5)反应Ⅵ后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70 ℃燥2小时,冷却,密封包装即得产品。于70 ℃真空干燥的目的是_________________________
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练3-1练习卷(解析版) 题型:填空题
下图表示的是向Na2CO3溶液中滴入稀盐酸时产生CO2
的过程。
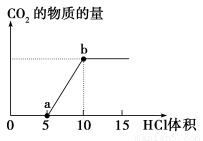
(1)写出a点以前发生反应的离子方程式:_____________________________________
(2)写出a到b点发生反应的离子方程式:_____________________________________
(3)若某Na2CO3溶液中含m mol Na2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于________mol(用含字母m的代数式表示)。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:选择题
硫代硫酸钠可作为脱氯剂,已知25.0 mL 0.100 mol·L-1Na2S2O3溶液恰
好把224 mL(标准状况下)Cl2完全转化为Cl-,则S2O42—将转化为( )
A.S2- B.SC.SO32— D.SO42—
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-3练习卷(解析版) 题型:选择题
下列物质分别与水发生反应:①Na、②NaH、③NO2、④Cl2、⑤SO3、
⑥Na2O2,其中属于氧化还原反应,但水既不是氧化剂又不是还原剂的是( )
A.①③⑥ B.②⑤C.③④⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-2练习卷(解析版) 题型:选择题
常温下,某未知溶液中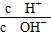 =1×1012,且含有大量Al3+和NO3—,检
=1×1012,且含有大量Al3+和NO3—,检
验此溶液中是否大量存在以下6种离子:①SiO32—、②NH4+、③Fe2+、④Na+、⑤HCO3—、⑥Cl-,其中不必检验就能加以否定的离子是( )
A.①③⑤ B.②③④C.①②⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练2-1练习卷(解析版) 题型:填空题
已知A、B,C为中学化学中常见的单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们可以按下图进行反应。
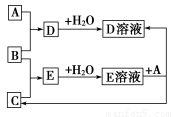
回答下列问题:
(1)A、B、C三种元素中的任意两种元素形成的化合物所属物质类别一定不是________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
(2)A、B、C三种元素中有一种是金属,则这种元素是A、B、C中的________,理由是________。
(3)如果E溶液是一种强酸,则E的化学式为________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练1-3练习卷(解析版) 题型:选择题
如图是某硫酸试剂瓶标签上的部分文字。据此,下列说法正确的是( )

A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量的该硫酸反应生成2 g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2 mol/L
D.向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习2-3-2氧化还原反应方程式配平及计算练习卷(解析版) 题型:填空题
高锰酸钾(KMnO4)是一种常用的氧化剂。
(1)有下列变化:CO32-→CO2、C2O42-→CO2、Fe3+→Fe2+,找出其中一个变化与“MnO4-→Mn2+”组成一个反应,写出该反应的离子方程式: 。
(2)高锰酸钾可代替二氧化锰用来制取Cl2,则反应中氧化剂和还原剂的物质的量之比为 。
(3)高锰酸钾与硫化亚铁有如下反应:10FeS+6KMnO4+24H2SO4=3K2SO4+6MnSO4+5Fe2(SO4)3+10S+24H2O。若上述反应前后固体的质量减少了2.8 g,则硫元素与KMnO4之间发生转移的电子数目为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com