
下列实验“操作和现象”与“结论”对应关系正确的是( )
| 操作和现象 | 结论 | |
| A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体 | HNO3分解生成了NO2 |
| B | 向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,没有红色沉淀生成 | 淀粉没有水解成葡萄糖 |
| C | 向无水乙醇中加入浓H2SO4,加热至170℃,产生的气体通入酸性KMnO4溶液,紫红色褪去 | 使溶液褪色的气体只是乙烯 |
| D | 向饱和Na2CO3溶液中通入足量CO2,溶液变浑浊 | 析出了NaHCO3 |
科目:高中化学 来源: 题型:
某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证:
猜想Ⅰ:甲酸具有酸性
实验Ⅰ:在甲酸溶液中滴加紫色石蕊试液
猜想Ⅱ:甲酸能发生酯化反应
实验Ⅱ:[装置如图(1)所示]
猜想Ⅲ:甲酸能发生银镜反应
实验Ⅲ:[步骤如图(2)所示]
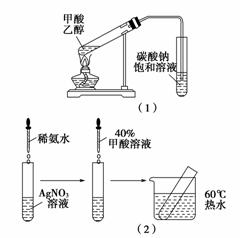
问题Ⅰ:请你进一步设计实验证明甲酸是强酸还是弱酸:______________________________________________。
问题Ⅱ:实验Ⅱ能验证猜想Ⅱ吗?________;如能,请说明你的理由;如不能,请指出实验Ⅱ中的错误__________________________________________________。
问题Ⅲ:分析甲酸的结构,实验Ⅲ中没有出现任何现象的可能原因是_______________________________。
问题Ⅳ:请你在仔细分析甲酸的组成和结构的基础上,再提出一个关于甲酸性质的猜想并设计实验方案验证你的猜想:
(1)你提出的猜想是______________________。
(2)你设计的实验方案是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
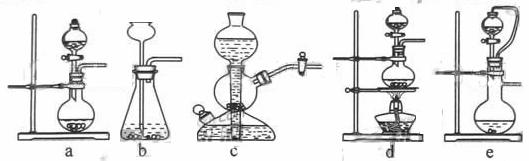
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是 (填写字母)。
41.若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,至少需要称取亚硫酸钠
g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠 g (保留一位小数)。
42.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。
石灰-石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO4·2H2O。其流程如下图:
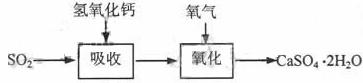
碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
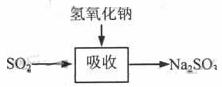
已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 。和碱法相比,石灰-石膏法的优点是 ,缺点是 。
43.在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A、②④⑤③①
B、③②④①⑤
C、③④②⑤①
D、②④③⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
C.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接存放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是( )
①除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离 ②除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤、分液、干燥、蒸馏 ③除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 ④除去乙醇中少量的乙酸:加足量生石灰,蒸馏
A.①② B.②④
C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
普通漏斗(如图所示)是中学化学实验室常用仪器之一。我们对它的用途并不陌生。
(1)请举两例说明普通漏斗在化学实验中的运用:_____________________________________________。
(2)你是否探讨过在化学实验中创新地使用普通漏斗?请你积极参与下面的讨论。
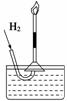
①如图是某同学实验室制备H2并验证H2具有可燃性装置的一部分,请说出他这样做的优点:________。

②某同学用苯萃取碘水中的碘时,找不到分液漏斗。他灵机一动,先在试管中将混合液充分振荡后静置,然后再用普通漏斗与其他常见实验仪器和用品组装成一个简易分液器进行分液(如图所示),解了燃眉之急。试分析该设计的不足之处。
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.12克铁粉加入2摩/升氯化铁溶液25毫升中,充分的反应后,其结果是 ( )
A. 铁有剩余 B. 往溶液中滴入无色KSCN溶液,显红色
C. Fe2+与Fe3+物质的量之比为6 :1
D. 氧化产物与还原产物的物质的量之比为2 :5
查看答案和解析>>
科目:高中化学 来源: 题型:
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是
| | |||
| A.将海带灼烧成灰 | B.过滤得含I-溶液 | C.萃取后放出碘 的CCl4溶液 | D.分离碘并回收CCl4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com