
����Ŀ����1����Ԫ��λ��Ԫ�����ڱ��ĵ�3����II A�壬��Ԫ�ص�ԭ�ӽṹʾ��ͼΪ
��д��Ԫ�ص�Ԫ�ط��ţ�___________��
�ڼ�Ԫ��ԭ�Ӻ�����_________�����Ӳ㡣
�ۼ�Ԫ�صĽ����ԣ���ԭ��ʧ���ӵ�����������Ԫ��_________������ǿ��������������
��2�������������ʵ��������ܷ����ֽⷴӦ��2H2O2 =2H2O+O2�����ֽ�������ʵ��̽�����ڼס�����֧��С��ͬ���Թ��и�װ��3mL 5%�Ĺ���������Һ���������еļ��Թ��м�������MnO2��ĩ�������ʵ��������д���пհס�
��ʵ��Ŀ�ģ��о������Թ�������ֽⷴӦ���ʵ�Ӱ�졣
��ʵ������___________��ѡ�������������������Թ��з�Ӧ�����ң�Ѹ�ٷų���ɫ���塣
��ʵ�����____________________________________________________��
���𰸡�Na 3 �� �� �����ɼӿ컯ѧ��Ӧ����
��������
��1����Ԫ��λ��Ԫ�����ڱ��ĵ�3����II A�壬���ΪMgԪ�أ�������Ԫ�ص�ԭ�ӽṹʾ��ͼ֪������NaԪ�أ��ݴ˴��⡣
��������Ԫ�أ�
��Ԫ�����ڵ�������������Ӳ�����ֵ��ȣ�
��ͬһ����Ԫ���У�Ԫ�صĽ���������ԭ�������������������
��2���ڴ����ܼӿ췴Ӧ���ʣ�
�۸���ʵ������ȷ�������Է�Ӧ���ʵ�Ӱ�졣
��1����Ԫ��λ��Ԫ�����ڱ��ĵ�3����IIA�壬���ΪMgԪ�أ�������Ԫ�ص�ԭ�ӽṹʾ��ͼ֪������NaԪ�أ�
������NaԪ�أ��ʴ�Ϊ��Na��
��Ԫ�����ڵ�������������Ӳ�����ֵ��ȣ����Լ�Ԫ��ԭ�Ӻ�����3�����Ӳ㣬�ʴ�Ϊ��3��
��ͬһ����Ԫ���У�Ԫ�صĽ���������ԭ��������������������ƺ�þ����ͬһ���ڣ����Ƶ�ԭ������С��þ������þ�Ľ�����С���ƣ��ʴ�Ϊ������
��2���ڴ����ܼӿ췴Ӧ���ʣ����Լ��Թ��з�Ӧ�Ͼ��ң��ʴ�Ϊ���ס�
�۸���ʵ������֪���д����ķ�Ӧ���ʱ�û�д����ķ�Ӧ���ʿ죬�ɴ˵ó������ܼӿ컯ѧ��Ӧ���ʣ��ʴ�Ϊ�������ɼӿ컯ѧ��Ӧ���ʡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������һ�����ܱ������и�������A��B��C��������һ�������·�����Ӧ�����Ļ�ѧƽ�⣺aA(g) + bB(g)![]() xC(g)��������ͼ��ʾ�Ĺ�ϵ(c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ)����ͼ�У�Y����ָ( )
xC(g)��������ͼ��ʾ�Ĺ�ϵ(c%��ʾƽ�������в���C�İٷֺ�����T��ʾ�¶ȣ�p��ʾѹǿ)����ͼ�У�Y����ָ( )

A����Ӧ��A�İٷֺ���
B��ƽ������������B�İٷֺ���
C��ƽ���������ܶ�
D��ƽ��������ƽ��Ħ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ӦN2��g��+3H2��g��![]() 2NH3��g������Ӧ���̵������仯��ͼ��ʾ����֪N2��g����H2��g����Ӧ����17 g NH3��g�����ų�46.1 kJ��������
2NH3��g������Ӧ���̵������仯��ͼ��ʾ����֪N2��g����H2��g����Ӧ����17 g NH3��g�����ų�46.1 kJ��������

��ش��������⣺
��1���÷�Ӧͨ���������������Ӵ�����ʹͼ��E��________��������������С������E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿_______��������____________________________��
��2��ͼ����H��______kJ��mol��1��
��3����ʼ����2mol��L��1 N2��5.5 mol��L��1 H2 ������50 min��NH3��Ũ��Ϊ1mol��L��1����v(N2)��_________mol��L��1��min��1��c(H2)��___________mol��L��1��
��4����֪NH3��g��=== NH3 (l) ��H=��QkJ��mol-1����дN2��g��+3H2��g��===2NH3 (l)���Ȼ�ѧ����ʽ___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼���仯����㷺��������Ȼ�硣��ش��������⣺
(1)��CO2��NH3Ϊԭ�Ͽɺϳ����ء���֪
��2NH3(g)+CO2(g)=NH2COONH4(s) ��H=��159.47 kJ��mol��1
��NH2COONH4(s)=CO(NH2)2(s)+H2O(g) ��H=+116.49 kJ��mol��1
��H2O(l)=H2O(g) ��H=+88.0 kJ��mol��1
д��NH3��CO2�ϳ����غ�Һ̬ˮ���Ȼ�ѧ����ʽ______________________________��
(2)�����ǵ�����̼Ԫ�ص�������ճء�
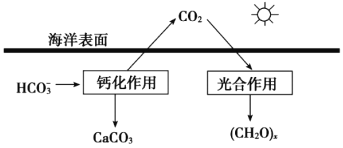
�����ں�ˮ�е�CO2��Ҫ��������̼��ʽ���ڣ�����CO2��H2CO3��___________��___________��
���ں���̼ѭ���У���ͨ����ͼ��ʾ��;����̼��д���ƻ����õ����ӷ���ʽ___________��
(3)���³�ѹ�£������е�CO2����ˮ�дﵽƽ��ʱ����ת����ϵ���£�
��CO2+H2O![]() H2CO3 K=1.8��10��3
H2CO3 K=1.8��10��3
��H2CO3![]() H++HCO3�� Ka1=4.3��10��7��
H++HCO3�� Ka1=4.3��10��7��
��HCO3��![]() H++CO32�� Ka2=5.6��10��11
H++CO32�� Ka2=5.6��10��11
ͨ������£���ˮ��pHԼΪ8��������ˮ�ĵ��뼰H2CO3�ĵڶ������룬����Һ��c(CO2)=____________________________________________mol/L��(������λ��Ч����)
(4)Ϊ�˲���ij��ˮ����̼��������ȡ100mL��ˮ���ữ����N2����CO2������NaOH��Һ���ա���1.0mol/L����ζ�����Һ�����ɵ�V(CO2)��V(����)�仯��ϵ��ͼ1��ʾ��������Һ������Ũ���ɴ�С��˳��Ϊ__________����ˮ����̼��Ũ��Ϊ___________mol/L��
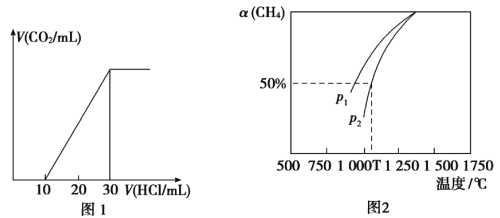
(5)��CO2����Ȼ�������Ʊ�CO��H2��CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)���ܱ�������Ũ�Ⱦ�Ϊ0.1mol/L��CH4��CO2����һ�������·�Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ2��ʾ����ѹǿp1___________p2(�>����<)����p2=3MPa����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kp=___________MPa2(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
2CO(g)+2H2(g)���ܱ�������Ũ�Ⱦ�Ϊ0.1mol/L��CH4��CO2����һ�������·�Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ2��ʾ����ѹǿp1___________p2(�>����<)����p2=3MPa����T��ʱ�÷�Ӧ��ƽ�ⳣ��Kp=___________MPa2(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��һ���¶��£��������ˮϡ��������Һ�ĵ�����������ͼ����ش�

��1����O����Ϊʲô������___________________��
��2��a��b��c�����������Ũ����С�����˳��Ϊ____________��
��3��a��b��c�����У�����ĵ���̶�����һ����_________��
��4����ʹc����Һ�е�c(CH3COO��)��ߣ������´�ʩ�У���ѡ��__________��
A������ B���Ӻ�ϡ��NaOH��Һ C���ӹ���KOH D����ˮ
E���ӹ���CH3COONa F����Zn�� G����MgO���� H����Na2CO3����
��5����ϡ�����У����Ŵ���Ũ�ȵĽ��ͣ�����ʼ�ձ����������Ƶ�����______________��
A��c(H��) B��H������ C��CH3COOH������ D��c(H��)/c(CH3COOH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2018��10��15�գ��й��á����������ҡ����ػ���ɹ��ԡ�һ��˫�ǡ���ʽ���䱱������ȫ����������ϵͳ��15��16�����ǣ������ƽ���Ϊ������泥�NH4ClO4���ȡ��Ʊ�NH4ClO4�Ĺ����������£�
����ʳ��ˮ![]() NaClO3
NaClO3![]() NaClO4
NaClO4![]() NaClO4
NaClO4![]() NH4ClO4
NH4ClO4
����˵���������
A. NH4ClO4�������ӻ�����
B. �ܽ�ȣ�NaClO4��NH4ClO4
C. ���NaClO3��Һʱ������ӦʽΪClO3-��H2O��2e-=C1O4-��2H+
D. �������п�ѭ�����õ�������NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ�£�һ��������(Cl2O)Ϊ�ػ�ɫ���壬�е�Ϊ3.8 �棬42 �����ϻ�ֽ�����Cl2��O2��Cl2O������ˮ����ˮ��Ӧ����HClO��
���Ʊ���Ʒ��
�������Ϳ���(�����뷴Ӧ)�������1��3���ͨ�뺬ˮ8%��̼�������Ʊ�Cl2O������ˮ����Cl2O(����Cl2)�Ʊ���������Һ��

��1����װ�õ�����˳��Ϊ___��___��___��________��____��___________
��2��װ��B�ж�����ݺͽ������������_��װ��C��������__��
��3���Ʊ�Cl2O�Ļ�ѧ����ʽΪ___��
��4����Ӧ�����У�װ��B�������ˮ�У���Ŀ����___��
��5���˷��������������ֱ������ˮ�Ʊ���������Һ��������Ҫ�ŵ㣬�ֱ���____��
���ⶨŨ�ȣ�
��6����֪������ɱ�FeSO4�����ʻ�ԭ��������ʵ�鷽���ⶨװ��E������Һ�д���������ʵ���Ũ�ȣ���ȡ10 mL������������Һ����ϡ����100 mL���ٴ�����ȡ��10.00 mL����ƿ�У�������10.00 mL 0.80 mol��L��1��FeSO4��Һ����ַ�Ӧ����0.050 00 mol��L��1������KMnO4��Һ�ζ����յ㣬����KMnO4��Һ24.00 mL����ԭ��������Һ��Ũ��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������X������Y��0.16 mol����10 L�����ܱ������У�������ӦX(g)+Y(g)![]() 2Z(g)����H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g)����H<0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����
A. ��Ӧǰ2 min��ƽ������v(Z)=2.0��10-3 mol��(L��min)-1
B. �����������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��)>v(��)
C. ���¶��´˷�Ӧ��ƽ�ⳣ��K=1.44
D. �����������䣬�ٳ���0.2 mol Z��ƽ��ʱX�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ʱHClO��Ka=3.0��10-8��HF��Ka=3.5��10-4���ֽ�pH���������ͬ�Ĵ�������������Һ�ֱ������ˮϡ�ͣ�pH����Һ����ı仯��ͼ��ʾ������������ȷ����
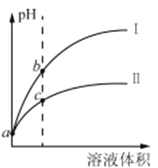
A. ����IΪ������ϡ��ʱpH�仯����
B. ȡa�����������Һ���к���ͬ�������ͬŨ�ȵ�NaOH��Һ�����Ĵ�����������С
C. a��ʱ������������ͬ��С��п������ʱ������ᷴӦ�����ʴ�
D. b����Һ��ˮ�ĵ���̶ȱ�c����Һ��ˮ�ĵ���̶�С
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com