
����Ŀ�����³�ѹ�£�һ��������(Cl2O)Ϊ�ػ�ɫ���壬�е�Ϊ3.8 �棬42 �����ϻ�ֽ�����Cl2��O2��Cl2O������ˮ����ˮ��Ӧ����HClO��
���Ʊ���Ʒ��
�������Ϳ���(�����뷴Ӧ)�������1��3���ͨ�뺬ˮ8%��̼�������Ʊ�Cl2O������ˮ����Cl2O(����Cl2)�Ʊ���������Һ��

��1����װ�õ�����˳��Ϊ___��___��___��________��____��___________
��2��װ��B�ж�����ݺͽ������������_��װ��C��������__��
��3���Ʊ�Cl2O�Ļ�ѧ����ʽΪ___��
��4����Ӧ�����У�װ��B�������ˮ�У���Ŀ����___��
��5���˷��������������ֱ������ˮ�Ʊ���������Һ��������Ҫ�ŵ㣬�ֱ���____��
���ⶨŨ�ȣ�
��6����֪������ɱ�FeSO4�����ʻ�ԭ��������ʵ�鷽���ⶨװ��E������Һ�д���������ʵ���Ũ�ȣ���ȡ10 mL������������Һ����ϡ����100 mL���ٴ�����ȡ��10.00 mL����ƿ�У�������10.00 mL 0.80 mol��L��1��FeSO4��Һ����ַ�Ӧ����0.050 00 mol��L��1������KMnO4��Һ�ζ����յ㣬����KMnO4��Һ24.00 mL����ԭ��������Һ��Ũ��Ϊ___��
���𰸡�ADBCE�ӿ췴Ӧ���ʣ�ʹ��Ӧ��ֽ��г�ȥCl2O�е�Cl22Cl2��Na2CO3===Cl2O��2NaCl��CO2(��2Cl2��Na2CO3��H2O===Cl2O��2NaCl��2NaHCO3)��ֹ��Ӧ���Ⱥ��¶ȹ��ߵ���Cl2O�ֽ��ƵõĴ�������Һ���Ƚϸߣ�Ũ�Ƚϴ�1.000mol��L��1
��������
Aװ���ö������̺�Ũ�����Ʊ���������Dװ�ñ���ʳ��ˮ���������е��Ȼ������壬������γ�1��3�Ļ������ͨ��Bװ�ã���ֹ��Ӧ���Ⱥ��¶ȹ��ߵ���Cl2O�ֽ⣬װ��B�������ˮ�У��ڽ�������������뺬ˮ8%��̼���Ƴ�ַ�Ӧ�Ʊ�Cl2O����ӦΪ��2Cl2+Na2CO3�TCl2O+2NaCl+CO2��ͨ��Cװ�����ճ�ȥCl2O�е�Cl2������Eװ������ˮ����Cl2O�Ʊ���������Һ���ݴ˷���������
��1��Aװ���Ʊ�������Dװ���������������е��Ȼ������壬������γ�1��3�Ļ������ͨ��Bװ�ã��뺬ˮ8%��̼���Ƴ�ַ�Ӧ�Ʊ�Cl2O��Cװ�����ճ�ȥCl2O�е�Cl2��Eװ������ˮ����Cl2O�Ʊ���������Һ���ʴ�Ϊ��A��D��B��C��E��������װ��B�ж�����ݺͽ�����������Ǽӿ췴Ӧ���ʣ�ʹ��Ӧ��ֽ��У�װ��Cװ�������������Ȼ�̼��Һ���������dz�ȥCl2O�е�Cl2�������������Ϳ����������뷴Ӧ���������1��3���ͨ�뺬ˮ8%��̼�������Ʊ�Cl2O����ӦΪ��2Cl2+Na2CO3�TCl2O+2NaCl+CO2��2Cl2+Na2CO3+H2O�TCl2O+2NaCl+2NaCO3�������������֪��Cl2O 42�����ϻ�ֽ�����Cl2��O2����Ϊ��ֹ��Ӧ���Ⱥ��¶ȹ��ߵ���Cl2O�ֽ⣬װ��B�������ˮ�У���5���˷��������������ֱ������ˮ�Ʊ���������Һ��������Ҫ�ŵ㣬�ֱ����ƵõĴ�������Һ���Ƚϸߣ�Ũ�Ƚϴ�����6�����ݷ�ӦH2O+ClO-+2Fe2+=Cl-+2Fe3++2OH-��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O����ԭ��������Һ��Ũ��Ϊ![]() =1.000mol��L��1��
=1.000mol��L��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о���ѧϰС���ij��ɫˮ���ijɷֽ��м��飬��֪��ˮ����ֻ���ܺ���K+��Mg2+��Fe3+��Cu2+��Al3+��Ag+��Ca2+��CO![]() ��SO
��SO![]() ��Cl���е����������ӣ���С��ͬѧȡ100mLˮ������ʵ�飬��ˮ�����ȵμ����ᱵ��Һ���ٵμ�1mol/L�����ᣬʵ������г��������ı仯�������ͼ��ʾ������ʾ:Al3+��CO
��Cl���е����������ӣ���С��ͬѧȡ100mLˮ������ʵ�飬��ˮ�����ȵμ����ᱵ��Һ���ٵμ�1mol/L�����ᣬʵ������г��������ı仯�������ͼ��ʾ������ʾ:Al3+��CO![]() �����棩
�����棩

��1��ˮ����һ�����е���������_____�������ʵ���Ũ��֮��Ϊ_____��
��2��д��BC������ʾ��Ӧ�����ӷ���ʽ��_____��
��3����B��C��仯������������������Ϊ_____��
��4���Ը���ʵ�����Ʋ�K+�Ƿ���ڣ�_____���������������������������ڣ�K+�����ʵ���Ũ��c��K+���ķ�Χ��_____������K+�����ڣ��ػش���ʣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���һ���ݻ�Ϊ3L������ܱ�������ͨ��1molN2��3molH2��2min��������ڵ�ѹǿ�ǿ�ʼʱ��0.8���������ʱ����V(H2)Ϊ�� ��
A.0.2mol/(L��min)B.0.6mol/(L��min)
C.0.1mol/(L��min)D.0.3mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���Ԫ�����ڱ���һ���֣���Ա��еĢ١�����Ԫ�أ���Ԫ�ط��Ż�ѧʽ��ջش��������⣺
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
�� | �� | �� | ||||||
�� | �� | �� | �� | �� | �� | �� | ||
�� | �� | �� |
(1)��ѧ��������õ�Ԫ��ԭ�ӵ�ԭ�ӽṹʾ��ͼΪ________��
(2)�Ƚ�Ԫ�آ١��ڵļ��⻯����ȶ���______________________(�û�ѧʽ��ʾ)��
(3)Ԫ�ص�����������Ӧ��ˮ������������ǿ����________��������ǿ����_______�������Ե�����������_______________��(��д��ѧʽ) Ԫ�آ۵�����������Ӧˮ�����к��еĻ�ѧ������Ϊ________________��
(4)�ڢۡ���Ԫ���У������Ӱ뾶��С����_________��
(5) Na2O2�ĵ���ʽΪ___________��CO2�ĵ���ʽΪ_________��
(6)�ڢ����ĵ����У������Խ�ǿ����_______________���û�ѧ��Ӧ����ʽ֤����_____________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������֮������ϵ�������(����)
A. O2��O3��Ϊͬ��������
B. 12C��14C��Ϊͬλ��
C. CH3CH2OH��CH3OCH3��Ϊͬ���칹��
D. CH3COOCH3��HCOOCH2CH3Ϊͬһ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���X�ĺϳ�·������ͼ��ʾ����ش��������⣺
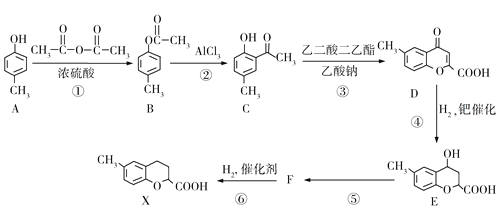
��1��A��������________________��X�ķ���ʽΪ_____________��
��2��B�ĺ˴Ź������������з�����֮����________________��
��3���л���D�к��������ŵ�������________________�����ķ�Ӧ����Ϊ________________��
��4����Ӧ���Ļ�ѧ����ʽΪ________________________________��
��5���л���F�Ľṹ��ʽΪ________________________________��
��6����������������C��ͬ���칹����_____�֣���д������һ�ֵĽṹ��ʽ_________��
��������ֻ������ȡ������
���������Ȼ�����Һ��Ӧ��ɫ��
�����Է���������Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
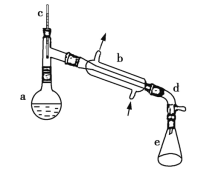
����Ŀ������ˮ�Ǻϳ�ϩ���ij��÷�����ʵ���Һϳɻ���ϩ�ķ�Ӧ��ʵ��װ����ͼ��ʾ��
![]()
![]()
![]() +H2O
+H2O
�����õ����й��������£�
��Է������� | �ܶ�/(g��cm3) | �е�/�� | �ܽ��� | |
������ | 100 | 0.961 8 | 161 | ����ˮ |
����ϩ | 82 | 0.810 2 | 83 | ������ˮ |
�ϳɷ�Ӧ��
��a�м���20 g��������2СƬ���Ƭ����ȴ��������������1 mL Ũ���ᡣb��ͨ����ȴˮ��ʼ��������a�������������¶Ȳ�����90 �档
�����ᴿ��
��Ӧ�ֲ��ﵹ���Һ©���У��ֱ�������5%̼������Һ��ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ơ�����ͨ������õ���������ϩ10 g��
�ش��������⣺
��1��װ��b��������___________________��
��2���������Ƭ��������___________________���������һ��ʱ��������ǼӴ�Ƭ��Ӧ�ò�ȡ����ȷ������___________________ (����ȷ�𰸱��)��
A���������� B����ȴ�� C�����貹�� D����������
��3����Һ©����ʹ��ǰ����ϴ�ɾ���___________________���ڱ�ʵ���������У�����Ӧ�ôӷ�Һ©����___________________ (��Ͽڵ��������¿ڷų���)��
��4�������ᴿ�����м�����ˮ�Ȼ��Ƶ�Ŀ����___________________��
��5���ڻ���ϩ�ֲ�����������У��������õ���������____________ (����ȷ�𰸱��)��
A��Բ����ƿ B���¶ȼ� C������ƿ D������������ E��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ����Ҫ�ĺ˹�ҵԭ�ϡ������й�
����Ҫ�ĺ˹�ҵԭ�ϡ������й�![]() ��
��![]() ˵����ȷ����
˵����ȷ����
A. ![]() ԭ�Ӻ��к���92������ B.
ԭ�Ӻ��к���92������ B. ![]() ԭ�Ӻ�����143������
ԭ�Ӻ�����143������
C. ![]() ��
��![]() ��Ϊͬλ�� D.
��Ϊͬλ�� D. ![]() ��
��![]() ��Ϊͬ��������
��Ϊͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ����������4������Ԫ��Xm+��Yn�������Ӻ�����Ӳ�ṹ��ͬ�������X��Y��Ԫ�ص�������ȷ����
A. X��ԭ������С��Y��ԭ������ B. X��Y�ĺ˵����֮���ǣ�m��n��
C. X��Y����ͬһ���� D. YԪ����XԪ�ص�������֮����8��(m+n)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com