
科目:高中化学 来源: 题型:
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得.
①铝土矿的主要成分是Al2O3和SiO2等.从铝土矿中提炼Al2O3的流程如图1所示:
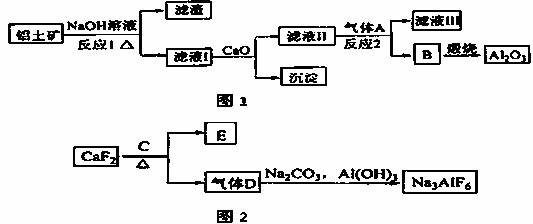
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如图2所示:
回答下列问题:
(1)写出反应1的化学方程式_____________、_______ ___;
(2)滤液Ⅰ中加入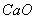 生成的沉淀是_______,若通入的气体A少量则反应2的离子方程式为_____________。
生成的沉淀是_______,若通入的气体A少量则反应2的离子方程式为_____________。
(3)E常用作制作豆腐的添加剂,化合物C是____,写出由D制备冰晶石的化学方程式______________;
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰酸的反应( )
NH3+CO2―→NNNHOOHOH+H2O
下列有关三聚氰酸的说法正确的是( )
A.分子式为C3H6N3O3
B.分子中既含极性键,又含非极性键
C.属于共价化合物
D.生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制备下列气体时,所用方法正确的是( )
A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置
B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理相同
B.制备乙酸乙酯时可用热的NaOH溶液收集产物以除去其中的乙酸
C.用饱和食盐水替代水跟电石反应,可以减缓乙炔的产生速率
D.用AgNO3溶液可以鉴别KCl和KI
查看答案和解析>>
科目:高中化学 来源: 题型:
下列不能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定 ②HClO氧化性比H2SO4强 ③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S ⑤Cl原子最外层有7个电子,S原子最外层有6个电子 ⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
A. ②⑤ B. ①② C. ①②④ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
化学反应的快慢和限度对人类生产生活有重要的意义
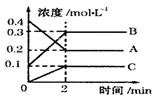
|
(1)该反应的方程式为 。
(2)2min内,C的反应速率为 。
(3)下列可作为判断反应已达到该状态的是________(填序号)。
A.A、B、C浓度相等 B.A、B的反应速率比为2∶3
C.A、B、C浓度保持不变,且不为0 D.生成A、C的速率相等
(4)对于上述反应在不同条件下的化学反应速率表示中,反应速率最快的是:( )
A、v(B) =0.8mol/(L•s) B.v(A) =0.4mol/(L•s)
C.v(C) =0.6mol/(L•s) D.v(B) =4.2mol/(L•min)
查看答案和解析>>
科目:高中化学 来源: 题型:
以铝屑为原料制备Al(OH)3实验方案的设计
(1)设计方案一:用稀硫酸跟铝屑反应,使铝转化为Al3+的溶液,再用NaOH溶液使Al(OH)3沉淀析出。
化学方程式:_________________________________。
(2)设计方案二:将铝屑跟浓NaOH溶液反应,再用稀硫酸中和过量的碱液,并促使AlO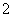 水解,以得到Al(OH)3。
水解,以得到Al(OH)3。
化学方程式:_________________________________。
(3)设计方案三:用铝屑分别与稀硫酸和浓NaOH溶液反应,然后将得到的铝盐溶液混合过滤,再将得到的沉淀洗涤,即可得到Al(OH)3。
化学方程式:_________________________________。
(4)计算方案一、方案二和方案三中酸、碱的用量填写下表:
| 方案 | 生成1 mol Al(OH)3消耗H+或OH-的物质的量/mol | |
| 消耗H+ | 消耗OH- | |
| 方案一 | ||
| 方案二 | ||
| 方案三 |
(5)对于上述三种设计方案,从反应物种类看,三种方案都使用了三种药品。从消耗酸、碱的物质的量来分析,方案________用量最多,方案________用量最少;从操作要求考虑,方案________也最为简单。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com