
【题目】(1) 良好的生态环境可以提升生活质量。
① 下列物质不属于空气质量周报中污染物的是________(填字母)。
a. SO2 b. NO2 c. PM2.5
② 垃圾应分类收集。导致“白色污染”的生活垃圾应放置于贴有________(填字母)标志的垃圾桶内。

③ 燃烧煤产生的SO2所形成的酸雨中,SO2最终转化成的酸是________(填化学式)。
(2) 右图是某品牌调料标签的一部分。

① 配料中的大量氨基酸态氮来源于黄豆中的蛋白质发生________反应得到。
② 小麦粉中的主要营养物质是________。
③ 配料表中属于防腐剂的是________。
④ 配料表中的辣椒红是着色剂。亚硝酸钠也可作着色剂,但亚硝酸钠有毒,要严格控制其用量。亚硝酸钠外观和咸味与食盐很相似,因此要防止因误食亚硝酸钠而发生事故。亚硝酸钠和氯化钠的部分性质如下表:
性质 | 亚硝酸钠 | 氯化钠 |
1. 酸性条件下的稳定性 | 微热分解为NO和NO2 | 微热时不分解 |
2. 熔点 | 271 ℃ | 801 ℃ |
3. 室温时的溶解度 | 约80 g | 约35 g |
请根据表中信息设计一种鉴别NaNO2和NaCl的方法,写出简单的操作过程、现象和结论:________。
(3) 材料是人类赖以生存和发展的重要物质基础。
① 钢铁是应用广泛的金属材料。钢铁在潮湿空气中易生锈,铁锈的主要成分是____________(填化学式),请列举一种防止钢铁腐蚀的方法:________。
② 水泥、玻璃、陶瓷是生活中常见的硅酸盐材料。制备普通玻璃的原料有CaCO3、________和________(填化学式)。青瓷是中国最早发明的瓷器,青瓷表面的绿色是釉层中的________价铁元素显色而成的。
③ 氮化硅陶瓷抗腐蚀能力强,工业上可用四氯化硅和氮气在氢气气氛中加强热发生反应制得。请写出该反应的化学方程式:________。
【答案】 c a H2SO4 水解 糖类或淀粉 苯甲酸钠 溶于水配成溶液,加入稀硫酸微热,有棕色气体生成者,原物质为NaNO2,否则为NaCl(或用酒精灯加热,熔化者为NaNO2,不熔者为NaCl;或取2支试管,各加入5 mL水,分别溶解这两种物质,至不再溶解时,溶解量大的是NaNO2,溶解量小的是NaCl) Fe2O3 涂油刷漆(或其他合理答案) Na2CO3 SiO2 +2 3SiCl4+2N2+6H2![]() Si3N4+12HCl
Si3N4+12HCl
【解析】(1) ① 属于空气污染物的是二氧化氮、二氧化硫、一氧化碳以及PM2.5等,各选项中只有二氧化碳不属于空气污染物,故选c;
②导致“白色污染”的生活垃圾主要成分是塑料,属于可回收垃圾,通过综合处理回收利用,可以减少污染,节省资源,故答案为a;
③酸雨中二氧化硫与水反应生成亚硫酸,亚硫酸不稳定,被氧气氧化为硫酸,硫酸的化学式为H2SO4;
(2) ①黄豆的成分是蛋白质,蛋白质水解生成氨基酸;
②小麦富含淀粉;
③苯甲酸钠属于防腐剂;
④由图可知,鉴别NaNO2和NaCl的方法:将两种固体分别溶于水制成溶液,再分别加入稀硫酸微热,有气泡生成的是亚硝酸钠,否则为氯化钠;
(3) ① 钢铁在潮湿空气中易生锈,铁锈的主要成分是Fe2O3,常用于防止钢铁腐蚀的方法有涂油刷漆;
②生产玻璃的原料是石灰石、纯碱和石英,其中纯碱为Na2CO3 、石英为SiO2;青瓷表面的绿色是釉层中的+2价铁元素显色而成的;
③四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,可得较高纯度的氮化硅以及氯化氢,方程式为3SiCl4+2N2+6H2![]() Si3N4+12HCl。
Si3N4+12HCl。


科目:高中化学 来源: 题型:
【题目】下列各组离子中,能在溶液中大量共存的是( )
A.H+ Na+ CO32﹣ Cl﹣
B.Ba2+ Na+Cl﹣ SO42﹣
C.K+ H+ SO42﹣OH﹣
D.Ag+ Al3+ NO3﹣H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品。苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构式如下,下列说法不正确的是

A.苹果酸在一定条件下能发生酯化反应
B.苹果酸在一定条件下能发生催化氧化反应
C.苹果酸在一定条件下能发生消去反应
D.1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如下图所示。

请回答下列问题:
(1)A的结构简式为_______________,B分子中的官能团名称为____________。
(2)反应⑦中物质X的分子式为____________,反应⑧的类型为____________。
(3)反应⑤的化学方程式为______________________________。反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是____________。
(4)已知D的相对分子量为118,其中碳、氢两元素的质量分数分别为40.68%、5.08%,其余为氧元素,则D的分子式为____________。
(5)请补充完整证明反应①是否发生的实验方案:取反应①的溶液2 mL于试管中,_________________________________________________________________________。
实验中可供选择的试剂:10%的NaOH溶液、5%的CuSO4溶液、碘水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在等体积的NaCl、MgCl2、AlCl3三种溶液中,分别加入等量的AgNO3溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为( )
A.1:2:3
B.3:2:1
C.1:1:1
D.6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废气中的H2S通过高温热分解可制取氢气:2H2S(g)![]() 2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
2H2(g)+S2(g)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
(1)某温度时,测得反应体系中有气体1.3lmol,反应1 min后,测得气体为l.37mol,则tmin 内H2的生成速率为___________。
(2)某温度时,H2S的转化率达到最大值的依据是_____________(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c.![]() 不发生变化 d.单位时间里分解的H2S和生成的H2一样多
不发生变化 d.单位时间里分解的H2S和生成的H2一样多
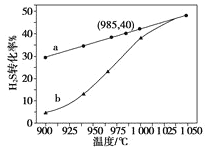
(3)实验结果如下图。图中曲线a表示H2S的平衡转化率与温度关系,曲线b表示不同温度下、反应经过相同时间且未达到化学平衡时H2S的转化率。该反应为_____反应(填“放热”或“吸热”)。曲线b随温度的升高,向曲线a通近的原因是_________。在容器体积不变的情况下,如果要提高H2的体积分数,可采取的一种措施是________。
(4)使1LH2S与20L空气(空气中O2体积分数为0.2)完全反应后恢复到室温,混合气体的体积是______L 。若2gH2S完全燃烧后生成二氧化硫和水蒸气,同时放出29.4 kJ的热量,该反应的热化学方程式是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如下图所示。A是黑色非金属单质,C、E、F均为氧化物,E、F常温下呈气态,且E能使品红褪色,G是一种常见的无色液体,I是一种难溶于水的白色胶状沉淀,能溶于B溶液。请回答下列问题:

(1) C的化学式为________。
(2)G的电子式为________。
(3)写出①反应的化学方程式:_______________________________________________。
(4)写出过量的F参加反应时②的离子方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行一氯取代反应后,只能生成三种沸点不同的烷烃的是( )
A.(CH3)2CHCH2CH2CH3
B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2
D.(CH3)3CCH2CH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com