
| A、CHCl3是正四面体形 |
| B、H2O分子中氧原子为sp2杂化,其分子几何构型为V形 |
| C、二氧化碳中碳原子为sp杂化,为直线形分子 |
| D、NH4+是三角锥形 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此反应可在瞬间产生大量高温气体,推动火箭飞行 |
| B、此反应是氧化还原反应,N2O4是氧化剂 |
| C、每生成1mol N2,该反应转移电子8mol |
| D、此反应中R的分子式为C2H8N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2既是氧化产物又是还原产物 |
| B、当x=1时,每生成2.5 mol N2,被氧化的气体有3 mol |
| C、当x=2时,有1 mol气体被还原,转移电子4 mol |
| D、反应通式配平表示为:6NOx+4xNH3═(3+2x)N2+6xH2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
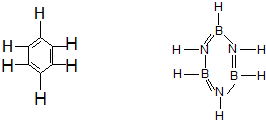 已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图所示,则硼氮苯的二氯取代物的同分异构体的数目为 ( )
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图所示,则硼氮苯的二氯取代物的同分异构体的数目为 ( )| A、6 | B、4 | C、3 | D、2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、②③ |
| C、②③④ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2+H2O═H2SO3 | ||||
B、C+CO2
| ||||
C、H2+CuO
| ||||
D、CaCO3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第二周期氢化物易燃性:CH4<NH3<H2O( ) |
| B、第三周期氢化物稳定性:SiH4>PH3>H2S>HCl |
| C、化合物毒性:若PH3>NH3,则H2S>H2O |
| D、氢化物的还原性:HF>H2O>NH3>CH4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com