
����Ŀ����ͼ1��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ� 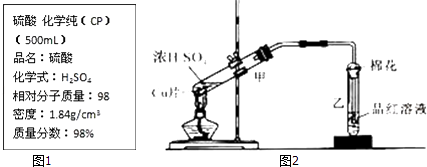
��1�����������A��D��ʾ�����ʣ����¹�����Ҫ������Ũ�������Щ���ʣ��뽫ѡ����ĸ�������и�С��������ڣ�
A���� B ��ˮ�� C ��ˮ�� D ǿ������
��Ũ������Ը�������
��Ũ����ʹľ�����
���ȵ�Ũ������ͭƬ��Ӧ
��Ũ����ʹ������Ϊ��ɫ
��2�������ø�Ũ��������100mL 1mol/L��ϡ���ᣮ�ɹ�ѡ�õ������У�
�ٽ�ͷ�ιܣ�����ƿ�����ձ�����ҩ�ף�����Ͳ����������ƽ��
��ش��������⣺
��i������ϡ����ʱ�����������в���Ҫʹ�õ�����ѡ����ţ�����ȱ�ٵIJ�����������д�������ƣ���
��ii�������㣬����100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������ΪmL������һλС������
��3������ͼ2ΪŨ������ͭƬ��Ӧ��װ�ã���ش�
��Ũ������ͭƬ��Ӧ�Ļ�ѧ����ʽΪ ��
�ڷ�Ӧһ��ʱ����Թ�����Ʒ����Һ�������� ��
���𰸡�
��1��B��C��AD��B
��2���ڢܢޣ�100m����ƿ����������5.4
��3��Cu+2H2SO4��Ũ�� ![]() ?CuSO4+SO2��+2H2O��Ʒ����Һ��ɫ
?CuSO4+SO2��+2H2O��Ʒ����Һ��ɫ
���������⣺��1.����Ũ������Ը�������������ΪŨ���������ˮ�ԣ���ѡ��B����Ũ����ʹľ����ڣ�����Ũ�������ˮ�ԣ���ѡ��C�����ȵ�Ũ������ͭƬ��Ӧ��������ͭ�����������ˮ�����Ჿ�ֱ���ǿ�����ԣ����ֱ������ԣ���ѡ��AD����Ũ�������յ����еĽᾧˮʹ������Ϊ��ɫ����Ũ�������ˮ�ԣ���ѡ��B��
��2.����i����100mL 1mol/L��ϡ��������Ʋ����У����㡢��ȡ��ϡ�͡���ȴ����Һ��ϴ����Һ�����ݡ�ҡ�ȵȲ�����һ������Ͳ��ȡ���õ���ͷ�ιܣ������ձ���ϡ�ͣ����ò��������裬��ȴ��ת�Ƶ�100mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ��μ�����Һ������̶���ˮƽ���У��Ǻ�ƿ����ҡ�ȣ���Ҫʹ�õ�����Ϊ����Ͳ���ձ�����������100mL����ƿ����ͷ�ιܣ����Բ���Ҫ������Ϊ���ڢܢޣ���ȱ�ٵ�����Ϊ����������100mL����ƿ�����Դ��ǣ��ڢܢޣ���������100mL����ƿ����ii��ͼʾ��Ũ��������ʵ���Ũ��Ϊ��c= ![]() mol/L=18.4mol/L������100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ��
mol/L=18.4mol/L������100mL1mol/L��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ�� ![]() ��0.0054L=5.4mL�����Դ��ǣ�5.4��
��0.0054L=5.4mL�����Դ��ǣ�5.4��
��3.����ͭ��Ũ�����ڼ��������·�Ӧ��������ͭ�����������ˮ������ʽ��Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O�����Դ��ǣ�Cu+2H2SO4��Ũ��
CuSO4+SO2��+2H2O�����Դ��ǣ�Cu+2H2SO4��Ũ�� ![]() CuSO4+SO2��+2H2O���ڶ����������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ��
CuSO4+SO2��+2H2O���ڶ����������Ư���ԣ��ܹ�ʹƷ����Һ��ɫ�����Դ��ǣ�Ʒ����Һ��ɫ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������[(NH4)3Fe( C6 H5O7)2��Ħ������488 g/mol] ��һ����Ҫ��ʳƷ���Ӽ���һ���Ʊ���������淋�ʵ�鲽�����£�

����1������ͼ������ƿ�м���16.7 g FeSO4��7H2O��40 ml.����ˮ��3mL�����1 g NaClO3��ǿ�����裻
����2��������80�����ٲ���l g NaClO3��
����3����Ӧ���м���NaOH��Һ���¶ȿ�����80��90�������ҽ��裻
����4�����ˣ�ϴ�ӣ����ɣ��û���Fe(OH)3��
����5����Fe(OH)3��һ������ˮ����������ƿ�У�����95�����ϣ��������������������Һ�����裬������1h��
����6����ȴ��50���������¼��백ˮ40 mL�����á�Ũ������״��80����������������24.9 g��
�ش��������⣺
��1������1������Ӧ�����ӷ���ʽΪ_____________________________��
��2������2�ٲ���NaClO3��Ŀ����_____________________________��
��3������3ȷ��Fe3+�ѳ�����ȫ�ķ�����_____________________________��
��4������4����ʱ��������������������ձ��⣬����Ҫ_____________________________��֤��Fe(OH)3�ѱ�ϴ�Ӹɾ��ķ���Ϊ__________________________��
��5����������淋IJ���Ϊ_________�����������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ģ�����˹���Ҷ���绯ѧװ����ͼ��ʾ����װ���ܽ�H2O��CO2ת��Ϊ����(C6H12O6)��O2��X��Y����������͵缫����֪��װ�õĵ���Ч�ʵ������ɲ�Ʒ����ĵ��������·��ͨ���ܵ�����֮�ȡ�����˵���������ǣ�������

A. ��װ����Y�缫����������Ӧ
B. X�缫�ĵ缫��ӦʽΪ 6CO2+24H++24e��=== C6H12O6+6H2O
C. �����ϣ�ÿ����22.4 L(��״���£�O2������4 mol H+��X������Y����Ǩ��
D. ����·��ͨ��3 mol eʱ������18 g C6H12O6�����װ�õĵ���Ч��Ϊ80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӷ���ʽCO32��+2H+�TH2O+CO2����CO32���Ĵ��������ʿ����ǣ� ��
A.CaCO3
B.NaHCO3
C.Na2CO3
D.BaCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������������Һ�д����������(����)
A. Ag����K����Cl����NO3��
B. Ba2����Cl����H����SO42��
C. H����CO32����Cl����Na��
D. Na����Ba2����OH����NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ʹ�÷�����ʵ�������ȷ���ǣ� ��
A.�ü�ʽ�ζ�����ȡ13.60mL���Ը��������Һ
B.�ⶨ����ͭ����ᾧˮ����ʱ�����Ⱥ���������ڸ���������ȴ���ٳ���
C.����ʱ��Ӧʹ�¶ȼ�ˮ������������Һ����
D.����ʱ���Ƚ���ֽʪ��Ȼ���ٽ���ֽ����©����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��̻��������ڵ����ʱ��Ե���
A.�ڼ�������Һ�м��뱥���Ȼ�����Һ
B.���켦��
C.ʹ�ü�ȩ��Һ���ݶ���걾
D.ҽ�þƾ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ɫ��Һ������Ӧ�ų������������������ڸ���Һ��һ�����Դ������ڵ���
A. Na+ B. OH�� C. NH4+ D. HCO3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com