
【题目】氮及其化合物的转化过程如图所示,下列分析合理的是
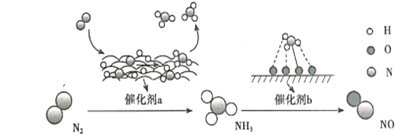
A. 催化剂a表面发生了极性共价键的断裂和形成
B. 在催化剂b表面形成氮氧键时,不涉及电子转移
C. N2与H2反应生成NH3的原子利用率为100%
D. 催化剂a、b能提高反应的平衡转化率
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
【题目】已知元素镓和砷的单质及其化合物在工业生产上有重要的用途。回答下列问题:
(1)砷元素基态原子的电子排布式为_______________________。
(2)砷与氢元素可形成化合物砷化氢,该化合物的空间构型为_____________,其中砷原子的杂化方式为__________。
(3)根据等电子原理,写出由短周期元素组成且与砷化氢互为等电子体的一种离子的化学式________。
(4)已知由元素砷与镓元素组成的化合物A为第三代半导体。已知化合物A的晶胞结构与金刚石相似,其中砷原子位于立方体内,镓原子位于立方体顶点和面心,请写出化合物A的化学式____________;
(5)已知铝与镓元素位于同一主族,金属铝属立方晶系,其晶胞边长为405 pm,密度是2.70g·cm-3,通过计算确定铝原子在三维空间中堆积方式________________(已知NA=6.02×1023,1pm=10-10cm,4053=6.64×107);晶胞中距离最近的铝原子可看作是接触的,列式计算铝的原子半径r(A1)=______pm.(只列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用如图装置模拟在A池中实现铁上镀铜,在C装置中实现工业KCl制取KOH溶液。
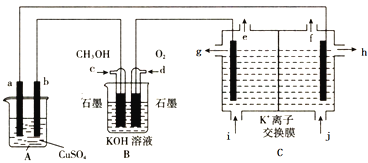
下列有关说法错误的是
A. a为精铜,b为铁制品可实现镀铜要求
B. c为负极,电极反应式为CH3OH+8OH--6e-=CO32-+6H2O
C. 从e出来的气体为氧气,从f出来的气体为氢气
D. 钾离子从电解槽左室向右室迁移,h口出来的为高浓度的KOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下:

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等; ②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:______________。
(2)浸出液中加入NaClO3的目的是____________________________。
(3)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是_____(填化学式)。
(4)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是______;其使用的适宜pH范围是___。

A.2.02.5 B.3.03.5 C.4.04.5
(5)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。己知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量 NaF后,所得滤液 c(Mg2+)/c(Ca2+) =____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 水合铜离子的模型如图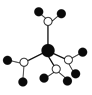 ,1个水合铜离子中有4个配位键
,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图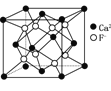 ,每个CaF2晶胞平均占有4个Ca2+
,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图 ,H原子核外大多数电子在原子核附近运动
,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图 ,为面心立方最密堆积,每个Cu原子的配位数均为12
,为面心立方最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.15g14CO与15N2的混合气体所含质子数为7.5NA
B.11.2LCl2与NaOH溶液反应转移电子数为0.5NA
C.2molSO2与1mol02反应生成SO3的分子数为2NA
D.48gO2和O3的混合气体中含有3NA个氧原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呋喃甲酸(![]() )俗名糠酸,其在塑料工业中可用作增塑剂、热固性树脂等。呋喃甲酸可由呋喃甲醛制备,其制备原理如下所示:
)俗名糠酸,其在塑料工业中可用作增塑剂、热固性树脂等。呋喃甲酸可由呋喃甲醛制备,其制备原理如下所示:
反应1: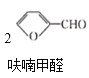 +NaOH→
+NaOH→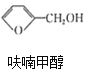 +
+![]() ;
;
反应2:![]() +HCl→
+HCl→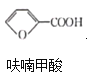 +NaCl;
+NaCl;
已知:I、反应1是放热反应;
II、乙醚的沸点是34.6℃,易挥发,遇明火易燃,其蒸气可使人失去知觉;
III、呋喃甲酸的溶解度随温度的升高而升高,且升温过程中溶解度变化较大;
实验步骤:向三颈烧瓶中加入16.4mL(约0.2mol)呋喃甲醛按以下流程图制备并获得粗品,粗品进一步提纯得到精产品9.5g
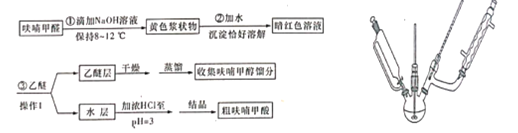
(1)若用如上图装置作为反应1的发生装置图中有一处明显错误的地方是________。
(2)步骤①中,为控制反应温度在8~12℃,可采取的措施有①____________;②________。
(3)操作1的名称为__________,要用到的玻璃仪器有______。
(4)在对乙醚层进行分离时,用下图中的_______(填字母代号)装置更好,与另一装置相比,该装置具有以下优点:
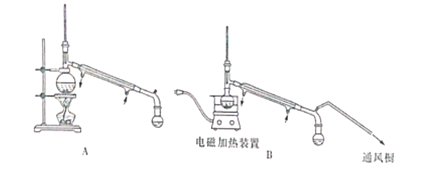
①______________;②___________。
(5)经过结晶得到的粗呋喃甲酸若要进一步提纯,要经过热水溶解→活性炭脱色→蒸发→浓缩→_______→______→抽滤→洗涤→干燥。
(6)呋喃甲酸的产率为______(保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吡洛芬是一种用于治疗风湿病的药物。它的合成路线如下:

已知:
①![]() (易被氧化)
(易被氧化)
②![]() +RCH2X
+RCH2X![]() +NaX
+NaX
回答下列问题:
(1)B→C的反应类型为______________________________。
(2)A→B的化学方程式为___________________________________________________。
(3)从整个合成路线看,步骤A→B的目的是__________________________________________________。
(4)E的结构简式为____________________________。
(5)非那西汀是一种解热药,其结构简式为![]() 。写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)__________________________。
。写出以苯酚钠、CH3CH2OH和(CH3CO)2O为原料制备非那西汀的合成路线流程图(无机试剂任用)__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将15.2 g 铜和镁组成的混合物加入250 mL4.0molL-1的稀硝酸中,固体完全溶解,生成的气体只有NO。向所得溶液中加入1.0L NaOH溶液,此时金属离子恰好沉淀完全,沉淀质量为25.4 g,下列说法正确的是
A.原固体混合物中,Cu和Mg的物质的量之比为1:2
B.氢氧化钠溶液的浓度为0.8 mol·L-1
C.固体溶解后的溶液中硝酸的物质的量为0.1mol
D.生成的NO气体在标况下的体积为2.24 L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com