
【题目】在体积为1 L的密闭容器中(体积不变)充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
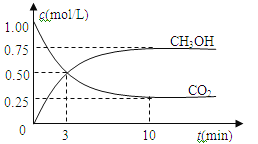
A.进行到3分钟时,正反应速率和逆反应速率相等
B.10分钟后容器中各物质浓度不再改变
C.达到平衡后,升高温度,正反应速率增大、逆反应速率减小
D.3min前v正>v逆,3min后v正<v逆
科目:高中化学 来源: 题型:
【题目】过渡金属钯催化的偶联反应是近年来有机合成的热点之一,如反应①:
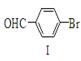 +
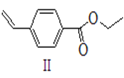
+
![]()

化合物II可由以下合成路线获得:
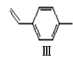
![]() Ⅳ
Ⅳ![]() Ⅴ
Ⅴ![]() Ⅵ
Ⅵ![]()
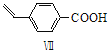
![]() Ⅱ
Ⅱ
(1)化合物I所含官能团的名称为_____________,化合物II的分子式为_____________。
(2)化合物IV的结构简式为__________,某同学设想无需经反应②、③、④和⑤,直接用酸性KMnO4溶液就可将化合物III氧化为化合物VII,该设想明显不合理,其理由是____________。
(3)化合物VII有多种同分异构体,请写出一种符合下列要求的结构简式____________。
①苯环上有两个取代基
②1 mol 该物质发生银镜反应能生成4 mol Ag
(4)反应⑥的化学方程式为____________。(注明条件)
(5)化合物![]() 与化合物
与化合物![]() 在一定条件下按物质的量之比1∶2可发生类似反应①的反应,请写出其产物的结构简式____________。
在一定条件下按物质的量之比1∶2可发生类似反应①的反应,请写出其产物的结构简式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮可以形成多种离子,如N3-,NH2-,N3-,NH4+,N2H5+,N2H62+等,已知N2H5+与N2H62+是由中性分子结合质子形成的,类似于NH4+,因此有类似于NH4+的性质。
⑴写出N2H62+在碱性溶液中反应的离子方程式_________;
⑵NH2-的电子式为_________;
⑶N3-有_______个电子;
⑷写出二种由多个原子组成的含有与N3-电子数相同的物质的化学式_________;
⑸等电子数的微粒往往具有相似的结构,试预测N3-的构型_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】党的十九大,继续倡导可持续发展理念,建设健康和谐美丽中国。下列错误的是
A.利用垃圾焚烧产生的热能发电或供热,从而充分地利用生活垃圾中的生物质能
B.通过煤的液化、气化等物理方法可以将煤转化为CO、![]() 等燃料,提高煤燃烧的热效率
等燃料,提高煤燃烧的热效率
C.推出共享单车,呼吁全民绿色出行,从而减少汽车尾气的排放
D.推广使用天然气和液化石油气等清洁燃料,从而减少大气污染物的排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于自然资源开发利用的说法错误的是
A.根据金属活泼性不同,冶炼金属采用的方法不同
B.通过煤的气化和液化等化学变化可将煤变为清洁能源
C.以石油、煤和天然气为原料可生产塑料、合成橡胶和合成纤维
D.从海带中提取碘经历的步骤有:灼烧![]() 浸泡
浸泡![]() 过滤
过滤![]() 萃取
萃取![]() 粗碘提纯
粗碘提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在3种不同条件下,分别向容积为1L的恒容密闭容器中充入4molA和2molB,发生反应:2A(g)+B(g)![]() 2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
2D(g) △H=QkJ/mol,相关条件和数据见表。下列说法正确的是( )
实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 5 | 30 |
n(D)平衡/mol | 3 | 3 | 2 |
化学平衡常数 | K1 | K2 | K3 |
A.实验Ⅲ达平衡后,恒温下再向容器中通入2 molA和2 molD,平衡正向移动
B.升高温度能加快反应速率的原理是降低了活化能,使活化分子百分数提高
C.实验Ⅰ达平衡后容器内的压强是实验Ⅲ的0.9倍
D.K3<K2 =K1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用如图装置进行中和热的测定。回答下列问题:
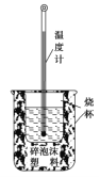
(1)该图中有两处未画出,它们是 ____________、_______________;
(2)在操作正确的前提下提高中和热测定的准确性的关键是____________________;
(3)如果用50 mL0.50 mol/L的盐酸和0.03 mol氢氧化钠固体进行实验,则实验中所测出的“中和热”的热值将____________(填“偏大”、“偏小”或“不变”);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的两种方法:
方法a | 用炭粉在高温条件下还原CuO |
方法b | 电解法,反应为2Cu+H2O |
(1)工业上常用方法b制取Cu2O而很少用方法a,其原因是反应条件不易控制,若控温不当易生成__________而使Cu2O产率降低。
(2)已知:①2Cu(s)+ ![]() O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
O2(g)=Cu2O(s) ΔH1=-169 kJ·mol-1
②C(s)+ ![]() O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH2=-110.5 kJ·mol-1
③Cu(s)+ ![]() O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
O2(g)=CuO(s) ΔH3=-157 kJ·mol-1
则方法a中发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=________。
(3)方法b是用肼燃料电池为电源,通过离子交换膜电解法控制电解液中OH-的浓度来制备纳米Cu2O,装置如图所示:
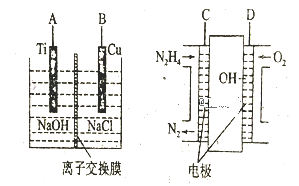
①上述装置中B电极应连_________电极(填“C”或“D”)。
②该离子交换膜为____离子交换膜(填“阴”或“阳”),该电解池的阳极反应式为_______。
③原电池中负极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关元素及其化合物叙述中不正确的是( )
A.氧化镁和氧化铝熔点均很高,常用作耐高温材料
B.在酒精灯加热条件下,![]() 和
和![]() 固体都能分解
固体都能分解
C.二氧化氯具有氧化性,可用于自来水杀菌消毒
D.电闪雷鸣的雨天,![]() 与
与![]() 会发生反应并最终转化为硝酸盐被植物吸收
会发生反应并最终转化为硝酸盐被植物吸收
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com