
【题目】两种气态烃以任意比例混合,在150℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,下列各组混合烃中符合此条件的是( )
A.CH4 和C2H4B.CH4 和C3H6C.C2H2 和C3H4D.C2H2 和C2H6
【答案】A
【解析】
令平均组成为CxHy,则CxHy+(x+![]() )O2→xCO2+
)O2→xCO2+![]() H2O,因为150℃时,生成的H2O是气体,因反应前后气体的体积不变,所以1+x+
H2O,因为150℃时,生成的H2O是气体,因反应前后气体的体积不变,所以1+x+![]() =x+
=x+![]() ,解得y=4,由于两种气态烃以任意比例混合,故混合烃中各组分分子式中H原子数目为4符合题意。
,解得y=4,由于两种气态烃以任意比例混合,故混合烃中各组分分子式中H原子数目为4符合题意。
A.CH4、C2H4中H原子数都为4,符合题意,故A符合题意;
B.CH4、C3H6中H原子数分别为4、6,平均值不可能为4,故B不符合题意;
C.C2H2、C3H4中H原子数分别为2、4,平均值不可能为4,故C不符合题意;
D.C2H2 和C2H6中H原子数分别为2、6,当二者比例为1:1时,H原子平均值为4,但其它比例时,H原子平均值不为4,故D不符合题意;
故答案为:A。


科目:高中化学 来源: 题型:
【题目】某实验小组将SO2通入Na2S和Na2SO3的混合溶液中制备硫代硫酸钠(Na2S2O3)。其装置如下图所示(省略夹持装置),下列说法错误的是
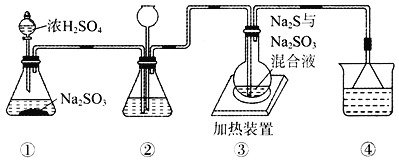
A. 装置②的作用之一是观察SO2的生成速率,其中的液体可以是饱和NaHSO3溶液
B. 为提高产品纯度,使烧瓶中Na2S和Na2SO3恰好完全反应,则![]()
C. 装置④的作用是吸收尾气,同时防止倒吸
D. 装置①也可用于高锰酸钾与浓盐酸反应制备氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法正确的是

A. 五种元素中,原子半径最大的是W
B. Y与Z形成的化合物都可以和盐酸反应
C. 简单阴离子的还原性:Y>W
D. Z与Q形成的化合物水溶液一定显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表给出了五种元素的相关信息,其中![]() 、
、![]() 、
、![]() 、
、![]() 为短周期元素。
为短周期元素。
元素 | 相关信息 |
| 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| 工业上通过分离液态空气获得它的一种单质,含它的另一种单质的浓度相对较高的平流层是保护地球地表环境的重要屏障 |
| 植物生长所需的主要元素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| 室温下其单质为粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| 它是人体不可缺少的微量元素,含该元素的合金是工业生产中不可缺少的金属材料,常用于建造桥梁、楼房等 |
根据上述信息填空:
(1)![]() 元素的原子含有________个能层,其中第二能层中的能级包括_________;画出
元素的原子含有________个能层,其中第二能层中的能级包括_________;画出![]() 的原子结构示意图:________________。
的原子结构示意图:________________。
(2)![]() 与
与![]() 形成的某种化合物能和
形成的某种化合物能和![]() 与
与![]() 形成的另一种无色化合物(这两种化合物分子中
形成的另一种无色化合物(这两种化合物分子中![]() 与另一元素原子的个数比均为
与另一元素原子的个数比均为![]() )一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:__________________________________。
)一起用作火箭推进剂,写出二者发生反应生成无毒物质的化学方程式:__________________________________。
(3)某矿藏主要含![]() 、
、![]() 两种元素组成的化合物,它是我国生产某强酸的主要原料。试写出生产该强酸过程中第一阶段主要反应的化学方程式:________。
两种元素组成的化合物,它是我国生产某强酸的主要原料。试写出生产该强酸过程中第一阶段主要反应的化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列几种有机化合物的结构简式:(选填序号,下同)
①CH3CH═CH﹣CH2CH3 ② ③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥
③CH3CH2﹣CH2﹣CH2OH ④CH3﹣C≡C﹣CH3 ⑤CH3﹣CH2﹣C≡CH ⑥![]()
⑦CH3CH2CH2OCH3 ⑧![]() ⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
⑨CH2═CH﹣CH═CH2 ⑩CH2═CH﹣CH2CH2CH3
(1)互为同分异构体的是______________ (2)互为同系物的是___________
(3)官能团位置不同的同分异构体是_______ (4)官能团类型不同的同分异构体是__
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室在蒸馏烧瓶中加NaBr、适量水、95%的乙醇和浓硫酸,用酒精灯对烧瓶微热,边反应边蒸馏,蒸出的溴乙烷用水下收集法获得。其中可能发生的副反应有:2HBr+H2SO4(浓)→Br2+SO2![]() +2H2O
+2H2O
完成下列填空:
(1)制备溴乙烷的化学方程式为:_________、_______。
(2)反应中加入少量水不能产生的作用是__________(选填编号)
A 防止溴乙烷被浓硫酸氧化 B 减少溴化氢的挥发
C 使反应混合物分层 D 溶解溴化钠
(3)为了保证容器均匀受热和控制恒温,加热方法最好采用________。
(4)采用边反应边蒸馏的操作设计,其主要目的是_________。
(5)溴乙烷可用水下收集法获得的依据是___________。
(6)下列装置在实验中既能吸收HBr气体,又能防止液体倒吸的是__________(选填编号)
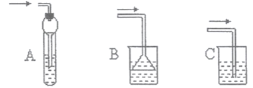
(7)粗产品用水洗涤后有机层仍呈红棕色,欲除去该杂质,可加入的试剂为________(选填编号)
A 碘化钾溶液 B 亚硫酸钠溶液 C 氢氧化钠溶液
(8)以下步骤,可用于检验溴乙烷中溴元素,其正确的操作顺序是:取少量溴乙烷,然后_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是
A. I中气体由无色变红棕色的化学方程式:2NO+O2=2NO2
B. II中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对比I、II中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是_________(用离子方程式表示)
(2)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式_________________。
(3)室温下将0.12 mol/L HCl溶液与0.1 mol/L NaOH溶液等体积混合,混合液的pH=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 某有机物
某有机物![]() 与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重
与足量的氧气充分反应后,将所得气体产物依次通过盛有浓硫酸和碱石灰的装置,两装置分别增重![]() 、
、![]() ;同温同压下,
;同温同压下,![]() 蒸气的密度是
蒸气的密度是![]() 的37倍。则能够与钠反应放出
的37倍。则能够与钠反应放出![]() 的
的![]() 的结构有(不考虑立体异构)( )
的结构有(不考虑立体异构)( )
A.6种B.5种C.4种D.3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com